- Общая характеристика
- МНН
- Описание
- Состав
- Форма выпуска
- Фармакотерапевтическая группа
- Фармакологические свойства
- Показания к применению
- Способ применения и дозировка
- Побочные действия
- Противопоказания
- Передозировка
- Меры предосторожности
- Дети
- Период беременности
- Управление автомобилем
- Взаимодействие
- Условия и срок хранения
- Упаковка
- Правила отпуска
- Информация о производителе
Валарокс инструкция по применению
Официальная инструкция лекарственного препарата Валарокс таблетки 10мг/80мг, 10мг/160мг, 20мг/80мг, 20мг/160мг. Описание и применение Valaroks, аналоги и отзывы. Инструкция Валарокс таблетки утвержденная компанией производителем.
Общая характеристика
Международное непатентованное наименование
Rosuvastatin and valsartan.
Описание
Таблетки, покрытые пленочной оболочкой темно-розового цвета, круглые, слегка двояковыпуклые, со скошенными краями и выгравированной меткой К4 на одной стороне (10мг/80мг).
Таблетки, покрытые пленочной оболочкой темно-розового цвета, капсуловидные, слегка двояковыпуклые, с выгравированной меткой К3 на одной стороне (20мг/80мг).
Таблетки, покрытые пленочной оболочкой темно-розового цвета, овальные, двояковыпуклые, с выгравированной меткой К2 на одной стороне (10мг/160мг).
Таблетки, покрытые пленочной оболочкой слегка коричневато-желтого цвета, овальные, двояковыпуклые, с выгравированной меткой К1 на одной стороне (20мг/160мг).
Состав лекарственного средства
10 мг/80 мг:
| 1 таб. | |
| розувастатин (в виде розувастатина кальция) | 10 мг |
| валсартан | 80 мг |
Вспомогательные вещества: целлюлоза микрокристаллическая тип 102, лактоза моногидрат 85.5, кроскармеллоза натрия, кремния диоксид коллоидный безводный, магния стеарат, маннитол, повидон К25, натрия лаурилсульфат, железа оксид желтый (Е172).
Состав покрывающей смеси (оболочки): поливиниловый спирт, титана диоксид (Е 171), макрогол 3350, тальк, железа оксид красный (Е 172).
20 мг/80 мг:
| 1 таб. | |
| розувастатин (в виде розувастатина кальция) | 20 мг |
| валсартан | 80 мг |
Вспомогательные вещества: целлюлоза микрокристаллическая тип 102, лактоза моногидрат 171 мг, кроскармеллоза натрия, кремния диоксид коллоидный безводный, магния стеарат, маннитол, повидон К25, натрия лаурилсульфат, железа оксид желтый (Е172).
Состав покрывающей смеси (оболочки): поливиниловый спирт, титана диоксид (Е 171), макрогол 3350, тальк, железа оксид красный (Е 172).
10 мг/160 мг:
| 1 таб. | |
| розувастатин (в виде розувастатина кальция) | 10 мг |
| валсартан | 160 мг |
Вспомогательные вещества: целлюлоза микрокристаллическая тип 102, лактоза моногидрат 180.89 мг, кроскармеллоза натрия, кремния диоксид коллоидный безводный, магния стеарат, маннитол, повидон К25, натрия лаурилсульфат, железа оксид желтый (Е172).
Состав покрывающей смеси (оболочки): поливиниловый спирт, титана диоксид (Е 171), макрогол 3350, тальк, железа оксид красный (Е 172).
20 мг/160 мг:
| 1 таб. | |
| розувастатин (в виде розувастатина кальция) | 20 мг |
| валсартан | 160 мг |
Вспомогательные вещества: целлюлоза микрокристаллическая тип 102, лактоза моногидрат 171 мг, кроскармеллоза натрия, кремния диоксид коллоидный безводный, магния стеарат, маннитол, повидон К25, натрия лаурилсульфат, железа оксид желтый (Е172).
Состав покрывающей смеси (оболочки): поливиниловый спирт, титана диоксид (Е 171), макрогол 3350, тальк.
Форма выпуска
Таблетки, покрытые пленочной оболочкой.
Фармакотерапевтическая группа
Гиполипидемические средства. Ингибиторы ГМГ-КоА-редуктазы, другие композиции.
Код ATС C10BX10.
Фармакологические свойства
Фармакодинамика.
Валсартан Валсартан является активным и специфическим антагонистом рецепторов ангиотензина II, предназначенным для внутреннего применения. Он действует избирательно на рецепторы подтипа АТ1, ответственные за эффекты ангиотензина II. Повышенные уровни ангиотензина II вследствие блокады АТ1-рецепторов валсартаном могут стимулировать незаблокированные АТ2-рецепторы, обладающие противоположными АТ1-рецепторами эффектами. Валсартан не имеет агонистической активности в отношении АТ1-рецепторов и имеет гораздо большее (приблизительно в 20000 раз) сродство с АТ1-рецепторами, чем с АТ2-рецепторами. Неизвестно случаев, когда валсартан вступал бы во взаимодействие или блокировал рецепторы других гормонов или ионные каналы, которые, как известно, играют важную роль в регуляции функций сердечно-сосудистой системы.
Валсартан не подавляет ангиотензинпревращающий фермент (АПФ), известный также под названием кининазы II, который превращает ангиотензин I в ангиотензин II и разрушает брадикинин. Поскольку валсартан не влияет на АПФ и соответственно не повышает уровни брадикинина или субстанции P, маловероятно, что он будет ассоциироваться с кашлем. В клинических исследованиях, где валсартан сравнивался с ингибитором АПФ, частота случаев сухого кашля была значительно меньше (Р < 0,05) у пациентов, лечившихся валсартаном, чем у пациентов, принимавших ингибитор АПФ (2,6% по сравнению с 7,9% соответственно). У пациентов, ранее лечившихся ингибитором АПФ, развивался сухой кашель, при лечении валсартаном это осложнение было отмечено в 19,5% случаев, а при лечении тиазидным диуретиком — в 19% случаев, в то время как в группе больных, получавших лечение ингибитором. АПФ, кашель наблюдался в 68,5% случаев (Р < 0,05).
Артериальная гипертензия Применение препарата пациентам с артериальной гипертензией приводит к снижению АД, не влияя при этом на частоту пульса. У большинства пациентов после назначения разовой дозы препарата внутрь антигипертензивный эффект развивается в течение 2 часов, а максимальное снижение АД достигается в пределах 4—6 часов. Антигипертензивный эффект сохраняется более 24 ч после приема разовой дозы препарата. При регулярном применении препарата максимальный терапевтический эффект обычно достигается в течение 2—4 недель и удерживается на достигнутом уровне в ходе длительной терапии. В сочетании с гидрохлоротиазидом достигается значительное дополнительное снижение артериального давления (АД). Внезапная отмена валсартана не приводит к восстановлению артериальной гипертензии или к другим побочным клиническим явлениям. Другое: двойная блокада ренин-ангиотензин-альдостероновой системы (РААС) При применении комбинации ингибитора АПФ с блокатором рецепторов ангиотензина II у пациентов с наличием в анамнезе сердечно-сосудистого или цереброваскулярного заболевания, или сахарного диабета 2 типа и у пациентов с сахарным диабетом 2 типа и диабетической нефропатией по сравнению с монотерапией наблюдался повышенный риск развития гиперкалиемии, острого поражения почек и/или гипотензии.
Принимая во внимание их подобные фармакодинамические свойства, эти последствия также действительны для других ингибиторов АПФ и блокаторов рецепторов ангиотензина II. Таким образом, ингибиторы АПФ и блокаторы рецепторов ангиотензина II не следует одновременно применять пациентам, страдающим диабетической нефропатией. При добавлении алискирена к стандартной терапии ингибитором АПФ или блокатором рецепторов ангиотензина II у пациентов с сахарным диабетом 2 типа и хроническим заболеванием почек, сердечно-сосудистым заболеванием или и тем и другим случаи смертей в результате сердечно-сосудистой патологии и инсульта были (в численном отношении) более частыми в группе приема алискирена, чем в группе приема плацебо, а о побочных явлениях и серьезных побочных явлениях, представляющих особый интерес (гиперкалиемия, гипотензия и печеночная дисфункция), сообщалось чаще в группе приема алискирена, чем в группе приема плацебо.
Розувастатин
Розувастатин является селективным конкурентным ингибитором ГМГ-КоА-редуктазы, фермента, который определяет скорость реакции и превращает 3-гидрокси-3-метилглутарил-коэнзим А в мевалонат, предшественник холестерина. Первичным местом действия розувастатина является печень, орган-мишень для снижения концентрации холестерина. Розувастатин увеличивает количество рецепторов липопротеинов низкой плотности (ЛПНП) на поверхности клеток печени, увеличивая захват и катаболизм ЛПНП, что приводит к угнетению синтеза в печени липопротеинов очень низкой плотности (ЛПОНП), уменьшая тем самым общее количество частиц ЛПНП и ЛПНП. Розувастатин снижает повышенный уровень холестерина (ХС) ЛПНП, общего холестерина и триглицеридов (ТГ), а также повышает уровень холестерина липопротеинов высокой плотности (ХС ЛПВП). Он также снижает уровень апопротеина В (АпоВ), холестерина не-ЛПВП (ХС не-ЛПВП), холестерина ЛПОНП (ХС ЛПОНП), триглицеридов ЛПОНП, а также повышает уровни апопротеина А-I (АпоА-I) (см. таблицу 1). Также розувастатин снижает соотношение ХС ЛПНП/ХС ЛПВП, общий ХС/ХС ЛВП и ХС не-ЛПВП/ХС ЛПВП и ApB/ApoA-I. Таблица 1 Эффективность дозы у пациентов с первичной гиперхолестеринемией (тип IIa и IIb) (скорректированное среднее изменение в процентах от начального уровня) Доза Количество ХС ЛПНП Общий ХС ХС ЛПВП ТГ ХС не-ЛПВП AпoB AпoA-I Плацебо 13 -7 -5 3 -3 -7 -3 0 5 17 -45 -33 13 -35 -44 -38 4 10 17 -52 -36 14 -10 -48 -42 4 20 17 -55 -40 8 -23 -51 -46 5 40 18 -63 -46 10 -28 -60 -54 0 Терапевтический эффект достигается в течение 1 недели после начала применения препарата, 90% максимального эффекта — через 2 недели. Максимальный эффект обычно достигается через 4 недели и поддерживается в дальнейшем. Розувастатин эффективен у взрослых пациентов с гиперхолестеринемией, гипертриглицеридемией или без, независимо от расы, пола или возраста, и у пациентов с сахарным диабетом или с семейной гиперхолестеринемией.
Наиболее распространенными побочными реакциями, приводящими к прекращению применения розувастатина, являются миалгия, абдоминальная боль, сыпь. Наиболее частыми побочными реакциями, которые возникали одинаково или чаще, чем при применении плацебо, являются инфекции мочевыводящей системы, назофарингит, боль в спине и миалгия.
Фармакокинетика. Всасывание Валсартан После перорального применения препарата максимальные концентрации валсартана в плазме крови (Сmax) достигаются в течение 2—4 ч, в виде раствора — через 1—2 ч. Средняя абсолютная биодоступность таблеток и раствора препарата составляет 23% и 39% соответственно. Прием пищи снижает экспозицию валсартана примерно на 40%, максимальную концентрацию в плазме крови (Сmax) примерно на 50%, хотя примерно через 8 часов после применения препарата концентрации валсартана в плазме крови аналогичны в группах приема препарата натощак и после еды. Однако такое снижение экспозиции не сопровождается клинически значимым снижением терапевтического эффекта, поэтому валсартан можно применять либо во время приема пищи, либо между приемами пищи. Розувастатин Максимальная концентрация розувастатина в плазме крови достигается через 5 ч после приема внутрь. Абсолютная биодоступность составляет около 20%.
Распределение Валсартан
Объем распределения валсартана в стабильном состоянии после введения составляет примерно 17 л, указывая на то, что валсартан не распределяется в ткани экстенсивно. Валсартан хорошо связывается с белками сыворотки крови (94—97%), в основном с альбумином. Розувастатин Розувастатин экстенсивно превращается в печени, являющейся первичным центром синтеза холестерина и клиренса холестерина ЛПНП. Объем распределения розувастатина составляет примерно 134 л. Приблизительно 90% розувастатина связываются с белками плазмы крови, главным образом с альбумином. Метаболизм Валсартан Валсартан не биотрансформируется в значительной степени, поскольку около 20% дозы выводится в форме метаболитов. Гидроксиметаболит был определен в плазме крови в малой концентрации (менее 10% AUC валсартана). Этот метаболит фармакологически неактивен.
Розувастатин
Метаболизм розувастатина ограничен (примерно 10%). Исследования метаболизма in vitro с применением гепатоцитов человека указывают на то, что розувастатин является очень слабым субстратом метаболизма на основе цитохрома Р450. CYP2C9 был основным изоферментом, участвовавшим в метаболизме, тогда как изоферменты 2С19, 3А4 и 2D6 были вовлечены в меньшей степени. Основными определенными метаболитами являются N-дезметил и лактон. Метаболит N-дезметил приблизительно на 50% менее активен, чем розувастатин, а форма лактон считается клинически неактивной. Выведение Валсартан Валсартан показывает мультиэкспоненциальную кинетику распада (t1/2α < 1 часа и t1/2β примерно 9 часов). Валсартан главным образом выводится через желчевыводящие пути с калом (около 83% дозы) и почками с мочой (около 13% дозы), в основном в неизмененном виде. После внутривенного введения плазменный клиренс валсартана составляет примерно 2 л/ч, а его почечный клиренс составляет 0,62 л/ч (около 30% общего клиренса). Период полувыведения валсартана составляет 6 часов.
Розувастатин
Приблизительно 90% дозы розувастатина выводится в неизмененном виде с калом (состоит из абсорбированного и неабсорбированного действующего вещества), а остаток выводится с мочой. Приблизительно 5% выводится в неизмененном виде с мочой. Период полувыведения составляет около 20 часов. Период полувыведения не увеличивается при высоких дозах. Среднее геометрическое значение плазменного клиренса составляет около 50 л/ч (коэффициент вариации 21,7%). Как и у других ингибиторов ГМГ-КоА-редуктазы, увлечение печенью розувастатина происходит с участием мембранного транспортера OATP-C. Этот транспортер играет немаловажную роль в выведении розувастатина из печени. Линейность/нелинейность Розувастатин Системная экспозиция розувастатина увеличивается пропорционально дозе. При приеме нескольких суточных доз фармакокинетические параметры не изменяются.
Отдельные группы пациентов. Возраст и пол На фармакокинетику розувастатина у взрослых возраст и пол значительно не влияли. Фармакокинетика розувастатина у детей и подростков с гетерозиготной семейной гиперхолестеринемией была подобна таковой у взрослых добровольцев (см. «Дети» ниже). Определенное повышение экспозиции валсартана наблюдалось у некоторых пациентов пожилого возраста по сравнению с лицами молодого возраста, однако клиническое значение этого неизвестно. Раса Фармакокинетические исследования демонстрируют повышение примерно в 2 раза медианных значений AUC и Сmax розувастатина у представителей народов Азии (японцев, китайцев, филиппинцев, вьетнамцев и корейцев) по сравнению с пациентами европеоидной расы; у индусов наблюдается увеличение примерно в 1,3 раза медианных значений AUC и Сmax. Популяционный фармакокинетический анализ не выявил клинически значимой разницы в фармакокинетике между представителями европеоидной и негроидной рас.
Нарушение функции почек
Во время исследования с участием пациентов с разной степенью нарушения функции почек изменений плазменных концентраций розувастатина или его метаболита N-дезметила в плазме крови у лиц со слабой или умеренной почечной недостаточностью не было отмечено. У пациентов с тяжелым нарушением функции почек (клиренс креатинина < 30 мл/мин) концентрация розувастатина в плазме крови увеличивалась в 3 раза, а концентрация N-дезметила — в 9 раз по сравнению с соответствующими показателями у здоровых добровольцев. Концентрации розувастатина в плазме крови в стабильном состоянии у пациентов, проходящих гемодиализ, были примерно на 50% выше, чем у здоровых добровольцев. Ожидаемо для соединений, почечный клиренс которых составляет лишь 30% общего клиренса плазмы крови, не наблюдалось никакой взаимосвязи между функцией почек и системным влиянием валсартана.
Поэтому корректировка дозы для пациентов с нарушением функции почек (клиренс креатинина > 10 мл/мин) не требуется. В настоящее время отсутствует опыт безопасного применения пациентам с клиренсом креатинина < 10 мл/мин и пациентам, находящимся на диализе, поэтому валсартан следует применять с осторожностью этой категории пациентов. Валсартан имеет высокую степень связывания с белками плазмы крови и вряд ли может быть удален с помощью гемодиализа. Нарушение функции печени В исследовании, в котором принимали участие пациенты с различными степенями нарушения функции печени, не выявлено признаков повышенного влияния розувастатина у пациентов с оценкой 7 или ниже по шкале Чайлда-Пью. Однако у двух пациентов с оценками 8 и 9 по шкале Чайлда-Пью наблюдалось увеличение системного воздействия по меньшей мере в 2 раза по сравнению с пациентами с более низкими показателями по шкале Чайлда-Пью. Опыта назначения препарата пациентам с оценкой выше 9 по шкале Чайлда-Пью нет.
Приблизительно 70% от всасываемой дозы валсартана выводится с желчью, преимущественно в неизмененном виде. Валсартан не подвергается значительной биотрансформации. В сравнении со здоровыми пациентами у больных с печеночной недостаточностью от легкой до умеренной степени наблюдалось увеличение AUC в два раза. Однако не было обнаружено никакой связи между концентрацией валсартана в плазме крови и степенью печеночной недостаточности. Действие валсартана у больных с тяжелой степенью печеночной недостаточности не изучалось. Дети Фармакокинетические показатели у педиатрических пациентов с гетерозиготной семейной гиперхолестеринемией в возрасте 10 — 17 лет не были полностью охарактеризованы. Небольшое фармакокинетическое исследование розувастатина (в форме таблеток), в котором приняли участие пациенты в возрасте младше 18 лет, показало, что влияние препарата у педиатрических пациентов соответствует влиянию препарата у взрослых пациентов. Кроме того, результаты указывают на то, что не должно быть значительного отклонения пропорционально дозам.
В исследовании с участием 26 детей с гипертонической болезнью (в возрасте 1 — 16 лет), которым назначали одну дозу суспензии валсартана (среднее значение —0,9 — 2 мг/кг, максимальная доза 80 мг), клиренс (л/ч/ кг) валсартана был сопоставим в возрастной группе 1 — 16 лет и соответствовал клиренсу у взрослых, получавших такой же препарат. Генетический полиморфизм В фармакокинетике ингибиторов редуктазы ГМГ-КоА, включая розувастатин, принимают участие транспортные белки OATP1B1 и BCRP. У больных с генетическим полиморфизмом SLCO1B1 (OATP1B1) и/или ABCG2 (BCRP) существует риск повышенного влияния розувастатина. Отдельные полиморфизмы SLCO1B1 с.521CC и ABCG2 с.421AA связаны с более высоким влиянием розувастатина (AUC) по сравнению с генотипами SLCO1B1 к.521TT или ABCG2 к.421CC. Это специфическое генотипирование обычно не используется в клинической практике, но пациентам, у которых обнаружены эти типы полиморфизма, рекомендуется меньшая суточная доза розувастатина.
Дети с нарушением функции почек
Применение препарата детям с клиренсом креатинина < 30 мл/мин и детям, которым проводят диализ, не изучалось, поэтому валсартан не рекомендуется таким пациентам. Для детей с клиренсом креатинина > 30 мл/мин коррекции дозы не требуется. Следует тщательно контролировать функцию почек и уровень калия в сыворотке крови. Клинические свойства
Валарокс Показания к применению
Валарокс показан как заместительная терапия артериальной гипертензии у взрослых пациентов, состояние которых должным образом контролируется одновременным применением валсартана и розувастатина в тех же дозировках и имеющих высокий риск первого возникновения сердечно-сосудистых осложнений (для профилактики сердечно-сосудистых осложнений) или при наличии таких условий: первичная гиперхолестеринемия (типа IIa, включая семейную гетерозиготную гиперхолестеринемию) или смешанная дислипидемия (типа IIb); гомозиготная семейная гиперхолестеринемия.
Способ применения Валарокс и дозировка
Дозировка
До начала лечения пациенту необходимо назначить стандартную гипохолестеринемическую диету, которую он должен соблюдать при лечении. Рекомендованная доза Валарокса 1 таблетка в сутки. Фиксированное сочетание не подходит для начальной терапии. До перехода на Валарокс состояние пациентов должно контролироваться стабильными дозами отдельных компонентов при одновременном применении. Доза Валарокса должна основываться на дозах отдельных компонентов комбинации в момент перехода.
Если требуется изменение дозы какого-либо действующего вещества фиксированной комбинации по любой причине (например, впервые диагностированные заболевания, изменение состояния пациента или взаимодействие лекарственных средств), отдельные компоненты должны быть применены повторно для определения дозы. Дополнительная информация о специальных группах населения Пациенты пожилого возраста Коррекция дозы не требуется. Пациенты с нарушением функции почек. У пациентов с легким и умеренным нарушением функции почек нет необходимости в коррекции дозы.
Применение Валарокса противопоказано пациентам с тяжелым нарушением функции почек (см. разделы «Противопоказания» и «Фармакокинетика»). Одновременное применение с алискиреном противопоказано пациентам с нарушением функции почек (СКФ < 60 мл/мин/1,73 м2) (см. раздел «Противопоказания»). Пациенты с нарушением функции печени Не наблюдался рост системной экспозиции розувастатина у пациентов с 7 и менее баллами по шкале Чайлда — Пью. Однако усиление системной экспозиции было отмечено у пациентов, состояние которых оценивалось в 8 и 9 баллов по шкале Чайлда — Пью. У таких пациентов следует проводить оценку функции печени.
Опыт применения препарата у лиц с показателем более 9 баллов по шкале Чайлда — Пью отсутствует. Валарокс противопоказан пациентам с заболеваниями печени в активной стадии (см. раздел «Противопоказания»), тяжелым нарушением функции печени, билиарным циррозом печени и пациентам с холестазом (см. разделы «Противопоказания», «Особенности применения» и «Фармакокинетика»). Для пациентов с легким и умеренным нарушением функции печени без холестаза доза валсартана не должна превышать 80 мг. Раса У пациентов монголоидной расы наблюдалась повышенная системная экспозиция препарата (см. разделы «Противопоказания», «Особенности применения», «Фармакокинетика»). Генетические полиморфизмы Известно, что специфические типы генетических полиморфизмов могут приводить к увеличению экспозиции розувастатина. Пациентам с наличием таких типов полиморфизма рекомендуется снизить суточную дозу розувастатина. Сопутствующая терапия Розувастатин представляет собой субстрат для различных транспортных белков (например, ОАTP1B1 и BCRP). Риск миопатии (включая рабдомиолиз) повышается при одновременном применении розувастатина с определенными лекарственными средствами, способными повышать концентрацию розувастатина в плазме крови через взаимодействие с этими транспортными белками (например с циклоспорином и некоторыми ингибиторами протеазы, включая комбинации ритонавира с атазанавиром, лопинавиром и/или типранавиром). Следует рассмотреть альтернативное лечение и, если необходимо, прекратить терапию розувастатином. В ситуациях, когда одновременного применения этих лекарственных средств с розувастатином избежать невозможно, следует взвесить пользу и риски от сопутствующего применения и тщательно подбирать дозу розувастатина.
Побочные действия
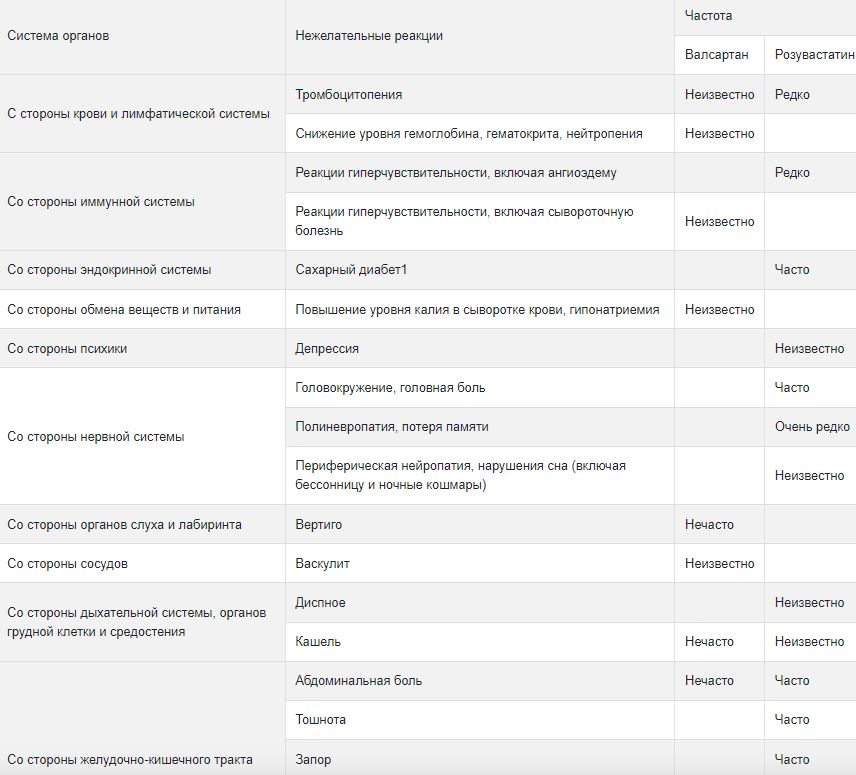
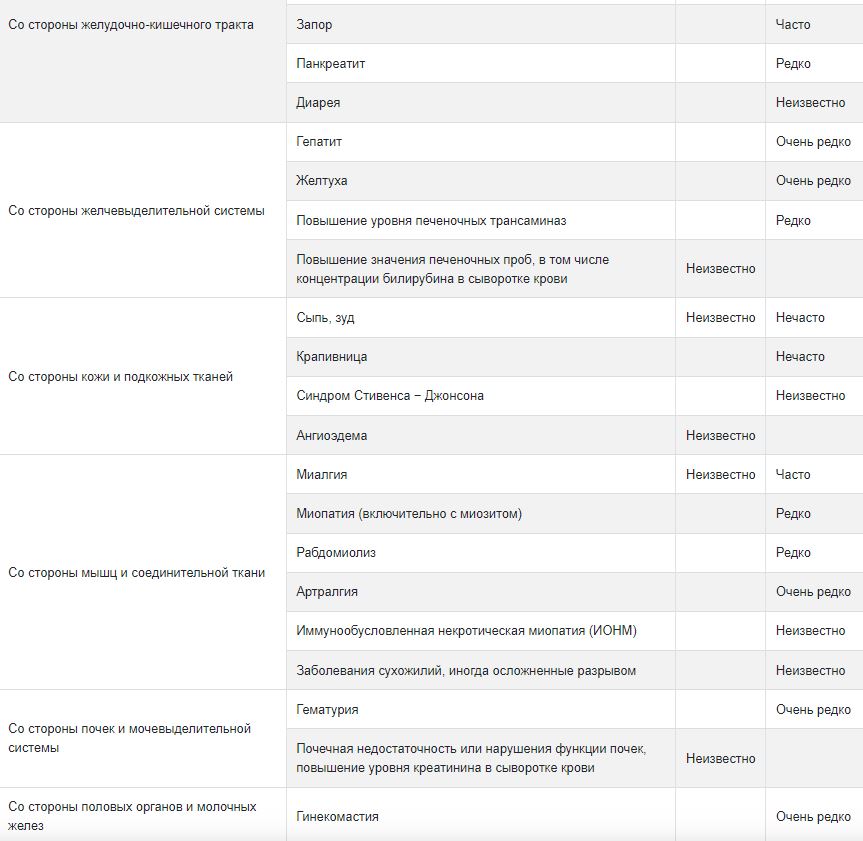
Неблагоприятные реакции, которые наблюдаются при применении розувастатина, обычно легкие и кратковременные. Менее 4% пациентов прекратили прием розувастатина из-за побочных реакций. При применении валсартана взрослым пациентам с артериальной гипертензией частота побочных реакций при применении плацебо соответствовала таковой при применении валсартана. Частота побочных реакций не связана с дозой или длительностью лечения, а также показано отсутствие связи с полом, возрастом или расой пациента. В таблице ниже представлены побочные эффекты при применении розувастатина и валсартана на основе данных клинических и постмаркетинговых исследований. Нежелательные реакции классифицируются в зависимости от частоты и системы органов: очень часто (≥ 1/10); часто (≥ 1/100 − < 1/10); нечасто (≥ 1/1,000 − < 1/100); редко (≥ 1/10,000 − < 1/1,000); очень редко (< 1/10000); неизвестно (нельзя оценить по имеющимся данным).
1 Частота зависит от наличия или отсутствия факторов риска (уровень глюкозы натощак ≥ 5,6 ммоль/л, ИМТ > 30 кг/м2, повышенный уровень триглицеридов, артериальная гипертензия в анамнезе).
Как и при применении других ингибиторов ГМГ-КоА-редуктазы, частота побочных реакций, как правило, зависит от дозы. Описание отдельных побочных реакций Воздействие на почки У пациентов, применявших розувастатин, наблюдались случаи протеинурии, преимущественно канальцевого происхождения (определенной по «тесту полоски»). Изменения содержания белка в моче от отсутствия или следов до ++ или более зарегистрированы через некоторое время у < 1% пациентов, принимавших препарат в дозе 10 и 20 мг, и примерно у 3% пациентов при применении дозы 40 мг.
Незначительное увеличение частоты случаев повышения белка в моче от отсутствия или следов до + наблюдалось при применении дозы 20 мг. В большинстве случаев выраженность протеинурии уменьшалась или исчезала спонтанно при продолжении применения препарата. Пересмотр данных клинических исследований и постмаркетинговых наблюдений не выявил причинной связи между протеинурией и острым или прогрессирующим заболеванием почек. Гематурия наблюдалась у пациентов, применявших розувастатин, и данные клинических исследований свидетельствуют о ее низкой частоте.
Воздействие на скелетную мускулатуру
Изменения со стороны скелетной мускулатуры, такие как миалгия, миопатия (в том числе миозит) и редко — рабдомиолиз с острой почечной недостаточностью или без нее наблюдались при применении любых доз розувастатина, особенно при применении доз > 20 мг. О редких случаях рабдомиолиза, иногда ассоциированных с почечной недостаточностью, сообщалось при применении розувастатина, а также других статинов. У пациентов, принимавших розувастатин, наблюдалось дозозависимое возрастание креатинфосфокиназы (КФК); в большинстве случаев явление было слабым, бессимптомным и временным. Если уровни КФК повышены (> 5 × ВГН), лечение следует прекратить.
Воздействие на печень
Как и при применении других ингибиторов ГМГ-КоА редуктазы, у небольшого количества пациентов, принимавших розувастатин, наблюдалось дозозависимое увеличение уровня трансаминаз; в большинстве случаев явление было слабым, бессимптомным и временным. Побочные реакции, которые наблюдались при применении некоторых статинов: сексуальная дисфункция; исключительные случаи интерстициального заболевания легких, особенно при длительной терапии (см. раздел «Особенности применения»). Рабдомиолиз, серьезные нарушения функции почек и печени (преимущественно заключаются в повышении печеночных трансаминаз) наблюдались чаще при применении препарата в дозе 40 мг.
Дети
У детей и подростков после упражнений или значительных физических нагрузок чаще отмечали повышение КФК > 10 ВМН и мышечные симптомы. Профиль безопасности розувастатина у детей, подростков и взрослых подобен.
Противопоказания Валарокс
Повышенная чувствительность к активной субстанции или любому из вспомогательных веществ препарата. Заболевания печени в активной фазе, в том числе неизвестной этиологии, устойчивое повышение уровня трансаминаз в сыворотке крови и повышение уровня любой трансаминазы в сыворотке более чем в 3 раза выше верхней границы нормы. Тяжелое нарушение функции почек (клиренс креатинина < 30 мл/мин). Миопатия. Сопутствующий прием циклоспорина. Беременность и период кормления грудью. Также противопоказано женщинам репродуктивного возраста, не применяющим соответствующие средства контрацепции. Тяжелые нарушения функции печени, билиарный цирроз печени или холестаз. Одновременное применение с алискиреном для пациентов с сахарным диабетом или почечной недостаточностью (СКФ < 60 мл/мин/1,73м2). Дети в возрасте младше 18 лет.
Передозировка
Симптомы.
Результатом передозировки валсартаном может быть выраженная артериальная гипотензия, что может привести к угнетению сознания, сосудистой недостаточности и/или шоку.
Лечение.
Терапевтические мероприятия зависят от времени приема избыточной дозы, типа и тяжести симптомов; стабилизация кровообращения состояния имеет первостепенное значение. При возникновении артериальной гипотензии пациент должен находиться в положении лежа, также следует провести коррекцию объема крови. Маловероятно, что валсартан можно вывести из организма путём гемодиализа. Польза от проведения гемодиализа маловероятна. Специфического лечения в случае передозировки нет. Лечение симптоматическое. В случае необходимости принимать поддерживающие меры. Следует проверить уровни КФК и провести тесты по оценке функционального состояния печени.
Меры предосторожности
Воздействие на почки У пациентов, применявших розувастатин в высоких дозах, особенно 40 мг, отмечались случаи протеинурии (определенной по «тесту полоски»), преимущественно канальцевой по происхождению и в большинстве случаев временной или непродолжительной. Протеинурия не свидетельствовала об остром или прогрессирующем заболевании почек (см. раздел «Побочные реакции»).
Нежелательные явления со стороны почек в постмаркетинговый период отмечали чаще при дозе 40 мг. У пациентов, принимающих препарат в дозе 30 или 40 мг, функцию почек следует регулярно проверять. Отсутствует опыт безопасности применения пациентам с клиренсом креатинина < 10 мл/мин и находящимся на диализе пациентам, поэтому валсартан следует применять с осторожностью. Для взрослых пациентов с клиренсом креатинина >10 мл/мин нет необходимости в коррекции дозы (см. разделы «Противопоказания» и «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»). Одновременное применение антагонистов рецепторов ангиотензина, в том числе валсартана или ингибиторов ангиотензинпревращающего фермента (ИАПФ), с алискиреном пациентам с сахарным диабетом или почечной недостаточностью (СКФ < 60 мл/мин/1,73м2) противопоказано (см. с другими лекарственными средствами и другими видами взаимодействий»).
Двойная блокада ренин-ангиотензин-альдостероновой системы (РААС) Известно, что сопутствующее применение ингибиторов АПФ и антагонистов рецепторов II ангиотензина или алискирена увеличивает риск артериальной гипотензии, гиперкалиемии и изменения функции почек, включая ОПН. В связи с двойной блокадой РААС сопутствующее применение ингибиторов АПФ и антагонистов рецепторов II ангиотензина или алискирена не рекомендуется (см. разделы «Побочные эффекты» и «Фармакокинетика»). При крайней необходимости двойной блокады следует под наблюдением врача контролировать функцию почек, уровень электролитов и артериальное давление. Не следует одновременно применять ингибиторы АПФ и антагонисты рецепторов II ангиотензина пациентам с диабетической нефропатией. Стеноз почечной артерии Безопасность применения валсартана пациентам с двусторонним стенозом почечных артерий или стенозом артерии единственной почки не установлена. Краткосрочное применение валсартана 12 пациентам со вторичной вазоренальной артериальной гипертензией и односторонним стенозом почки не повлекло за собой значительных изменений почечной гемодинамики, уровня креатинина в сыворотке крови или уровня мочевины в крови.
Однако другие вещества, влияющие на ренин-ангиотензиновую систему, могут увеличивать уровень мочевины и креатинина в сыворотке крови у пациентов с односторонним стенозом почки, поэтому следует контролировать функцию почек у пациентов, принимающих валсартан. Трансплантация почки Нет опыта безопасного применения валсартана пациентам с недавно проведенной трансплантацией почки. Гиперкалиемия Сопутствующий прием добавок калия, калийсберегающих диуретиков, содержащих калий заменителей соли или других препаратов, которые могут увеличить уровень калия (гепарин и т.п.) не рекомендуется. В случае необходимости приема лекарственного препарата, влияющего на уровне калия, в комбинации с валсартаном, рекомендуется проводить мониторинг уровней калия в плазме.
Пациенты с дефицитом объема циркулирующей жидкости и/или натрия в организме У пациентов с дефицитом объема циркулирующей жидкости и/или натрия в организме вследствие применения высоких доз диуретиков редко может возникать симптоматическая гипотензия, особенно после приема первой дозы валсартана. Такие состояния требуют проведения их коррекции к применению валсартана, например, уменьшение дозы диуретика. Воздействие на скелетную мускулатуру Поражение скелетной мускулатуры, например миалгия, миопатия и редко — рабдомиолиз наблюдались у пациентов при применении всех доз розувастатина, особенно доз > 20 мг.
При применении эзетимиба в комбинации с ингибиторами ГМГ-КоА-редуктазы очень редко сообщалось о случаях развития рабдомиолиза. Нельзя исключать возможности фармакодинамического взаимодействия, поэтому такую комбинацию следует применять с осторожностью (см. раздел «Побочные эффекты»). Как и при применении других ингибиторов ГМГ-КоА редуктазы, случаи рабдомиолиза, связанные с применением розувастатина, в постмаркетинговый период встречались чаще при применении дозы 40 мг. Определение уровня креатинфосфокиназы (КФК) Уровни креатинфосфокиназы не следует измерять после значительных физических нагрузок или при наличии возможных альтернативных причин повышения креатинфосфокиназы, которые могут мешать интерпретации результатов.
Если начальные уровни креатинфосфокиназы значительно повышены [> 5×ВГН (верхняя граница нормы)], в течение 5—7 дней необходимо сделать дополнительный подтвердительный анализ. Если результат повторного анализа подтверждает начальный уровень > 5 ВГН, начинать лечение не следует. Перед лечением Валарокс, как и другие ингибиторы ГМГ-КоА редуктазы, следует с осторожностью назначать пациентам с факторами, способствующими развитию миопатии/рабдомиолиза. К таким факторам относятся: нарушение функции почек; гипотиреоз; наличие в индивидуальном или семейном анамнезе наследственных мышечных заболеваний; наличие в анамнезе поражения мышц, вызванного другими ингибиторами ГМГ-КоА-редуктазы или фибратами; злоупотребление алкоголем; возраст > 70 лет; ситуации, которые могут привести к повышению уровней препарата в плазме крови (см. раздел «Способ применения и дозы», «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий» и «Фармакокинетика»); одновременное применение фибратов.
У таких пациентов следует сравнить риск и возможную пользу при применении препарата; также рекомендован клинический мониторинг. Не следует начинать лечение в случае значительно повышенных начальных уровней КФК (> 5 × ВГН). В период лечения Пациентам следует предупредить о необходимости немедленно сообщать о мышечной боли невыясненного происхождения, мышечной слабости или судорогах, особенно если они сопровождаются недомоганием или повышением температуры. У таких пациентов следует определить уровни КФК. Следует прекратить лечение, если уровни КФК значительно повышены (> 5 × ВГН) или если мышечные симптомы тяжелые и вызывают дискомфорт в повседневной жизни (даже если уровни КФК ≤ 5 × ВГН). Если симптомы проходят, а уровень КФК возвращается в норму, Валарокс или альтернативный ингибитор ГМГ-КоА можно попробовать применить снова, но в минимальных дозах и под тщательным наблюдением.
Регулярный контроль уровня КФК у пациентов без вышеуказанных симптомов не требуется. Очень редко сообщалось об иммунообусловленной некротической миопатии (ИОНМ) во время или после лечения статинами, в том числе розувастатином. ИОНМ клинически характеризуется слабостью проксимальных мышц и повышенным уровнем КФК, которые сохраняются, несмотря на прекращение лечения статинами. В клинических исследованиях у небольшого количества пациентов, применявших розувастатин и сопутствующие препараты, усиленного влияния на скелетную мускулатуру не отмечалось. Однако повышенная частота случаев миозита и миопатии наблюдалась у пациентов, применяющих другие ингибиторы ГМГ-КоА-редуктазы с производными фиброевой кислоты, в том числе гемфиброзилом, циклоспорином, никотиновой кислотой, азольными противогрибковыми средствами и ингибиторами протеазы.
Гемфиброзил повышает риск развития миопатии при сопутствующем применении с некоторыми ингибиторами ГМГ-КоАредуктазы, поэтому Валарокс не рекомендуется применять в комбинации с гемфиброзилом. Следует учесть благоприятное влияние дальнейших изменений уровня липидов при одновременном применении Валарокса с фибратами или ниацином и потенциальные риски при применении такой комбинации. Одновременное применение розувастатина в дозе 30 мг или 40 мг и фибратов противопоказаны (см. разделы «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий» и «Побочные эффекты»). Валарокс не следует применять одновременно с фузидовой кислотой или в течение 7 дней после прекращения лечения фузидовой кислотой. Пациентам, для которых системное применение фузидовой кислоты считается необходимым, лечение статинами необходимо прекратить в течение всего периода лечения фузидовой кислотой. Были сообщения о случаях рабдомиолиза (включая летальные исходы) у пациентов, получавших фузидовую кислоту и статины в комбинации.
Пациент должен немедленно обратиться к врачу, если он испытывает симптомы, такие как мышечная слабость, боль или дряблость. Терапия статинами может быть повторно проведена через 7 дней после последней дозы фузидовой кислоты. В исключительных случаях, когда необходимо длительное системное применение фузидовой кислоты, например для лечения тяжелых инфекций, одновременное применение Валарокса и фузидовой кислоты возможно только под тщательным контролем. Валарокс не следует применять пациентам с острыми, серьезными состояниями, способствующими развитию миопатии или повышающими риск развития почечной недостаточности на фоне рабдомиолиза (такими как сепсис, гипотензия, большое хирургическое вмешательство, травма, тяжелые метаболические, эндокринные или электролитные нарушения).
Воздействие на печень Как и другие ингибиторы ГМГ-КоА-редуктазы, Валарокс следует с осторожностью применять пациентам, злоупотребляющим алкоголем и/или имеющим заболевания печени в анамнезе. Функцию печени рекомендуется проверить перед применением препарата и через 3 месяца лечения. Если уровень трансаминаз в сыворотке крови более чем в три раза превышает верхнюю границу нормы, применение Валарокса следует прекратить. О серьезных нарушениях функции печени (преимущественно повышения уровня печеночных трансаминаз) в постмаркетинговый период сообщалось чаще при применении дозы 40 мг. У пациентов с вторичной гиперхолестеринемией, вызванной гипотиреозом или нефротическим синдромом, сначала следует провести лечение основного заболевания, а затем начинать применение Валарокса.
Раса В исследованиях фармакокинетики наблюдалось возрастание системной экспозиции препарата у пациентов монголоидной расы по сравнению с европейцами. Ингибиторы протеазы Повышенная системная экспозиция розувастатина наблюдалась у лиц, применявших розувастатин в сочетании с различными ингибиторами протеазы в сочетании с ритонавиром. Следует учитывать, как пользу от снижения уровня липидов с помощью препарата Валарокс у пациентов с ВИЧ, получающих ингибиторы протеазы, так и возможность повышения концентраций розувастатина в плазме крови в начале терапии и при повышении дозы Валарокса для пациентов, получающих ингибиторы протеазы.
Одновременное применение препарата с ингибиторами протеазы не рекомендуется, если доза розувастатина не скорректирована. Интерстициальное заболевание легких Единичные случаи интерстициального заболевания легких были зарегистрированы при применении некоторых статинов, особенно в случае длительной терапии (см. раздел «Побочные эффекты»). К симптомам нарушения относятся диспноэ, непродуктивный кашель и ухудшение общего состояния (усталость, потеря массы тела и лихорадка). Если подозревается, что у пациента развилось интерстициальное заболевание легких, применение статинов следует прекратить.
Сахарный диабет Некоторые факты свидетельствуют, что статины повышают уровень глюкозы в крови и у некоторых пациентов с высоким риском развития диабета могут вызвать гипергликемию такого уровня, которая потребует лечения. Однако снижение риска сосудистых нарушений при применении статинов превышает эту угрозу, и поэтому она не должна являться основанием для прекращения терапии статинами. За пациентами группы риска (уровень глюкозы натощак 5,6—6,9 ммоль/л, индекс массы тела (ИМТ) > 30 кг/м2, повышенный уровень триглицеридов, артериальная гипертензия) следует установить как клинический, так и биохимический контроль в соответствии с действующими наставлениями. В исследованиях зарегистрированная общая частота сахарного диабета составляла 2,8% в группе приема розувастатина и 2,3% в группе плацебо, преимущественно у пациентов с уровнем глюкозы натощак от 5,6 до 6,9 ммоль/л.
Первичный гиперальдостеронизм Пациенты с первичным гиперальдостеронизмом не должны применять Валарокс, поскольку у них не активирована ренин-ангиотензин-альдостероновая система. Стеноз аорты и митрального клапана, обструктивная гипертрофическая кардиомиопатия. Как и при применении других сосудорасширяющих препаратов, следует с особой осторожностью применять Валарокс пациентам, страдающим стенозом аорты или митрального клапана или гипертрофической обструктивной кардиомиопатией. Беременность Прием антагонистов рецепторов ангиотензина II (АРА II) не следует начинать в период беременности. Если продолжение терапии антагонистами рецепторов ангиотензиина II не считается необходимым, пациенток, планирующих беременность, следует перевести на альтернативное антигипертензивное лечение препаратами с подтвержденным профилем безопасности применения во время беременности.
Если выявлена беременность, лечение АРА II следует немедленно прекратить, и, если это возможно, следует начать альтернативную терапию (см. разделы «Противопоказания» и «Применение в период беременности или кормления грудью»). Ангионевротический отек в анамнезе Возникновение отека Квинке (в том числе отека гортани и голосовой щели, что приводит к обструкции дыхательных путей и/или отек лица, губ, глотки и/или языка) наблюдалось у пациентов, получавших валсартан, некоторые из этих пациентов имели в анамнезе отек Квинке при применении других препаратов, в том числе ингибиторов АПФ. При развитии отека Квинке лечение Валароксом следует немедленно прекратить. Повторное применение препарата противопоказано. Валарокс содержит лактозу. Пациентам с редкой наследственной непереносимостью галактозы, дефицитом лактазы Лаппа или нарушением всасывания глюкозы-галактозы не следует применять этот препарат.
Дети
Поскольку при артериальной гипертензии у детей и подростков сопутствующие нарушения функции почек наблюдаются часто, следует с осторожностью одновременно применять валсартан и другие вещества, подавляющие РААС, которые могут увеличить уровень калия в сыворотке крови. Следует контролировать функцию почек и уровень калия в сыворотке крови.
Безопасность и эффективность для детей (до 18 лет) не установлены. Валарокс противопоказан применение пациентам в возрасте до 18 лет.
Применение в период беременности и кормления грудью
Валарокс противопоказан во время беременности и кормления грудью. Беременность Розувастатин Женщинам репродуктивного возраста следует применять соответствующие средства контрацепции. Поскольку холестерин и другие продукты биосинтеза холестерина существенны для развития плода, потенциальный риск ингибирования ГМГ-КоА-редуктазы превышает возможную пользу от применения препарата в период беременности. В некоторых исследованиях на животных выявлена репродуктивная токсичность.
Если пациентка беременна в период применения препарата, лечение следует немедленно прекратить. Валстартон Применение антагонистов рецепторов ангиотензина II (АРА II) противопоказано в течение беременности. Данные эпидемиологических исследований риска тератогенности после применения ингибиторов АПФ в течение первого триместра беременности не были убедительными; однако небольшое возрастание риска исключать нельзя. Хотя данные контролируемых эпидемиологических исследований антагонистов рецепторов ангиотензина II (АРА II) отсутствуют, существует риск тератогенности при применении препаратов этого класса.
Пациенток, планирующих беременность, следует перевести на альтернативные гипотензивные препараты с подтвержденным профилем безопасности в период беременности. Если во время лечения этим лекарственным средством подтверждается беременность, его применение следует прекратить и, если необходимо, заменить другим лекарственным средством, разрешенным к применению беременным. АРА II во втором и третьем триместре, как известно, оказывают токсическое действие на плод человека (снижение почечной функции, олигогидрамнион, задержка осификации костей черепа) и новорожденного (почечная недостаточность, артериальная гипотензия, гиперкалиемия).
При применении АРА II, начиная со второго триместра беременности, рекомендуется ультразвуковое исследование функции почек и костей черепа плода. Младенцы, матери которых принимали АРА II, должны находиться под пристальным наблюдением на случай развития артериальной гипотензии (см. разделы «Противопоказания» и «Особенности применения»). Кормление грудью Розувастатин проникает в грудное молоко крыс. Нет данных о проникновении розувастатина в грудное молоко человека. Поскольку информация о применении препарата в период кормления грудью отсутствует, его не рекомендуется применять в период кормления грудью; желательно применять альтернативные препараты с изученным профилем безопасности, особенно при кормлении грудью новорожденных или недоношенных детей.
Фертильность Валсартан не влияет на репродуктивную функцию самцов и самок крыс при пероральном применении в дозировке до 200 мг/кг/день. Эта доза в 6 раз превышает рекомендованную дозу для человека в мг/м2 (расчеты при пероральном применении 320 мг/сут пациенту весом 60 кг).
Способность влиять на скорость реакции при управлении транспортом
Не проводили исследований по определению влияния Валарокса на способность управлять автомобилем и другими механическими средствами. Однако при управлении автомобилем и другими механическими средствами следует учитывать, что во время лечения может возникнуть головокружение.
Взаимодействие с другими лекарственными средствами
Взаимодействия Валарокса с другими лекарственными средствами не исследовались. Взаимодействия, связанные с валсартаном Двойная блокада ренин-ангиотензин-альдостероновой системы (РААС) препаратами групп АРА, ИАПФ или алискиреном Данные исследований показывают, что двойная блокада ренин-ангиотензин-альдостероновой системы (РААС) ингибиторами АПФ, блокаторами рецепторов ангиотензина II или алискиреном связана с более высокой частотой побочных эффектов, таких как артериальная гипотензия, гиперкалиемия и снижение почечной функции (в том числе почечная недостаточность), по сравнению с применением одного блокатора РААС (см. разделы «Противопоказания», «Особенности применения», «Фармакодинамика»).
Сопутствующее применение не рекомендуется Литий Сообщалось о временном повышении концентраций лития в сыворотке крови и токсичности при одновременном приеме лития и ингибиторов АПФ. Если доказана необходимость применения комбинации, рекомендуется тщательный мониторинг уровня лития в плазме крови. Калийсберегающие диуретики, добавки калия, заменители соли, содержащие калий или другие препараты, которые могут увеличить уровень калия. В случае необходимости приема лекарственного препарата, влияющего на уровне калия, в комбинации с валсартаном, рекомендуется проводить мониторинг уровня калия в плазме крови. Одновременное применение, требующее осторожности Нестероидные противовоспалительные препараты (НПВП), включая селективные ингибиторы ЦОГ-2, ацетилсалициловую кислоту > 3 г/сут и неселективные НПВП При одновременном приеме антагонистов ангиотензина II с НПВП может возникать ослабление антигипертензивного эффекта.
Также одновременное применение антагонистов ангиотензина II и НПВП повышает риск ухудшения функции почек и может привести к повышению уровня калия в сыворотке крови. Поэтому рекомендуется мониторинг функции почек в начале лечения и достаточное обеспечение пациента жидкостью. Транспортеры По результатам исследований in vitro валсартан является субстратом для печеночного транспортера захвата OATP1B1/OATP1B3 и печеночного транспортера выведения MRP2. Клиническое значение этих данных не известно. Одновременное применение ингибиторов захватного транспортера (например рифампицина, циклоспорина) или транспортера выведения (например ритонавира) может увеличить системную экспозицию валсартана. Следует принимать надлежащие меры в начале или конце одновременного применения этих лекарственных средств. Не определялось взаимодействие Исследования не выявили никакого клинически значимого взаимодействия валсартана с каким-либо из таких веществ: циметидин, варфарин, фуросемид, дигоксин, атенолол, индометацин, гидрохлоротиазид, амлодипин, глибенкламид.
Взаимодействия, связанные с розувастатином Влияние сопутствующих лекарственных средств на экспозицию розувастатина Ингибиторы транспортных белков Розувастатин является субстратом для определенных транспортных белков, включая OATP1B1, обеспечивающий печеночный транспорт, и эфлюксный переносчик BCRP. Одновременное применение с лекарственными средствами — ингибиторами этих транспортных белков может привести к повышению концентрации розувастатина в плазме крови и увеличению риска миопатии (см. раздел «Способ применения и дозы», «Особенности применения» и таблицу 2).
Циклоспорин В период сопутствующего применения розувастатина и циклоспорина значения AUC розувастатина были в среднем примерно в 7 раз выше, чем наблюдавшаяся у здоровых добровольцев (см. таблицу 2). Розувастатин противопоказан пациентам, одновременно получающим циклоспорин (см. раздел «Противопоказания»). Сопутствующее применение не влияло на концентрацию циклоспорина в плазме крови. Ингибиторы протеазы Хотя точный механизм взаимодействия неизвестен, одновременное применение ингибиторов протеазы может значительно увеличивать экспозицию розувастатина (см. таблицу 2). Например, в исследовании фармакокинетики одновременное применение 10 мг розувастатина и комбинированного лекарственного средства, содержащего два ингибитора протеазы (300 мг атазанавира/100 мг ритонавира), у здоровых добровольцев сопровождалось повышением AUC и Cmax розувастатина примерно в 3 и 7 раз соответственно.
Одновременное применение препарата и некоторых комбинаций ингибиторов протеазы возможно после тщательного рассмотрения коррекции дозы розувастатина, исходя из ожидаемого возрастания его экспозиции (см. раздел «Способ применения и дозы», «Особенности применения», «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий», таблицу 2). Гемфиброзил и другие гиполипидемические препараты Одновременное применение розувастатина и гемфиброзила приводило к росту AUC и Cmax розувастатина в 2 раза (см. раздел «Особенности применения»). Исходя из данных специальных исследований взаимодействия, значительного фармакокинетического взаимодействия с фенофибратом не ожидается, однако возможно фармакодинамическое взаимодействие.
Гемфиброзил, фенофибрат, другие фибраты и ниацин (никотиновая кислота) в гиполипидемических дозах (≥ 1 г/сут) повышают риск развития миопатии при сопутствующем применении с ингибиторами ГМГ-КоА-редуктазы, возможно потому, что они способны приводить к миопатии и при применении по отдельности. Дозировка 30 и 40 мг противопоказана при сопутствующем применении фибратов. Лечение в таких случаях следует начинать с дозы 5 мг. Эзетимиб Одновременное применение препарата с 10 мг розувастатина и 10 мг эзетимиба пациентам с гиперхолестеринемией приводило к возрастанию AUC розувастатина в 1,2 раза (таблица 2). Нельзя исключать фармакодинамическое взаимодействие между препаратом Валарокс и эзетимибом, которое может привести к нежелательным явлениям (см. раздел «Особенности применения»).
Антациды Одновременное применение розувастатина с суспензиями антацидов, содержащих алюминий и гидроксид магния, привело к снижению концентрации розувастатина в плазме примерно на 50%. Этот эффект был менее выражен, когда антацид вводили через 2 ч после Валарокса. Клиническая значимость этого взаимодействия не установлена. Эритромицин Одновременное применение розувастатина и эритромицина снижало AUC розувастатина на 20%, а Cmax — на 30%. Такое взаимодействие может быть вызвано повышением перистальтики кишечника в результате действия эритромицина. Ферменты цитохрома Р450 Результаты исследований in vitro и in vivo свидетельствуют о том, что розувастатин не ингибирует и не стимулирует изоферменты цитохрома Р450. Кроме того, розувастатин является слабым субстратом этих изоферментов. Таким образом, взаимодействия с лекарственными средствами в результате метаболизма, опосредованного Р450, не ожидается.
Не наблюдалось клинически значимых взаимодействий между розувастатином и флуконазолом (ингибитором CYP2C9 и CYP3A4) или кетоконазолом (ингибитором CYP2A6 и CYP3A4). Взаимодействия, требующие коррекции дозы розувастатина (см. также таблицу 2): При необходимости сопутствующего применения розувастатина с другими лекарственными средствами, увеличивающими экспозицию розувастатина, дозы последнего должны быть скорректированы. Если ожидается увеличение экспозиции (AUC) примерно в 2 раза или выше, лечение следует начинать с 5 мг розувастатина 1 раз в сутки. Максимальная суточная доза розувастатина должна быть отрегулирована таким образом, чтобы ожидаемая экспозиция розувастатина не превышала экспозицию, отмечаемую при приеме 40 мг розувастатина в сутки без применения лекарственных средств, взаимодействующих с препаратом. Например, при применении с гемфиброзилом максимальная доза розувастатина составит 20 мг (1,9-кратное увеличение) и при применении с комбинацией атазанавир/ритонавир — 10 мг розувастатина (3,1-кратное увеличение).
Данные, представленные в виде% изменения, представляют собой процентную разницу в отношении показателей при применении розувастатина в отдельности. Увеличение отмечено значком — ↑, отсутствие изменений — ↔, уменьшение — ↓. ** Было проведено несколько исследований взаимодействия при разных дозах розувастатина, в таблице представлено наиболее значимое соотношение. Воздействие розувастатина на лекарственные средства при одновременном применении Антагонисты витамина К Как и при применении других ингибиторов ГМГ-КоА-редуктазы, в начале лечения или при подборе дозы Валарокса одновременное применение антагонистов витамина К (например, варфарина или другого кумаринового антикоагулянта) может привести к увеличению международного нормализованного соотношения (МНО).
Прекращение применения или уменьшение дозы Валарокса может привести к уменьшению МНО. В таких ситуациях желателен соответствующий контроль МНО. Пероральные контрацептивы/гормонозаместительная терапия (ГЗТ) Одновременное применение розувастатина и пероральных контрацептивов приводило к повышению AUC этинилэстрадиола и норгестрела на 26% и 34% соответственно. Повышение плазменных уровней следует учитывать при подборе пероральных доз контрацептивов. Нет данных о фармакокинетике препаратов у пациентов, одновременно принимающих розувастатин и ГЗТ, поэтому возможность взаимодействия исключать нельзя. Однако такая комбинация широко применялась женщинам в клинических исследованиях, и она переносилась хорошо.
Другие лекарственные средства
Дигоксин
Исходя из данных специальных исследований, клинически существенного взаимодействия с дигоксином не ожидается. Фузидовая кислота Риск миопатии, включая рабдомиолиз, может повышаться за счет сопутствующего системного применения фузидовой кислоты со статинами. Механизм этого взаимодействия (фармакодинамический или фармакокинетический) пока неизвестен. Были сообщения о рабдомиолизе (включая летальные исходы) у пациентов, получавших эту комбинацию. Если системное лечение фузидовой кислотой необходимо, то применение розувастатина должно быть прекращено в течение всего периода лечения фузидовой кислотой (см. раздел «Особенности применения»). Дети Исследования взаимодействия проводились только у взрослых. Степень взаимодействия у детей неизвестна.
Условия и срок хранения Валарокс
3 года. Условия хранения Для лекарственного средства не требуются специальные температурные условия хранения. Хранить в оригинальной упаковке для защиты от влаги. Хранить в недоступном для детей месте.
Упаковка
По 10 таблеток в блистере; по 3 блистера в картонной коробке.
Правила отпуска
По рецепту.
Информация о производителе
Шамрьешка цеста 6, 8501 Новое место, Словения/Smarjeska cesta 6, 8501 Novo mesto, Словения.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Валарокс только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание! Эта инструкция по применению лекарственного средства является официальной инструкцией производителя KRKA, d.d..
Авторское право:
- https://www.krka.biz/by/ - KRKA, d.d.
- https://www.rceth.by - Государственный реестр ЛС Республики Беларусь
| Тип данных | Сведения из реестра |
| Торговое наименование: | Валарокс |
| Форма выпуска: | таблетки, покрытые пленочной оболочкой, 10мг/80мг, 10мг/160мг, 20мг/80мг, 20мг/160мг в блистерах в упаковке №10х3 |
| Международное наименование: | Rosuvastatin and valsartan |
| Производитель: | KRKA, d.d., Словения |
| Заявитель: | KRKA, d.d., Словения |
| Номер регистрации: | 10818/20 |
| Дата регистрации: | 05.12.2020 |
| Срок действия: | 05.12.2025 |
| Дата переоформления: | 01.01.2100 |
| Тип: | Лекарственное средство |
| Оригинальное: | генерик |
| Состав лекарственного средства: | Rosuvastatin and valsartan |
| Код АТХ: | C10BX10 |
| Производитель готовой лекарственной формы: | KRKA, d.d., Словения |
| Производитель, осуществляющий фасовку/упаковку: | KRKA, d.d., Словения |
| Контроль качества: | |
| Выдача разрешения на выпуск лекарственного средства: | KRKA, d.d., Словения |
| Другие участники производства: | Выпуск серии: KRKA, d.d., Словения |
| Заявленная цена: | 11,5USD |
| Порядок отпуска: | по рецепту |
| Список хранения: | |
| Срок годности лекарства: | 2 года |
| Нормативная документация: | НД РБ 9413-2020 |
| Дата утверждения нормативной документации: | 12 мая 2020 г. 0:00 |
| Срок действия нормативной документации: | 12 мая 2025 г. 0:00 |
| Изменение в нормативной документации: | |
| Номер разрешения НД: | 11733 |
| Код АТХ | Название группы |
| C | Сердечно-сосудистая система |
| C10 | Гиполипидемические препараты |
| C10B | Гиполипидемические препараты, комбинации |
| C10BX | Ингибиторы ГМГ-КоА-редуктазы, другие комбинации |
| C10BX10 | Розувастатин и валсартан |