- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Ксалтофай инструкция по применению
Официальная инструкция лекарственного препарата Ксалтофай раствор 100 ОД/мл, 3,6 мг/мл. Описание и применение Ksaltofaj, аналоги и отзывы. Инструкция Ксалтофай раствор утвержденная компанией производителем.
Состав
действующие вещества: инсулин деглюдек, лираглутид;
1 мл содержит 100 ЕД инсулина деглюдек * и 3,6 мг лираглутид *.
1 предварительно заполненая шприц-ручка содержит 3 мл, что эквивалентно 300 ЕД инсулина деглюдек и 10,8 мг лираглутид;
вспомогательные вещества: глицерин, фенол, цинка ацетат, кислота соляная (для коррекции pH), натрия гидроксид (для коррекции pH), вода для инъекций.
* Выработанные по технологии рекомбинантной ДНК в Saccharomyces cerevisiae.
Лекарственная форма
Раствор для инъекций.
Основные физико-химические свойства: прозрачный, бесцветный, изотонический раствор.
Фармакологическая группа
Лекарственные средства, применяемые при сахарном диабете. Инсулины и аналоги длительного действия для инъекций.
Код АТХ A10A E56.
Фармакологические свойства
Фармакологические.
Механизм действия.
Ксалтофай является комбинированным лекарственным средством , состоящий из инсулина деглюдек и лираглутид, механизмы действия которых дополняют друг друга, улучшая гликемический контроль.
Инсулин деглюдек - это базальный инсулин, который после введения препарата образует растворимый мультигексамер. В результате формируется депо, из которого инсулин деглюдек непрерывно и медленно всасывается в кровоток, что приводит к равной и устойчивый эффект снижения уровня глюкозы в крови с низкой ежедневной вариабельностью действия инсулина.
Инсулин деглюдек специфически связывается с рецептором инсулина человека, обеспечивая такой же фармакологический эффект, что и инсулин человека.
Сахароснижающий эффект инсулина деглюдек заключается в содействии поглощения глюкозы после связывания инсулина с рецепторами мышечных и жировых клеток, а также в одновременном угнетении выделения глюкозы из печени.
Лираглутид является аналогом глюкагоноподобного пептида-1 (ГПП-1) с последовательностью аминокислот, на 97% гомологична ГПП-1 человека, он связывается с рецептором ГПП-1 (ГПП-1Р) и активирует его. Пролонгированное действие введенного подкожно лираглутид обусловлена тремя механизмами самоассоциации, что замедляет всасывание, связыванием с альбумином крови и повышенной устойчивостью к действию ферментов дипептидилпептидазы 4 (ДПП-4) и нейтральной эндопептидазы (НЭП), что обеспечивает длительный период полувыведения лекарственного средства из плазмы .
Действие лираглутид происходит за счет его специфического взаимодействия с рецепторами ГПП-1 и способствует улучшению гликемического контроля путем снижения уровня глюкозы в крови натощак и после еды. Лираглутид стимулирует секрецию инсулина и уменьшает чрезмерно высокую секрецию глюкагона глюкозозависимый путем. Таким образом, когда уровень глюкозы в крови высок, происходит стимулирование секреции инсулина и подавление секреции глюкагона. И наоборот, при гипогликемии лираглутид ослабляет секрецию инсулина и не препятствует секреции глюкагона. Кроме того, механизм снижения уровня глюкозы в крови также обусловлен незначительной задержкой опорожнения желудка. Лираглутид снижает массу тела и уменьшает массу жировой ткани благодаря механизмам, включающих уменьшения чувства голода и снижение потребления энергии.
ГПП-1 является физиологическим регулятором аппетита и потребления пищи, однако точный механизм его действия пока не выяснено полностью. В ходе исследований на животных периферийное введение лираглутид приводило к поглощению препарата специфическими участками головного мозга, задействованных в процессах регуляции аппетита, в которых лираглутид через специфическую активацию ГПП-1Р усиливал сигналы насыщения и ослаблял сигналы голода, тем самым вызывая уменьшение массы тела.
Рецепторы ГПП-1 представлены также и в специфических участках сердца, сосудов, иммунной системы и почек. В экспериментальных моделях атеросклероза на мышах лираглутид предотвращал дальнейшему развитию аортальной бляшки и снижал степень воспаления в бляшке. Кроме того, лираглутид благоприятным образом влиял на липиды плазмы крови. Лираглутид не уменьшало размер уже имеющихся бляшек.
Фармакодинамические эффекты.
Ксалтофай имеет стабильный фармакодинамический профиль с продолжительностью действия, являющиеся результатом комбинированного действия инсулина деглюдек и лираглутид, что позволяет применять Ксалтофай один раз в сутки в любое время независимо от приема пищи. Ксалтофай улучшает гликемический контроль путем устойчивого снижения уровня глюкозы в крови натощак и после всех приемов пищи.
Снижение уровня глюкозы после приема пищи было подтверждено в ходе вспомогательного исследования продолжительностью 4:00 после стандартизированного приема пищи у пациентов с неудовлетворительным контролем при применении монотерапии метформином или его комбинации с пиоглитазоном. Ксалтофай вызывал более значительное снижение уровня глюкозы в плазме крови после приема пищи (средний уровень за 4:00), чем инсулин деглюдек. Результаты применения лекарственного средства Ксалтофай и лираглутид были одинаковыми.
Клиническая эффективность и безопасность.
Безопасность и эффективность лекарственного средства Ксалтофай оценивались в ходе 6 рандомизированных контролируемых исследований фазы 3 в параллельных группах с участием различных популяций пациентов с диабетом 2-го типа в зависимости от предварительной противодиабетической терапии. Терапия препаратами сравнения включала применение базального инсулина, агонистов рецепторов ГПП-1, плацебо и базально-болюсного режима. Испытания продолжались 26 недель с рандомизации от 199 до 833 пациентов для приема лекарственного средства Ксалтофай. Одно исследование было дальше продлено до 52 недель. Во всех исследованиях начальная доза лекарственного средства определялась согласно инструкции для медицинского применения; и два раза в неделю осуществлялось титрования дозы лекарственного средства Ксалтофай (см. таблицу 1). Такой же алгоритм титрования дозы использовался и при применении препаратов сравнения- базальных инсулинов. В ходе 5 исследований Ксалтофай продемонстрировал клинически и статистически значимое улучшение гликемического контроля против препаратов сравнения по уровню гликозилированного гемоглобина A1c (HbA1c), тогда как в одном исследовании было продемонстрировано одинаковое снижение HbA1c в обеих группах лечения.
Таблица 1. Титрование дозы лекарственного средства Ксалтофай.
Уровень глюкозы в плазме крови натощак * | Коррекция дозы (дважды в неделю) | |
ммоль/л | мг/дл | Ксалтофай (шаги дозы) |
<4,0 | <72 | ˗2 |
4,0˗5,0 | 72˗90 | 0 |
> 5,0 | > 90 | +2 |
* Уровни глюкозы, измеренные пациентом самостоятельно. В ходе исследования применения лекарственного средства Ксалтофай, который прилагался к препаратам сульфонилмочевины, целевой уровень составлял 4,0-6,0 ммоль / л.
Гликемический контроль.
Добавление пероральных сахароснижающих лекарственных средств.
Добавление лекарственного средства Ксалтофай к метформина или к комбинации метформина и пиоглитазона в ходе рандомизированного контролируемого исследования открытого типа продолжительностью 26 недель позволило 60,4% пациентов, получавших Ксалтофай, достичь целевого уровня HbA1c <7% без подтвержденных эпизодов гипогликемии через 26 недель лечения. Эта доля пациентов была существенно больше, чем при применении инсулина деглюдек (40,9%; отношение шансов (ОШ): 2,28; p <0,0001) и схожей с долей пациентов при применении лираглутид (57,7%; ВШ 1,13; p = 0,3184).
Ключевые результаты исследования приведены на рисунке 1 и в таблице 2.
Частота случаев подтвержденной гипогликемии была ниже при применении лекарственного средства Ксалтофай, чем при применении инсулина деглюдек, независимо от степени гликемического контроля (см. Рисунок 1).
Частота случаев тяжелой гипогликемии (которая определялась как эпизод, при котором существует потребность в помощи со стороны другого человека) на один пациенто-год экспозиции (доля пациентов в процентах) составила 0,01 (2 из 825 пациентов) при применении лекарственного средства Ксалтофай 0 , 01 (2 из 412 пациентов) при применении инсулина деглюдек и 0,00 (ни один из 412 пациентов) при применении лираглутид. Частота случаев ночной гипогликемии была похожей при применении лекарственного средства Ксалтофай и инсулина деглюдек.
Вообще, пациенты, которые принимали Ксалтофай, имели меньше побочных эффектов со стороны желудочно-кишечного тракта, чем те, кто получали лираглутид. Это может быть следствием более медленного (по сравнению с монотерапией лираглутид) увеличение дозы лираглутид как компонента лекарственного средства Ксалтофай течение периода начала лечения.
Уровень эффективности и безопасности лекарственного средства Ксалтофай оставался стабильным в течение периода до 52 недель лечения. Снижение показателя HbA1c от исходного уровня до 52-й недели лечения составило 1,84% при применении лекарственного средства Ксалтофай при рассчитанной разницы между группами лечения - 0,65% по сравнению с результатами применения лираглутид (p <0,0001) и - 0, 46% по сравнению с результатами применения инсулина деглюдек (p <0,0001). Масса тела уменьшилась на 0,4 кг с рассчитанной разницей между результатами лечения лекарственным средством Ксалтофай и инсулином деглюдек - 2,80 кг (p <0,0001), а частота подтвержденных случаев гипогликемии оставалась на уровне 1,8 явления на один пациенто-год экспозиции,
Рис. 1. Средние уровни HbA1c (%) по неделям лечения (слева) и частота подтвержденных случаев гипогликемии на один пациенто-год экспозиции в зависимости от средних уровней HbA1c (%) (справа) у пациентов с сахарным диабетом 2-го типа с неудовлетворительным контролем при применении монотерапии метформином или его комбинации с пиоглитазоном.
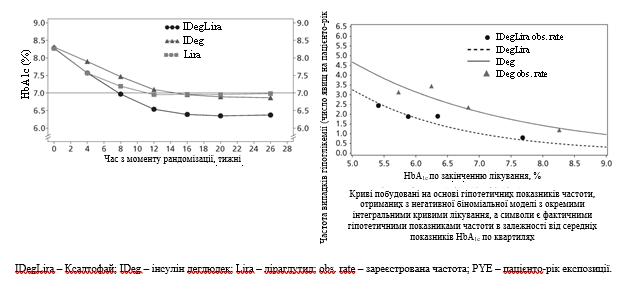
Применение лекарственного средства Ксалтофай совместно с сульфонилмочевины или с комбинацией сульфонилмочевины с метформином изучалось в ходе рандомизированного плацебо контролируемого двойного слепого исследования продолжительностью 26 недель.
Ключевые результаты исследования приведены на рисунке 2 и в таблице 2.
Рис. 2. Средние уровни HbA1c (в%) по неделям лечения у пациентов с сахарным диабетом 2-го типа с неудовлетворительным контролем при применении монотерапии сульфонилмочевины или его комбинации с метформином.
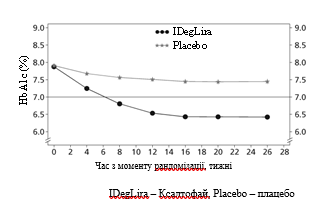
Частота случаев тяжелой гипогликемии на один пациенто-год экспозиции (доля пациентов в процентах) составила 0,02 (2 из 288 пациентов) при применении лекарственного средства Ксалтофай и 0,00 (ни один из 146 пациентов) при применении плацебо.
Таблица 2. Результаты через 26 недель. Добавление пероральных сахароснижающих лекарственных средств.
Добавление метформина ± пиоглитазон | Добавление сульфонилмочевины ± метформин | ||||
Халтофай | инсулин деглюдек | лираглутид | Халтофай | Плацебо | |
N | 833 | 413 | 414 | 289 | 146 |
HbA1c,% Начало → конец исследования | 8,3→6,4 | 8,3→6,9 | 8,3→7,0 | 7,9→6,4 | 7,9→7,4 |
среднее изменение | ˗ 1,91 | ˗ 1,44 | ˗ 1,28 | ˗ 1,45 | ˗ 0,46 |
рассчитана разница | ˗ 0,47AB [˗ 0,58; ˗ 0,36] | ˗ 0,64AB [˗ 0,75; ˗ 0,53] | ˗ 1,02AB [˗ 1,18; ˗ 0,87] | ||
Пациенты (%), которые достигли HbA1c <7% | |||||
все пациенты | 80,6 | 65,1 | 60,4 | 79,2 | 28,8 |
Рассчитан показатель отношения шансов | 2,38B [1,78; 3,18] | 3,26B [2,45; 4,33] | 11,95B [7,22; 19,77] | ||
Пациенты (%), которые достигли HbA1c £ 6,5% | |||||
все пациенты | 69,7 | 47,5 | 41,1 | 64,0 | 12,3 |
Рассчитан показатель отношения шансов | 2,82B [2,17; 3,67] | 3,98B [3,05; 5,18] | 16,36B [9,05; 29,56] | ||
Частота случаев подтвержденной гипогликемии * на один пациенто-год экспозиции (доля пациентов в%) | 1,80 (31,9 %) | 2,57 (38,6 %) | 0,22 (6,8 %) | 3,52 (41,7 %) | 1,35 (17,1 %) |
рассчитано соотношение | 0,68AC [0,53; 0,87] | 7,61B [5,17; 11,21] | 3,74B [2,28; 6,13] | ||
Масса тела, кг Начало → конец исследования | 87,2→86,7 | 87,4→89,0 | 87,4→84,4 | 87,2→87,7 | 89,3→88,3 |
среднее изменение | ˗ 0,5 | 1,6 | ˗ 3,0 | 0,5 | ˗ 1,0 |
рассчитана разница | ˗ 2,22AB [˗ 2,64; ˗ 1,80] | 2,44B [2,02; 2,86] | 1,48B [0,90; 2,06] | ||
ГПН, ммоль/л Начало → конец исследования | 9,2→5,6 | 9,4→5,8 | 9,0→7,3 | 9,1→6,5 | 9,1→8,8 |
среднее изменение | ˗ 3,62 | ˗ 3,61 | ˗ 1,75 | ˗ 2,60 | ˗ 0,31 |
рассчитана разница | ˗ 0,17 [˗ 0,41; 0,07] | ˗ 1,76 млрд [˗ 2,0; ˗ 1,53] | ˗2,30 млрд [˗ 2,72; ˗ 1,89] | ||
Доза в конце исследования Инсулин деглюдек, единиц | 38 | 53 | - | 28 | - |
Лираглутид, мг | 1,4 | - | 1,8 | 1,0 | - |
Рассчитана разница, доза инсулина деглюдек | 14,90 AB [˗ 17,14; | - | |||
Зарегистрированные показатели перед началом, в конце лечения и их изменение . Последние зарегистрированные показатели перенесены вперед. 95% доверительный интервал указан в квадратных скобках ([]).
* Подтверждена гипогликемия определяется как тяжелая форма гипогликемии (эпизод, при котором требуется помощь со стороны другого человека) и / или легкая гипогликемия (уровень глюкозы в плазме крови <3,1 ммоль / л, независимо от симптомов).
A Конечные точки с подтвержденной преимуществом лекарственного средства Ксалтофай по сравнению с препаратом сравнения;
B p <0,0001;
C p <0,05.
ОПН - уровень глюкозы в плазме крови натощак.
Переход от терапии агонистами рецепторов ГПП-1.
В ходе рандомизированного исследования открытого типа продолжительностью 26 недель изучался переход по терапии агонистами рецепторов ГПП-1 на лечение лекарственным средством Ксалтофай по сравнению с применением неизменной терапии агонистами рецепторов ГПП-1 (дозировка по инструкции для медицинского применения) с участием пациентов с сахарным диабетом 2 го типа с неудовлетворительным контролем при применении агониста рецепторов ГПП-1 и метформина (74,2%) или его комбинации с пиоглитазоном (2,5%), с сульфонилмочевины (21,2%) или с обоими препаратами (2,1%) .
Ключевые результаты исследования приведены на рисунке 3 и в таблице 3.
Рис. 3. Средний уровень HbA1c (в%) по неделям лечения у пациентов с сахарным диабетом 2-го типа с неудовлетворительным контролем при применении агонистов рецепторов ГПП-1.
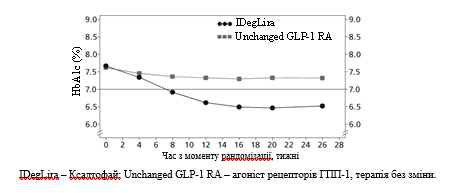
Частота случаев тяжелой формы гипогликемии на один пациенто-год экспозиции (доля пациентов в процентах) составила 0,01 (1 из 291 пациента) при применении лекарственного средства Ксалтофай и 0,00 (ни один из 199 пациентов) при применении агонистов рецепторов ГПП-1.
Таблица 3. Результаты через 26 недель. Переход с терапии агонистами рецепторов ГПП-1.
Переход с терапии агонистом рецепторов ГПП-1 | ||
Халтофай | Агонист рецепторов ГПП-1 | |
N | 292 | 146 |
HbA1c,% | ||
Начало → конец исследования | 7,8→6,4 | 7,7→7,4 |
среднее изменение | ˗1,3 | ˗0,3 |
рассчитана разница | ˗0.94AB [˗1,11; 0,78 фунта стерлингов] | |
Пациенты (%), которые достигли HbA1c <7% | ||
все пациенты | 75,3 | 35,6 |
Рассчитан показатель отношения шансов | 6,84B [4,28; 10,94] | |
Пациенты (%), которые достигли HbA1c £ 6,5% | ||
все пациенты | 63,0 | 22,6 |
Рассчитан показатель отношения шансов | 7,53B [4,58; 12,38] | |
Частота случаев подтвержденной гипогликемии * на один пациенто-год экспозиции (доля пациентов в%) | 2,82 (32,0 %) | 0,12 (2,8 %) |
рассчитано соотношение | 25,36B [10,63; 60,51] | |
Масса тела, кг | ||
Начало → конец исследования | 95,6→97,5 | 95,5→94,7 |
среднее изменение | 2,0 | ˗0,8 |
рассчитана разница | 2,89B [2,17; 3,62] | |
ГПН, ммоль/л | ||
Начало → конец исследования | 9,0→6,0 | 9,4→8,8 |
среднее изменение | ˗2,98 | ˗0,60 |
рассчитана разница | 2,64B [˗3,03; ˗2,25] | |
Доза в конце исследования | Доза агониста рецепторов ГПП-1 должна была оставаться неизменной с начала исследования | |
Инсулин деглюдек, единиц | 43 | |
Лираглутид, мг | 1,6 | |
Рассчитана разница, доза инсулина деглюдек | ||
Зарегистрированные показатели перед началом, в конце лечения и их изменение. Последние зарегистрированные показатели перенесены вперед. 95% доверительный интервал указан в квадратных скобках ([]).
* Подтверждена гипогликемия определяется как тяжелая форма гипогликемии (эпизод, при котором требуется помощь со стороны другого человека) и / или легкая гипогликемия (уровень глюкозы в плазме крови <3,1 ммоль / л, независимо от симптомов).
A Конечные точки с подтвержденной преимуществом лекарственного средства Ксалтофай по сравнению с препаратом сравнения; B p <0,001.
Переход по терапии базальным инсулином.
В ходе исследования продолжительностью 26 недель изучался переход по терапии инсулином гларгин (100 ЕД / мл) на лечение лекарственным средством Ксалтофай по сравнению с интенсификацией применения инсулина гларгин пациентам с неудовлетворительным контролем при применении инсулина гларгин (20-50 единиц) и метформина. Применяемая в ходе этого исследования максимально допустимая доза лекарственного средства Ксалтофай составляла 50 шагов дозы, максимальная доза инсулина гларгин НЕ устанавливалась. В 54,3% пациентов, принимавших Ксалтофай, было достигнуто целевой уровень HbA1c <7% без подтвержденных эпизодов гипогликемии, по сравнению с 29,4% пациентов, принимавших инсулин гларгин (отношение шансов: 3,24; p <0,001).
Ключевые результаты исследования приведены на рисунке 4 и в таблице 4.
Рис. 4. Средние уровни HbA1c (в%) по неделям лечения у пациентов с сахарным диабетом 2-го типа с неудовлетворительным контролем при применении инсулина гларгин.
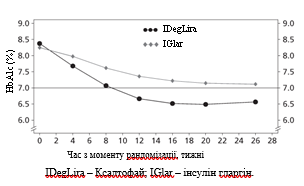
Частота случаев тяжелой гипогликемии на один пациенто-год экспозиции (доля пациентов в процентах) составила 0,00 (ни один из 278 пациентов) при применении лекарственного средства Ксалтофай и 0,01 (1 из 279 пациентов) при применении инсулина гларгин. Частота случаев ночной гипогликемии была значительно ниже при применении лекарственного средства Ксалтофай по сравнению с применением инсулина гларгин (рассчитано отношение в зависимости от лечения: 0,17; p <0,001).
В ходе второго исследования, было рандомизированное двойное слепое исследование продолжительностью 26 недель с участием пациентов с неудовлетворительным контролем при применении базального инсулина (20-40 единиц) и монотерапии метформином или его комбинации с сульфонилмочевины / глиниды, изучался переход из базального инсулина на лекарственное средство Ксалтофай или инсулин деглюдек. Применение базального инсулина и сульфонилмочевины / глиниды было приостановлено во время рандомизации. Максимально допустимая доза составляла 50 шагов дозы лекарственного средства Ксалтофай и 50 единиц для инсулина деглюдек. В 48,7% пациентов, получавших Ксалтофай, было достигнуто целевой уровень HbA1c <7% без подтвержденных эпизодов гипогликемии. Эта доля была значительно больше, чем при применении инсулина деглюдек (15,6%; отношение шансов: 5,57; p <0,0001).
Ключевые результаты исследования приведены на рисунке 5 и в таблице 4.
Рис. 5. Средние уровни HbA1c (в%) по неделям лечения у пациентов с сахарным диабетом 2-го типа с неудовлетворительным контролем при применении базального инсулина.
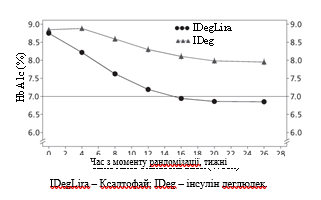
Частота случаев тяжелой гипогликемии на один пациенто-год экспозиции (доля пациентов в процентах) составила 0,01 (1 из 199 пациентов) при применении лекарственного средства Ксалтофай и 0,00 (ни один из 199 пациентов) при применении инсулина деглюдек. Частота случаев ночной гипогликемии была похожей при лечении лекарственным средством Ксалтофай и инсулином деглюдек.
Таблица 4. Результаты через 26 недель. Переход по терапии базальным инсулином.
Переход по терапии инсулином гларгин (100 ЕД / мл) | Переход по терапии базальным инсулином [НПХ-инсулин (нейтральный протамин Хагедорна), инсулин детемир, инсулин гларгин] | |||
Халтофай | Инсулин гларгин, без ограничения дозы | Халтофай | Инсулин деглюдек, максимальная разрешенная доза - 50 единиц | |
N | 278 | 279 | 199 | 199 |
HbA1c,% | ||||
Начало → конец исследования | 8,4→6,6 | 8,2→7,1 | 8,7→6,9 | 8,8→8,0 |
среднее изменение | ˗1,81 | ₋1,13 | ₋1,90 | ₋0,89 |
рассчитана разница | 0,59AB [₋0,74; ₋0,45] | ₋1,05AB [₋1,25; ₋0,84] | ||
Пациенты (%), которые достигли HbA1c <7% | ||||
все пациенты | 71,6 | 47,0 | 60,3 | 23,1 |
Рассчитан показатель отношения шансов | 3,45B [2,36; 5,05] | 5,44B [3,42; 8,66] | ||
Пациенты (%), которые достигли HbA1c £ 6,5% | ||||
все пациенты | 55,4 | 30,8 | 45,2 | 13,1 |
Рассчитан показатель отношения шансов | 3,29B [2,27; 4.75] | 5,66B [3,37; 9,51] | ||
Частота случаев подтвержденной гипогликемии * на один пациенто-год экспозиции (доля пациентов в%) | 2,23 (28,4%) | 5,05 (49,1%) | 1,53 (24,1%) | 2,63 (24,6%) |
рассчитано соотношение | 0,43AB [0,30; 0,61] | 0,66 [0,39; 1,13] | ||
Масса тела, кг | ||||
Начало → конец исследования | 88,3→86,9 | 87,3→89,1 | 95,4→92,7 | 93,5→93,5 |
среднее изменение | ₋1,4 | 1,8 | -2,7 | 0,0 |
рассчитана разница | ₋3,20AB [₋3,77; ₋2,64] | ₋2,51B [₋3,21; ₋1,82] | ||
ГПН, ммоль/л | ||||
Начало → конец исследования | 8,9→6,1 | 8,9→6,1 | 9,7→6,2 | 9,6→7,0 |
среднее изменение | ₋2,83 | ₋2,77 | ₋3,46 | ₋2,58 |
рассчитана разница | ₋0,01 [₋0,35; 0,33] | 0,73C [1,19; ₋0,27] | ||
Доза в конце исследования | ||||
Инсулин, единиц | 41 | 66D | 45 | 45 |
Лираглутид, мг | 1,5 | - | 1,7 | - |
Рассчитана разница доза базального инсулина | ₋25,47B [₋28,90; 22,05] | ₋0,02 [₋1,88; 1,84] | ||
Зарегистрированные показатели перед началом, в конце лечения и их изменение. Последние зарегистрированные показатели перенесены вперед. 95% доверительный интервал указан в квадратных скобках ([]).
* Подтверждена гипогликемия определяется как тяжелая форма гипогликемии (эпизод, при котором требуется помощь со стороны другого человека) и / или легкая гипогликемия (уровень глюкозы в плазме крови <3,1 ммоль / л, независимо от симптомов).
A Конечные точки с подтвержденной преимуществом лекарственного средства Ксалтофай по сравнению с препаратом сравнения;
B p <0,0001; C p <0,05;
D средняя доза инсулина гларгин, что была применена перед началом исследования, составила 32 единицы.
Результаты исследования продолжительностью 26 недель, в ходе которого изучалось применение лекарственного средства Ксалтофай по сравнению с лечением базально-болюсным режимом инсулинотерапии, Включавшая базальный инсулин (инсулин гларгин 100 ЕД / мл) в сочетании с болюсным инсулином (инсулин аспарт), при участии пациентов с сахарным диабетом 2-го типа с неудовлетворительным контролем при применении инсулина гларгин и метформина, продемонстрировали похоже снижение уровня HbA1c в обеих группах лечения (средний показатель в обеих группах составлял от 8,2% до 6,7%). В обеих группах в 66-67% пациентов был достигнут уровень HbA1c <7%. По сравнению с данными до начала лечения наблюдалось уменьшение массы тела в среднем на 0,9 кг при применении лекарственного средства Ксалтофай и увеличение на 2,6 кг у пациентов, получавших базально-болюсной режим инсулинотерапии, причем рассчитана разница в зависимости от лечения составляла ₋3 57 кг (95% доверительный интервал: ₋4,19; ₋2,95). Доля пациентов в процентах, у которых наблюдалась тяжелая гипогликемия или подтверждена симптоматическая гипогликемия, составила 19,8% в группе лекарственного средства Ксалтофай и 52,6% - в группе лечения с применением базально-болюсного режима инсулинотерапии, а рассчитано отношение показателей частоты составил 0,11 (95% ДИ : 0,08-0,17). Суммарная суточная доза инсулина в конце исследования составляла 40 единиц у пациентов, получавших Ксалтофай и 84 единицы (52 единицы базального инсулина и 32 единицы болюсного инсулина) ⸻ у пациентов, получавших базально-болюсной режим инсулинотерапии.
Сердечно-сосудистая безопасность.
Исследования по сердечно-сосудистых последствий применения лекарственного средства Ксалтофай не проводились.
лираглутид
Исследование "Результаты оценки сердечно-сосудистых последствий влияния и действия лираглутид при диабете" было многоцентровым плацебо вдвойне слепым клиническим исследованиям. 9340 пациентов были рандомизированы образом распределены по группам применения лираглутид (4668 пациентов) или плацебо (4672 пациента), в обеих группах препараты добавлялись к стандартной терапии, которая влияла на уровень HbA1c и факторы сердечно-сосудистых (СС) рисков. Информация о первичных результаты или состояние здоровья в конце исследования была получена относительно 99,7% и 99,6% участников исследования, рандомизированное образом распределенных по группам применения лираглутид или плацебо соответственно. Продолжительность периода наблюдения составила не менее 3,5 года и не более 5 лет. Когорта исследования включала пациентов в возрасте ≥ 65 лет (n = 4329) и ≥ 75 лет (n = 836) и пациентов с легкой (n = 3907), умеренным (n = 1934) или тяжелым (n = 224) нарушением функции почек. Средний возраст пациентов составил 64 года, а средний ИМТ (индекс массы тела) ⸻ 32,5 кг / м². Средняя продолжительность заболевания диабетом составляла 12,8 года.
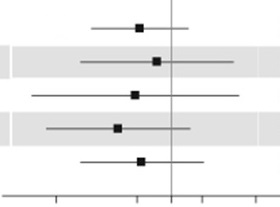
Первичной конечной точкой исследования было время после рандомизации до появления первых серьезных побочных сердечно-сосудистых явлений (СПССЯ), а именно: смерти по причине СС патологии, нелетального инфаркта миокарда или нелетального инсульта. Применение лираглутид дало лучшие результаты в предотвращении СПССЯ по сравнению с плацебо (см. Рисунок 6).
Рис. 6. Диаграмма данных анализа отдельных типов сердечно-сосудистых явлений. Популяция пациентов с полным пакетом данных для анализа.
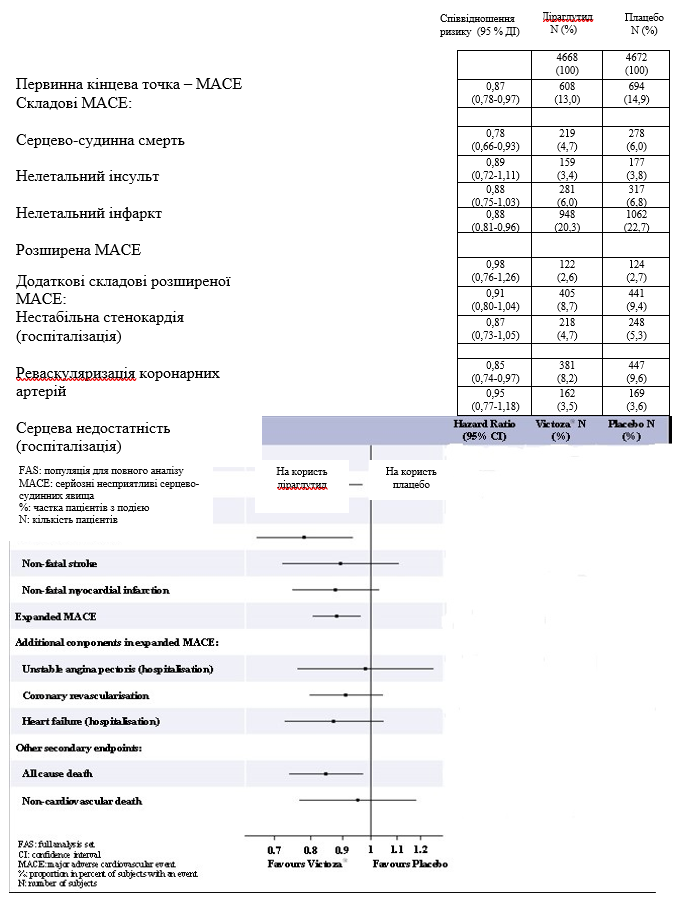
При применении лираглутид по сравнению с плацебо при их добавлении к стандартной терапии наблюдалось снижение уровня HbA1c от начала исследования до 36-го месяца лечения [₋1,16% по сравнению с ₋0,77%; рассчитана разница между группами лечения ₋0,40% (₋0,45; ₋0,34)].
инсулин деглюдек
Исследование "DEVOTE" было рандомизированное двойное слепое сосредоточенным на определенных явлениях клиническим исследованиям продолжительностью 2 года с целью сравнения сердечно-сосудистой безопасности применения инсулина деглюдек и инсулина гларгин (100 ЕД / мл) в 7637 пациентов с сахарным диабетом 2-го типа с высоким риском сердечно -сосудистых явлений.
Первичной конечной точкой исследования было время после рандомизации до первого появления любого из трех серьезных побочных сердечно-сосудистых явлений (СПССЯ), которые определялись как смерть по причине сердечно-сосудистой патологии, нелетальный инфаркт миокарда или нелетальный инсульт. Это исследование планировалось исследование для доказательства не более риска развития СПССЯ при применении инсулина деглюдек по сравнению с инсулином гларгин с учетом предварительно заданного порога отношение рисков (ОР) на уровне 1,3. Была подтверждена сердечно-сосудистая безопасность инсулина деглюдек по сравнению с инсулином гларгин [ОР: 0,91 (0,78; 1,06)] (см. Рисунок 7).
В обеих группах лечения уровень HbA1c перед началом исследования составил 8,4%, а через 2 года ⸻7,5% при применении в качестве инсулина деглюдек, так и инсулина гларгин.
Рис. 7. Диаграмма данных анализа комплексной конечной точки СПССЯ, состоящий из трех компонентов и отдельных сердечно-сосудистых конечных точек в исследовании "DEVOTE".
Соотно-ния рисков (95% ДИ) | инсулин деглюдек N (%) | инсулин гларгин N (%) | |||||||
Основной анализ (3-компонентный показатель MACE) |
| 0,91 (0,78-1,06) | 325 (8,51) | 356 (9,32) | |||||
Смерть з с-с причин | 0,96 (0,76-1,21) | 136 (3,56) | 142 (3,72) | ||||||
нефатальный инсульт | 0,90 (0,65-1,23) | 71 (1,86) | 79 (2,07) | ||||||
нефатальный ИМ | 0,85 (0,68-1,06) | 144 (3,77) | 169 (4,43) | ||||||
Смерть с каким-либо причинам | 0,91 (0,76-1,11) | 202 (5,29) | 221 (5,79) | ||||||
0,7 0,9 1 1,1 1,3 | |||||||||
В пользу инсулина деглюдек | В пользу инсулина гларгин | ||||||||
N - количество пациентов с первым событием, подтвержденной EAC , которая возникла в ходе исследования.
% - процент пациентов с первым событием, подтвержденной EAC, от общего количества рандомизированных пациентов.
EAC - комитет по экспертной оценке.
С-c - cерцево-сосудистый.
ИМ - инфаркт миокарда.
ДИ - 95% доверительный интервал.
Секреция инсулина / функция бета-клеток
По сравнению с инсулином деглюдек, Ксалтофай улучшает функцию бета-клеток, о чем свидетельствуют результаты измерения, полученные на модели гомеостаза для оценки функции бета-клеток. Улучшенная секреция инсулина по сравнению с инсулином деглюдек была продемонстрирована через 52 недели лечения в 260 пациентов с диабетом 2-го типа в ходе исследования по стандартизированным приемом пищи. Данные за период после 52 недель лечения отсутствуют.
артериальное давление
У пациентов с неудовлетворительным контролем при применении монотерапии метформином или его комбинации с пиоглитазоном применения лекарственного средства Ксалтофай способствовало снижению среднего систолического артериального давления на 1,8 мм рт. ст. по сравнению со снижением на 0,7 мм рт. ст. при применении инсулина деглюдек и на 2,7 мм рт. ст. - лираглутид. У пациентов с неудовлетворительным контролем при применении монотерапии сульфонилмочевины или его комбинации с метформином такое снижение составило 3,5 мм рт. ст. при применении лекарственного средства Ксалтофай и 3,2 мм рт. ст. при приеме плацебо. Разница не была статистически значимой. В ходе трех исследований с привлечением пациентов с неудовлетворительным контролем при применении базального инсулина систолическое артериальное давлениеснижался на 5,4 мм рт. ст. при применении лекарственного средства Ксалтофай и на 1,7 мм рт. ст. - при применении инсулина деглюдек при статистически значимой рассчитанной разницы результатов между группами лечения ₋3,71 мм рт. ст. (p = 0,0028) артериальное давление снижалось на 3,7 мм рт. ст. при применении лекарственного средства Ксалтофай по сравнению с 0,2 мм рт. ст. при применении инсулина гларгин при статистически значимой рассчитанной разницы результатов между группами лечения ₋3,57 мм рт. ст. (p <0,001) и на 4,5 мм рт. ст. при применении лекарственного средства Ксалтофай по сравнению с 1,16 мм рт. ст. при применении инсулина гларгин 100 ЕД / мл вместе с инсулином аспарт при статистически значимой рассчитанной разницы результатов между группами лечения ₋3,70 мм рт. ст. (p = 0,0003).
Фармакокинетика
Вообще, фармакокинетика инсулина деглюдек и лираглутид при применении лекарственного средства Ксалтофай клинически значимо не отличалась по сравнению с отдельными инъекциями инсулина деглюдек и лираглутид.
Ниже приведена информация о фармакокинетических свойствах лекарственного средства Ксалтофай, если не указано, что представленные данные получены при применении отдельно инсулина деглюдек или отдельно лираглутид.
Всасывания.
Общая экспозиция инсулина деглюдек была одинаковой после введения лекарственного средства Ксалтофай и отдельного введения инсулина деглюдек, тогда как Cmax была выше на 12%. Общая экспозиция лираглутид была одинаковой после введения лекарственного средства Ксалтофай и отдельного введения лираглутид, тогда как Cmax была ниже на 23%. Такая разница считается клинически незначимой, поскольку начальная доза лекарственного средства Ксалтофай и ее коррекция избираются индивидуально в соответствии с целевым уровня глюкозы в крови каждого отдельного пациента.
По результатам популяционного фармакокинетического анализа, экспозиция инсулина деглюдек и лираглутид увеличивалась пропорционально дозе лекарственного средства Ксалтофай во всем диапазоне доз.
Фармакокинетический профиль лекарственного средства Ксалтофай позволяет вводить один раз в сутки, а равновесная концентрация инсулина деглюдек и лираглутид достигается через 2-3 дня ежедневного введения лекарственного средства.
Распределение.
Инсулин деглюдек и лираглутид активно связываются с белками плазмы (> 99% и> 98% соответственно).
Метаболизм.
Инсулин деглюдек.
Распад инсулина деглюдек происходит подобно деградации инсулина человека; все метаболиты, при этом образуются, являются неактивными.
Лираглутид.
В течение 24 часов после введения однократной дозы [3H] -миченого лираглутид здоровым волонтерам, главным компонентом препарата в плазме крови оставался неизменен лираглутид. Были обнаружены два второстепенные метаболиты в плазме (≤ 9% и ≤ 5% суммарной радиоактивно меченой дозы в плазме). Лираглутид метаболизируется аналогично большим по размеру белкам, и ни один конкретный орган не является главным путем выведения из организма.
Вывод.
Период полувыведения инсулина деглюдек из организма составляет примерно 25 часов, а лираглутид - примерно 13 часов.
Особые группы пациентов.
Пациенты пожилого возраста.
По результатам популяционного фармакокинетического анализа, охватывающего данные взрослых пациентов в возрасте до 83 лет, которые применяли Ксалтофай, возраст не влиял клинически значимым образом на фармакокинетику лекарственного средства Ксалтофай.
Стать.
По результатам популяционного фармакокинетического анализа данных, пол не влияла клинически значимым образом на фармакокинетику лекарственного средства Ксалтофай.
Этническое происхождение.
По результатам популяционного фармакокинетического анализа, охватывающего данные пациентов европеоидной, негроидной, индийской, азиатской и испанской этнических групп, этническое происхождение не влияло клинически значимым образом на фармакокинетику лекарственного средства Ксалтофай.
Нарушение функции почек.
Инсулин деглюдек.
Не выявлено разницы в фармакокинетике инсулина деглюдек между здоровыми волонтерами и пациентами с нарушением функции почек.
лираглутид
У пациентов с нарушением функции почек экспозиция лираглутид была ниже, по сравнению с людьми с нормальной функцией почек. У пациентов с легким (клиренс креатинина CrCl: 50˗80 мл / мин.), Умеренным (CrCl: 30˗50 мл / мин), тяжелым (CrCl <30 мл / мин) нарушением функции почек и с терминальной стадией заболевания почек, требовала гемодиализа, наблюдалось снижение экспозиции лираглутид на 33%, 14%, 27% и 26% соответственно.
Также в ходе клинического исследования продолжительностью 26 недель у пациентов с сахарным диабетом 2-го типа и с нарушением функции почек средней степени тяжести (CrCL: 30-59 мл / мин) экспозиция лираглутид была на 26% ниже, чем в привлеченных к другому исследования пациентов с сахарным диабетом 2-го типа с нормальной функцией почек или с легким нарушением функции почек.
Нарушение функции печени.
Инсулин деглюдек.
Не выявлено разницы в фармакокинетике инсулина деглюдек между здоровыми волонтерами и пациентами с нарушением функции печени.
Лираглутид.
Фармакокинетику лираглутид оценивали у пациентов с разной степенью нарушения функции печени в ходе исследования с применением одноразовых доз препарата. У пациентов с нарушением функции печени легкой или средней степени тяжести экспозиция лираглутид была меньше на 13-23%, чем у здоровых людей. У пациентов с тяжелым нарушением функции печени (> 9 баллов по шкале Чайлда˗Пью) экспозиция была значительно меньше (44%).
Дети .
Исследование применения лекарственного средства Ксалтофай у детей и подростков в возрасте до 18 лет не проводились.
Доклинические данные по безопасности.
Программа доклинической разработки инсулина деглюдек / лираглутид включала основные исследования комбинированной токсичности продолжительностью до 90 дней в едином соответствующем требованиям виде животных (крысы линии Вистар) с целью получения данных для поддержки программы клинической разработки лекарственного средства. Локальную переносимость оценивали на кроликах и свиньях.
По результатам исследований токсичности повторных доз, доклинические данные по безопасности показали отсутствие проблем безопасности для человека.
Реакции тканей в месте введения лекарственного средства, зарегистрированные в ходе двух исследований на кроликах и свиньях соответственно, ограничивались реакциями воспаление легкой степени тяжести.
Исследования по оценке канцерогенности, мутагенности или нарушения фертильности при применении комбинации инсулина деглюдек с лираглутид не проводились. Приведенные ниже данные получены в ходе исследований отдельно инсулина деглюдек и отдельно лираглутид.
Инсулин деглюдек.
По результатам доклинических исследований фармакологической безопасности, токсичности повторных доз, возможной канцерогенности и репродуктивной токсичности не выявлено угрозы для безопасности человека.
Соотношение митогеном и метаболической активности инсулина деглюдек не отличается от инсулина человека.
Лираглутид.
По результатам доклинических исследований фармакологической безопасности, токсичности повторных доз или генотоксичности не обнаружено угрозы для безопасности человека. В ходе исследований канцерогенности продолжительностью 2 года у крыс и мышей наблюдалось образование смертельных С-клеточных опухолей щитовидной железы. У крыс не было определено дозу, которая не вызывает видимых побочных эффектов. Такие опухоли не были обнаружены у обезьян, получавших лечение в течение 20 месяцев. Такие результаты применения лекарственного средства у грызунов вызванные Негенотоксичные специфическим механизмом с участием рецепторов ГПП-1, к которому грызуны особенно чувствительными. Похоже, что релевантность таких последствий для организма человека низкая, однако ее нельзя исключить полностью. Не было выявлено других опухолей связанных с лечением.
В ходе экспериментов на животных не было выявлено прямого вредного воздействия на фертильность, однако при введении высоких доз отмечалось незначительное повышение ранней эмбриональной смертности. Применение лираглутид в середине периода беременности приводило к уменьшению массы тела самок и замедление развития плода с неясным воздействием на ребра у крыс и нарушение скелета у кроликов. При применении самой дозы лираглутид у крыс наблюдалось замедление роста новорожденных, которое оставалось и в течение периода после отлучения от материнского кормления. Неизвестно, чем именно вызвано такое замедление роста крысят - уменьшением потребления ими материнского молока вследствие непосредственного воздействия ГПП-1 или уменьшением образования молока у кормящих вследствие меньшего потребления калорий.
Клинические характеристики
Ксалтофай Показания
Лекарственное средство Ксалтофай применяют при недостаточно контролируемом сахарном диабете II типа у взрослых с целью улучшения гликемического контроля как дополнение к диете, физических упражнений и других пероральных лекарственных средств для лечения сахарного диабета.
Противопоказания
Повышенная чувствительность к действующим веществам или другим компонентам, которые указаны в списке вспомогательных веществ.
Особые меры безопасности.
Предварительно наполнена шприц-ручка предназначена для использования с одноразовыми иглами НовоТвист® или НовоФайн длиной до 8 мм калибром 32G.
Предварительно наполнена шприц-ручка предназначена только для индивидуального пользования.
Ксалтофай нельзя использовать, если раствор не прозрачен и не бесцветный.
Ксалтофай нельзя использовать, если он был заморожен.
Для каждой инъекции необходимо всегда использовать новую иглу. Использованные иглы нельзя применять во второй раз. После каждой инъекции пациент должен выбрасывать использованную иглу.
В случае закупорки иглы пациент должен придерживаться рекомендаций, приведенных ниже.
Неиспользованный препарат или отходы следует утилизировать в соответствии с местными требованиями.
См. подробную инструкция по использованию шприц-ручки лекарственного средства, сопровождает лекарственное средство.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Фармакодинамическая взаимодействие.
Исследование взаимодействия лекарственного средства Ксалтофай с другими лекарствами не проводились.
Ряд веществ нарушают метаболизм глюкозы и могут требовать коррекции дозы лекарственного средства Ксалтофай.
Вещества способны, приводить к уменьшению потребности в лекарственном средстве Ксалтофай: противодиабетические лекарственные средства, ингибиторы моноаминоксидазы (МАО), блокаторы бета-адренорецепторов, ингибиторы АПФ (АПФ), салицилаты, анаболические стероиды и сульфаниламиды.
Вещества, способные приводить к увеличению потребности в лекарственном средстве Ксалтофай: пероральные контрацептивы, тиазиды, глюкокортикоиды, гормоны щитовидной железы, симпатомиметики, гормоны роста и даназол.
Блокаторы бета-адренорецепторов способны маскировать симптомы гипогликемии.
Октреотид / ланреотид могут приводить как к увеличению, так и к уменьшению потребности в лекарственном средстве Ксалтофай.
Алкоголь может усиливать или уменьшать гипогликемический эффект действия лекарственного средства Ксалтофай.
Фармакокинетическая взаимодействие.
Данные экспериментов in vitro свидетельствуют о том, что возможность фармакокинетического взаимодействия лекарств, метаболизм которых связан с CYP и связыванием с белками плазмы крови, является очень низкой как для лираглутид, так и для инсулина деглюдек.
Небольшая задержка опорожнения желудка, наблюдается при применении лираглутид, может влиять на всасывание одновременно введенных пероральных лекарственных средств. Исследование взаимодействия лекарств не показали ни клинически значимой задержки всасывания.
Варфарин и другие производные кумарина.
Исследование взаимодействия не проводились. Нельзя исключить возможность клинически значимого взаимодействия с слаборастворимые действующими веществами или с действующими веществами с узким терапевтическим индексом, такими как варфарин. После начала лечения ликарськм средством Ксалтофай пациентам, принимающим варфарин или другие производные кумарина, рекомендуется более частый контроль МНО (международное нормализованное отношение).
Парацетамол.
Лираглутид не вызывало изменения общей экспозиции парацетамола после приема однократной дозы 1000 мг. Cmax (максимальная концентрация) парацетамола уменьшалась на 31%, а медиана tmax (время до достижения максимальной концентрации) увеличивалась до 15 минут. При одновременном применении с парацетамолом коррекция дозы не требуется.
Аторвастатин.
Лираглутид не вызывало клинически существенного изменения общей экспозиции аторвастатина после однократного применения аторвастатина в дозе 40 мг. Таким образом, при одновременном применении аторвастатина с лираглутид коррекция дозы аторвастатина не нужна. При одновременном применении аторвастатина и лираглутид Cmax аторвастатина уменьшалась на 38%, а медиана tmax увеличивалась от 1:00 до 3:00.
Гризеофульвин.
Лираглутид не вызывало клинически существенного изменения общей экспозиции гризеофульвина после однократного применения гризеофульвина в дозе 500 мг. Cmax гризеофульвина увеличивалась на 37%, тогда как медиана tmax оставалась неизменной. Коррекция дозы гризеофульвина и других веществ с слабой растворимостью и высокой проницаемостью не нужна.
Дигоксин.
Однократное применение дигоксина в дозе 1 мг одновременно с лираглутид приводило к уменьшению AUC (площадь под кривой) дигоксина на 16%; Cmax уменьшалась на 31%. Медиана времени до достижения максимальной концентрации дигоксина (tmax) увеличивалась от 1 часа до 1,5 часа. Таким образом, коррекция дозы дигоксина не нужна.
Лизиноприл.
Однократное применение лизиноприла в дозе 20 мг одновременно с лираглутид приводило к уменьшению AUC лизиноприла на 15%; Cmax уменьшалась на 27%. При применении лираглутид медиана tmax лизиноприла увеличивалась от 6 часов. до 8 часов. Исходя из этих результатов, коррекция дозы лизиноприла не нужна.
Пероральные контрацептивы.
Лираглутид вызывал уменьшение Cmax этинилэстрадиола и левоноргестрела на 12% и 13% соответственно после приема однократной дозы каждого из этих пероральных противозачаточных препаратов. Применение лираглутид приводило к уменьшению tmax обоих веществ на 1,5 часа. Клинически важное влияние на общую экспозицию как этинилэстрадиола, так и левоноргестрела не наблюдалось. Таким образом, ожидается, что при одновременном применении противозачаточных препаратов с лираглутид контрацептивный эффект не нарушается.
Особенности применения
Ксалтофай не следует применять пациентам с сахарным диабетом 1-го типа или для лечения диабетического кетоацидоза.
Гипогликемия.
Если доза лекарственного средства Ксалтофай является большей необходимой, может развиться гипогликемия. Пропуск приема пищи или непредвиденная напряженная физическая деятельность может привести к развитию гипогликемии. При комбинированном применении с препаратами сульфонилмочевины риск развития гипогликемии можно снизить путем уменьшения дозы сульфонилмочевины. Наличие сопутствующих болезней почек, печени или заболеваний, поражающих надпочечник, гипофиз или щитовидную железу, может потребовать изменения дозы лекарственного средства Ксалтофай. У пациентов с существенным улучшением контроля уровня глюкозы (например, при интенсификации терапии) может наблюдаться изменение привычных предупредительных симптомов гипогликемии, о чем им надо сообщить. У пациентов с длительным диабетом привычные симптомы гипогликемии (см. Раздел «Побочные реакции») могут исчезнуть.
Гипергликемия.
Введение неадекватных доз и / или прекращения противодиабетической терапии может привести к развитию гипергликемии и, возможно, к возникновению гиперосмолярной комы. В случае прекращения лечения лекарственным средством Ксалтофай необходимо обеспечить соблюдение инструкций по применению альтернативных противодиабетических лекарств. Кроме того, возникновение сопутствующих заболеваний, особенно инфекционных, может привести к развитию гипергликемии и, таким образом, привести к увеличению потребности в противодиабетических терапии. Обычно, первые симптомы гипергликемии развиваются постепенно, в течение нескольких часов или дней. Они включают жажду, повышенную частоту мочеиспускания, тошноту, рвоту, сонливость, гиперемия и сухость кожи, сухость рта и потерю аппетита, а также запах ацетона изо рта.
В случае тяжелой формы гипергликемии следует рассмотреть возможность применения инсулина быстрого действия. При отсутствии лечения гипергликемические явления могут в конце концов привести к возникновению гиперосмолярной комы / диабетического кетоацидоза, которые могут быть смертельно опасными.
Комбинированное применение пиоглитазона с препаратами инсулина.
Сообщалось о случаях развития сердечной недостаточности при применении пиоглитазона в комбинации с препаратами инсулина, особенно у пациентов с факторами риска развития застойной сердечной недостаточности. Это следует учитывать, назначая лечение комбинацией пиоглитазона с лекарственным средством Ксалтофай. При применении такой комбинированной терапии необходимо наблюдать за состоянием пациента на предмет возникновения у него признаков и симптомов сердечной недостаточности, увеличение веса и отеков. В случае какого-либо ухудшения функции сердца лечение пиоглитазоном следует прекратить.
Нарушение зрения.
Интенсификация терапии инсулином, который является составной лекарственного средства Ксалтофай, с быстрым улучшением гликемического контроля может сопровождаться временным ухудшением диабетической ретинопатии, но долговременное улучшение гликемического контроля приводит к уменьшает риск прогрессирования диабетической ретинопатии.
Образование антител.
Применение лекарственного средства Ксалтофай может вызвать образование антител к инсулину деглюдек и / или лираглутид. В редких случаях присутствие таких антител может потребовать коррекции дозы лекарственного средства Ксалтофай для предотвращения развития гипер- или гипогликемии. В очень небольшого числа пациентов лечение лекарственным средством Ксалтофай вызывало образование антител, которые являются специфическими к инсулину деглюдек, перекрестных антител к инсулину человека или антител к лираглутид. Образование антител не сопровождалось снижением эффективности лекарственного средства Ксалтофай.
Острый панкреатит.
При применении агонистов рецепторов ГПП-1, в том числе лираглутид, наблюдались случаи острого панкреатита. Пациентам следует рассказать о характерные симптомы острого панкреатита. При подозрении на панкреатит лечение лекарственным средством Ксалтофай следует прекратить; в случае подтверждения диагноза острого панкреатита лечение лекарственным средством Ксалтофай восстанавливать не следует.
Побочные явления со стороны щитовидной железы.
В ходе клинических исследований при применении агонистов рецепторов ГПП-1, в том числе лираглутид, сообщалось о случаях возникновения побочных явлений со стороны щитовидной железы (например, зоб), в частности у пациентов с уже имеющимся заболеванием щитовидной железы. В связи с этим, таким пациентам Ксалтофай следует применять с осторожностью.
Воспалительное заболевание кишечника и диабетический Гастропарез.
Опыт применения лекарственного средства Ксалтофай пациентам с воспалительным заболеванием кишечника и диабетическим гастропарезом отсутствует. В связи с этим таким пациентам не рекомендуется принимать Ксалтофай.
Дегидратация.
В ходе клинических исследований при применении агонистов рецепторов ГПП-1, в том числе лираглутид, входящий в состав лекарственного средства Ксалтофай, сообщалось о случаях возникновения признаков и симптомов дегидратации, включая нарушение функции почек и острую почечную недостаточность. Пациенты, применяющие препарат Ксалтофай, должны быть проинформированы о риске дегидратации, связанный с побочными эффектами со стороны желудочно-кишечного тракта, и должны принимать меры для предотвращения гиповолемии.
Предотвращения ошибочного применению лекарственного средства.
Пациентов следует проинструктировать о необходимости всегда проверять надпись на этикетке шприц-ручки перед каждой инъекцией чтобы уникненуты случайного переплутання лекарственного средства Ксалтофай с другими инъекционными гипогликемическими лекарствами.
Пациенты должны визуально проверять на счетчике шприц-ручки количество единиц набранной дозы. Таким образом, условием самостоятельного введения лекарственного средства пациентами является их способность прочитать цифры на счетчике дозы. Следует проинструктировать незрячих пациентов или пациентов со слабым зрением о необходимости всегда пользоваться помощью / поддержкой со стороны других людей с хорошим зрением, которые умеют применять прибор для введения инсулина.
Чтобы предотвратить ошибочном дозировке и потенциальному передозировке, пациенты и медицинские специалисты не должны ни в коем случае применять другой шприц для набора лекарственного средства из картриджа предварительно наполненной шприц-ручки.
В случае закупорки иглы пациент должен придерживаться рекомендаций, приведенных в инструкция по использованию шприц-ручки лекарственного средства.
Категории пациентов, не охваченных исследованиями.
Исследование о переходе с терапии базальным инсулином в дозах <20 и> 50 единиц на лечение лекарственного средства Ксалтофай не проводились.
Опыт лечения пациентов с застойной сердечной недостаточностью класса IV по классификации Нью-Йоркской ассоциации кардиологов (NYHA) отсутствует, в связи с чем применение лекарственного средства Ксалтофай таким пациентам не рекомендуется.
Ксалтофай содержит менее 1 ммоль натрия (23 мг) в одной дозе, поэтому этот препарат считается практически не содержит натрия.
Применение в период беременности или кормления грудью
Беременность.
Клинический опыт применения лекарственного средства Ксалтофай, инсулина деглюдек или лираглутид беременным женщинам отсутствует. Если пациентка хочет забеременеть или становится беременной, лечение лекарственным средством Ксалтофай следует прекратить.
Исследование репродуктивной функции на животных с применением инсулина деглюдек не выявили никакой разницы между инсулином деглюдек и инсулином человека относительно эмбриотоксичности и тератогенности. Исследование лираглутид на животных показали наличие репродуктивной токсичности (см. « Доклинические данные по безопасности») выше. Потенциальный риск для человека неизвестен.
Кормления грудью.
Клинический опыт применения лекарственного средства Ксалтофай в период кормления грудью отсутствует. Неизвестно, проникает инсулин деглюдек или лираглутид в грудное молоко. В связи с недостатком опыта, Ксалтофай не следует применять в период кормления грудью.
У крыс инсулин деглюдек проникал в молоко; его концентрация в молоке буле меньше, чем в плазме крови. Исследования на животных показало низкий ступень поступления лираглутид и близких ему по структуре метаболитов в молоко. Доклинические исследования применения лираглутид показали связано с лечением замедление неонатального роста в сосунков крыс (см. «Доклинические данные по безопасности») выше.
Фертильность.
Клинический опыт применения лекарственного средства Ксалтофай в контексте изучения фертильности отсутствует.
Исследования на животных по применению инсулина деглюдек не обнаружили ни одного отрицательного влияния на фертильность. Кроме незначительного уменьшения числа живых зародышей, исследования на животных с применением лираглутид не обнаружили никаких свидетельств вредного воздействия на фертильность.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
При гипогликемии способность пациента к концентрации внимания и скорость реакции могут ухудшиться. Это может быть рисковым в тех ситуациях, когда такие способности особенно важными (например, при управлении транспортными средствами или работе с механизмами).
Пациентам необходимо рекомендовать принимать определенные меры, чтобы предотвратить развитие гипогликемии при управлении транспортными средствами. Это особенно важно для тех пациентов, у которых наблюдается снижение или отсутствие осознания угрожающих признаков гипогликемии или у которых наблюдаются частые эпизоды гипогликемии. В таких случаях следует рассмотреть вопрос о целесообразности управления транспортными средствами.
Способ применения Ксалтофай и дозы
Дозировки.
Лекарственное средство Ксалтофай вводится подкожно один раз в сутки. Лекарственное средство Ксалтофай можно вводить в любое время в течение дня, желательно в одно и то же время.
Доза лекарственного средства Ксалтофай подбирается с учетом индивидуальных потребностей пациента. Рекомендовано оптимизировать гликемический контроль путем коррекции дозы в зависимости от уровня глюкозы в плазме крови натощак.
Коррекция дозы может потребоваться при изменении физической активности или привычного рациона питания пациента и при сопутствующих заболеваниях.
Пациентам, пропустили своевременно ввести дозу препарата, рекомендуется сделать инъекцию сразу, как они об этом вспомнили, после чего вернуться к обычному режиму ввода - один раз в сутки. Интервал между инъекциями должен всегда составлять минимум 8:00. Это касается также тех случаев, когда ввод в одно и то же время суток невозможно.
Лекарственное средство Ксалтофай применяется путем введения шагов дозы. Один шаг дозы содержит 1 единицу инсулина деглюдек и 0,036 мг лираглутид. Предварительно заполненная шприц-ручка обеспечивает ввод от одного до пятидесяти шагов дозы в одной инъекции с постепенным увеличением дозы на одно шаг дозы. Максимальная суточная доза Ксалтофай составляет 50 шагов дозы (50 единиц инсулина деглюдек и 1,8 мг лираглутид). Счетчик на шприц-ручке показывает количество шагов дозы.
Добавление к пероральным сахароснижающих лекарственных средств .
Рекомендованная начальная доза лекарственного средства Ксалтофай составляет 10 шагов дозы (10 единиц инсулина деглюдек и 0,36 мг лираглутид).
Лекарственное средство Ксалтофай можно применять дополнительно к уже применяемых сахароснижающих лекарственных средств. При одновременном применении лекарственного средства Ксалтофай и сульфонилмочевины, следует уменьшить дозу сульфонилмочевины (см. Раздел «Особенности применения»).
Переход от терапии агонистом рецепторов ГПП-1.
Перед тем, как начать лечение лекарственным средством Ксалтофай, применение агонистов рецепторов ГПП-1 следует прекратить. При переходе от терапии с применением агониста рецепторов ГПП-1 рекомендуемая начальная доза лекарственного средства Ксалтофай составляет 16 шагов дозы (16 единиц инсулина деглюдек и 0,6 мг лираглутид) (см. Раздел «Фармакологические»). Рекомендованную начальную дозу превышать нельзя. При переходе от лечения с применением агониста рецепторов ГПП-1 длительного действия (например, при введении один раз в неделю) необходимо учитывать его пролонгированное действие. Лечение лекарственным средством Ксалтофай следует начинать в тот момент времени, когда предполагался прием агониста рецепторов ГПП-1 длительного действия. Рекомендуется осуществлять тщательный контроль уровня глюкозы крови при переходе и в течение следующих недель.
Переход от терапии с применением базального инсулина.
Перед началом лечения лекарственным средством Ксальтофай, применение базального инсулина следует прекратить. При переходе от терапии с применением базального инсулина рекомендуемая начальная доза лекарственного средства Ксалтофай составляет 16 шагов дозы (16 единиц инсулина деглюдек и 0,6 мг лираглутид) (см. Разделы «Особенности применения» и «Фармакокинетика»). Рекомендованную начальную дозу превышать нельзя. Рекомендуется осуществлять тщательный контроль уровня глюкозы крови при переходе и в течение следующих недель.
Особые группы пациентов.
Пациенты пожилого возраста (≥ 65 лет). Лекарственное средство Ксалтофай можно применять пациентам пожилого возраста. Следует проводить более тщательный мониторинг уровня глюкозы в крови и коррекцию дозы выполнять индивидуально.
Нарушение функции почек. При применении лекарственного средства Ксалтофай пациентам с нарушением функции почек легкой, средней или тяжелой степени тяжести необходимо усилить контроль уровня глюкозы крови и обеспечить индивидуальную коррекцию дозы. Не рекомендуется применять препарат Ксалтофай пациентам с терминальной стадией заболевания почек ( см. Разделы «Фармакологические» и «Фармакокинетика») .
Нарушение функции печени. Лекарственное средство Ксалтофай можно применять пациентам с легкой или умеренной тяжести нарушения функции печени. Необходимо усилить контроль уровня глюкозы крови и обеспечить индивидуальную коррекцию дозы.
Не рекомендуется применять препарат Ксалтофай пациентам с тяжелым нарушением функции печени, из-за содержания лираглутид (см. Раздел «Фармакокинетика»).
Дети . Данные о применении лекарственного средства Ксалтофай у детей отсутствуют.
Способ введения.
Лекарственное средство Ксалтофай предназначен только для подкожного введения. Лекарственное средство Ксалтофай нельзя вводить внутривенно или внутримышечно.
Лекарственное средство Ксалтофай вводится подкожно путем инъекции в бедро, в плечо или в живот. Чтобы уменьшить риск развития липодистрофии, необходимо постоянно менять место инъекции даже в той же самой области введения препарата. За дальнейшими инструкциями по применению лекарственного средства необходимо обратиться к разделу «Особые меры безопасности».
Лекарственное средство Ксалтофай нельзя набирать шприцем с картриджа предварительно заполненной шприц-ручки (см. Раздел «Особые меры безопасности».).
Пациентов следует проинструктировать о необходимости всегда использовать новую иглу. Повторное использование инсулиновых игл повышает риск закупорки игл, может привести к введению недостаточной дозы или до введения чрезмерной дозы лекарственного средства. В случае закупорки иглы пациент должен придерживаться рекомендаций, приведенных в инструкция по использованию шприц-ручки лекарственного средства (см. Раздел «Особые меры безопасности».).
Подробная информация о результатах клинических исследований комбинации с другими препаратами, влияния на гликемический контроль и применение в различных популяциях предоставлена в разделах «Особенности применения», «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий», «Фармакологические».
Инструкция по использованию шприц-ручки лекарственного средства Ксалтофай 100 ЕД / мл + 3,6 мг / мл, раствор для инъекций.
Пожалуйста, внимательно прочитайте эту инструкцию перед применением Вашей предварительно наполненной шприц-ручки с лекарственным средством Ксалтофай.
Не используйте шприц-ручку, пока Ваш врач или медсестра не научат Вас правильно пользоваться ею .
Начните с проверки маркировки на своей шприц-ручке, чтобы убедиться, что она содержит именно Ксалтофай 100 ЕД / мл + 3,6 мг / мл, после чего внимательно просмотрите следующие иллюстрации, чтобы ознакомиться с различными частями Вашей шприц-ручки и иглой.
Если Вы незрячие или имеете слабое зрение и не видите цифры на счетчике дозы, не используйте эту шприц-ручку без посторонней помощи. Обратитесь за помощью к человеку с нормальным зрением, которая научилась правильному пользованию предварительно наполненной шприц-ручкой с лекарственным средством Ксалтофай.
Ксалтофай является лекарственным средством, содержащим инсулин деглюдек и лираглутид. Ксалтофай вводится с "шагом дозы". Один шаг дозы содержит 1 единицу инсулина деглюдек и 0,036 мг лираглутид.
Ваша предварительно наполнена шприц-ручка оборудована селектором дозы. Она содержит 3 мл лекарственного средства Ксалтофай в виде раствора. Шприц-ручка позволяет осуществить ввод таких доз:
- один шаг дозы
- до 50 шагов дозы максимум (что соответствует 50 единицам инсулина деглюдек + 1,8 мг лираглутид).
Ваша шприц-ручка позволяет вводить дозы порциями по одному шагу дозы.
Не перечисляет свою дозу. Набранное Вами число шагов дозы соответствует той цифре, которая показана на счетчике дозы шприц-ручки.
Ваша шприц-ручка предназначена для использования с одноразовыми иглами НовоТвист® или НовоФайн длиной до 8 мм калибром 32G. Иглы в комплект упаковки не входят.
Важно!
Обратите особое внимание на комментарии, помеченные таким символом, потому что они важны для безопасного применения шприц-ручки.
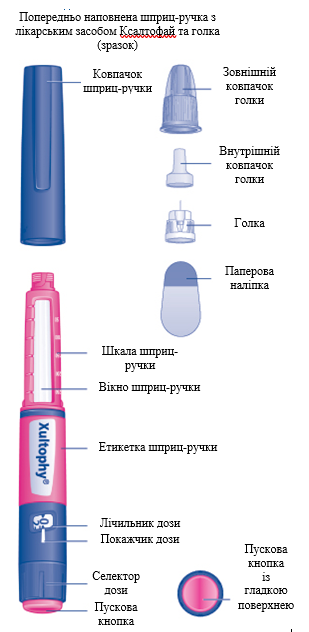
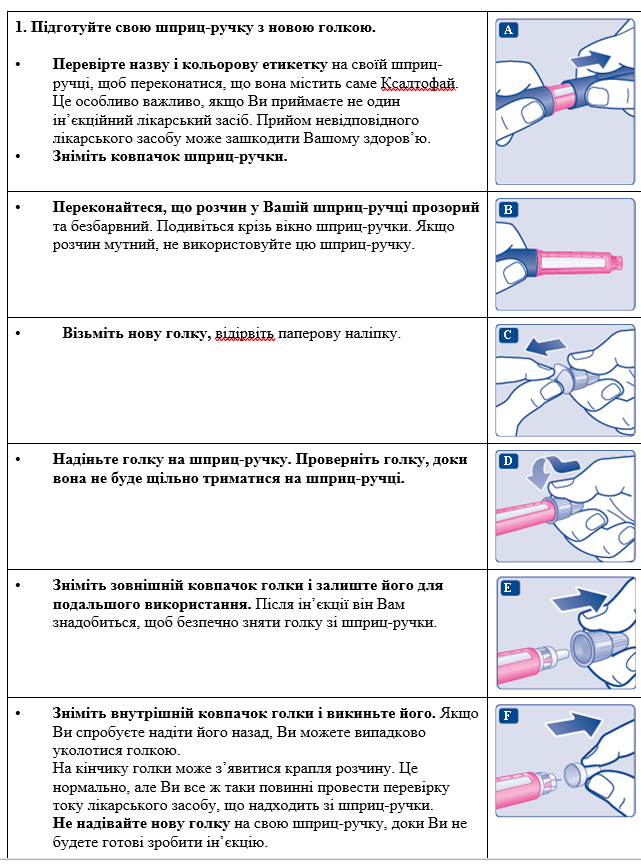
- Всегда используйте новую иглу для каждой инъекции.
Это позволит предотвратить закупоривание игл, загрязнению, инфицирование и введению неправильной дозы.
Никогда не используйте иглу, если она погнута или повреждена.

- Перед каждой инъекцией всегда убедитесь в том, что на кончике иглы появляется капля раствора . Это гарантирует поступление раствора.
Если капля не появляется, Вам не удастся ввести лекарственное средство, даже если счетчик дозы двигаться. Это может свидетельствовать о том, что игла закупорена или повреждена.
- Важно всегда перед каждой инъекцией проверять ток лекарственного средства со шприц-ручки. Если Вы не проверите ток раствора со шприц-ручки, Вы можете ввести недостаточное количество лекарственного средства или не ввести его совсем. Это может привести к слишком высокого уровня сахара в крови.
3. Выберите свою дозу.
• Проверните селектор дозы для выбора нужной Вам дозы.
Счетчик дозы показывает дозу в шагах дозы.
Если Вы установили неправильную дозу, можно вернуть селектор дозы вперед или назад, пока не выберете правильную дозу.
Максимальная доза, которую можно установить на шприц-ручке, составляет 50 шагов дозы.
Селектор дозы позволяет изменять количество шагов дозы.
Только счетчик дозы и указатель дозы покажут количество шагов дозы в выбранной Вами дозе.
Вы можете набрать до 50 шагов дозы на одну дозу. Если в Вашей шприц-ручке содержится менее 50 шагов дозы, счетчик остановится на отметке того количества шагов дозы осталась.
Когда селектор дозы проворачивают вперед, назад или когда выбранная доза превышает количество шагов дозы осталась в шприц-ручке, Вы слышите разное щелчок. Не считает количество щелчков.
- Перед каждой инъекцией лекарственного средства всегда посмотрите на счетчик дозы и на указатель дозы, чтобы проверить, какое именно количество шагов дозы Вы выбрали.
Не считает количество щелчков шприц-ручки. Если Вы наберете и введете неправильную дозу, уровень сахара в крови может стать слишком высоким или низким.
Не ориентируйтесь на показатели шкалы шприц-ручки, потому что она показывает только приблизительное количество раствора, оставшегося в Вашей шприц-ручке.
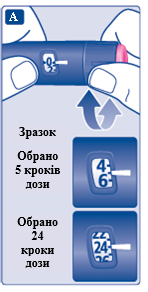

- Если Вы распределяете нужную Вам дозу таким образом, будьте очень внимательными при ее расчете.
Если Вы не уверены, укажите полную дозу, использовав новую шприц-ручку. Если Вы неправильно распределите нужную Вам дозу, Вы введете мало или много лекарственного средства. Это может привести к слишком высокого или слишком низкого уровня сахара у Вас в крови.
Как выявить закупорки или повреждения иглы?
• Если после длительного нажатия на пусковую кнопку на счетчике дозы не является отметка "0", это может означать, что игла, которую Вы применяете закупорена, или повреждена.
• Это означает, что Вы вовсе не получили лекарственное средство, даже если счетчик дозы сдвинулся с той начальной дозы, которую Вы установили.
Что делать с закупоренной иглой?
Замените иглу, как указано в пункте 5, и повторите все этапы, начиная с пункта 1 "Подготовьте свою шприц-ручку с новой иглой". Убедитесь в том, что Вы установили полную нужную Вам дозу.
Никогда не прикасайтесь счетчика дозы в ходе инъекции. Это может привести к прерыванию инъекции.

- Важно!
• Всегда имейте при себе запасную шприц-ручку и новые иглы в случае их утери или повреждения.
• Всегда храните свою шприц-ручку и иглы в скрытом и недоступном для других лиц, особенно для детей, месте .
• Никогда не давайте свою шприц-ручку другим людям. Ваши лекарства могут повредить их здоровью.
• Никогда не давайте свои иглы другим людям. Это может привести к перекрестного инфицирования.
• Лица, ухаживающие за больными, должны быть очень осторожными при обращении с использованными иглами , чтобы предотвратить повреждение иглой и перекрестном инфицированию.
Уход за Вашей шприц-ручкой. • Не оставляйте шприц-ручку в автомобиле или в другом месте, где она может перегреться или переохладиться. • Не храните свою шприц-ручку при температуре свыше 30 ° C. • Защищайте свою шприц-ручку от попадания на нее пыли, грязи или воды. • не мойте свою шприц-ручку погружать ее в жидкость и не смазывайте ее. При необходимости ее можно очистить влажной тканью с мягким моющим средством. • Следите за тем, чтобы Ваша шприц-ручка не падала и не билась о твердую поверхность. Если она падала или Вы сомневаетесь в ее работе, присоедините новую иглу и проверьте ток лекарственного средства со шприц-ручки перед тем, как сделать инъекцию. • Не пытайтесь повторно наполнить шприц-ручку. Пустую шприц-ручку следует выбросить. • Не пытайтесь ремонтировать шприц-ручку или разбирать ее на части. |
Дети
Препарат не применяют в педиатрической практике. Опыта применения лекарственного средства Ксалтофай детям и подросткам в возрасте до 18 лет не существует.
Передозировка
Информация о передозировке лекарственного средства Ксалтофай ограничено.
Если пациент получает дозу лекарственного средства Ксалтофай, которая выше, чем нужно, у него может развиться гипогликемия:
- гипогликемию легкой степени тяжести можно лечить путем приема глюкозы или других средств, содержащих сахар. Поэтому пациентам рекомендуется всегда иметь при себе продукты, содержащие сахар;
- в случае возникновения эпизодов тяжелой гипогликемии, когда пациент не способен самостоятельно помочь себе, ему может помочь введение лицом, прошла соответствующий инструктаж, глюкагона (в дозе от 0,5 до 1 мг) внутримышечно или подкожно, или внутривенное введение глюкозы медицинским специалистом . Глюкозу также необходимо ввести внутривенно, если пациент в течение 10-15 минут не реагирует на введенный глюкагон. После восстановления сознания пациенту рекомендуется принять пероральные углеводы с целью профилактики рецидива гипогликемии.
Побочные эффекты
К участию в клинической программе разработки лекарственного средства Ксалтофай было привлечено примерно 1900 пациентов, принимавших Ксалтофай.
Частыми зарегистрированными побочными реакциями при лечении лекарственным средством Ксалтофай были гипогликемия и побочные реакции со стороны желудочно-кишечного тракта (см. Ниже «Описание отдельных побочных реакций»).
Ниже приведены побочные реакции, связанные с применением лекарственного средства Ксалтофай и приведенные по системам органов, а также по частоте случаев их возникновения. Категории частоты определены следующим образом: очень часто (≥ 1/10); часто (≥ 1/100 до <1/10); нечасто (≥ 1/1000 до <1/100); изредка (≥ 1/10000 до <1/1000); очень редко (<1/10000), неизвестно (невозможно оценить на основе имеющихся данных).
Таблица 5. Побочные реакции, зарегистрированные в ходе контролируемых исследований фазы 3.
Системы органов по классификации MedDRA | частота случаев | Побочная реакция на лекарственное средство |
Со стороны иммунной системы | Нечасто | крапивница |
Нечасто | гиперчувствительность | |
неизвестно | анафилактическая реакция | |
Со стороны обмена веществ и питания | очень часто | гипогликемия |
Часто | снижение аппетита | |
Нечасто | дегидратация | |
Со стороны желудочно-кишечного тракта | Часто | Тошнота, диарея, рвота, запор, диспепсия, гастрит, боль в животе, гастроэзофагеальная рефлюксная болезнь, вздутие живота |
Нечасто | Отрыжка, метеоризм | |
неизвестно | Панкреатит (включая некротический панкреатит) | |
Со стороны печени и желчевыводящих путей | Нечасто | желчнокаменная болезнь |
Нечасто | холецистит | |
Со стороны кожи и подкожных тканей | Нечасто | сыпь |
Нечасто | зуд | |
Нечасто | Приобретенная липодистрофия | |
Общие расстройства и нарушения в месте введения | Часто | Реакция в месте инъекции |
неизвестно | периферический отек | |
Показатели лабораторных исследований | Часто | Повышение уровня липазы |
Часто | Повышение уровня амилазы | |
Нечасто | Повышение частоты сердечных сокращений |
Описание отдельных побочных реакций.
Гипогликемия.
Гипогликемия может развиться, если доза лекарственного средства Ксалтофай выше, чем нужно. Тяжелая форма гипогликемии может привести к потере сознания и / или возникновения судорог и вызвать временное или постоянное нарушение функции головного мозга или даже смерть. Обычно симптомы гипогликемии возникают внезапно. Они могут включать холодный пот, бледную холодную кожу, усталость, нервозность или тремор, чувство тревоги, необычную усталость или слабость, спутанность сознания, трудности при концентрации внимания, сонливость, чрезмерный голод, нарушение зрения, головную боль, тошноту и сильное сердцебиение. Относительно частоты случаев гипогликемии см. раздел "Фармакологические" .
Аллергические реакции.
При применении лекарственного средства Ксалтофай сообщалось о случаях аллергических реакций, которые проявлялись в виде признаков и симптомов, таких как крапивница (в 0,3% пациентов, принимавших Ксалтофай), сыпь (0,7%), зуд (0,5 %) и / или отек лица (0,2%). В течение послерегистрационного периода применения лираглутид сообщалось о нескольких случаях анафилактических реакций, сопровождавшиеся дополнительными симптомами, такими как гипотензия, сердцебиение, одышка и отек. Анафилактические реакции могут быть угрожающими для жизни.
Побочные реакции со стороны желудочно-кишечного тракта.
Побочные реакции со стороны желудочно-кишечного тракта могут возникать более часто в начале лечения лекарственным средством Ксалтофай они, как правило, ослабевают в течение нескольких дней или недель при продолжении лечения. В 7,8% пациентов наблюдалась тошнота, которая у большинства из них была временной. Доля пациентов, сообщали о наличии тошноты в любое время в течение лечения, составила менее 4% в неделю. Диарея и рвота были зарегистрированы в 7,5% и 3,9% пациентов соответственно. Частота случаев тошноты и диареи была отнесена к категории «часто» при применении лекарственного средства Ксалтофай и "очень часто" - при применении лираглутид. Кроме того, в почти 3,6% пациентов, принимавших Ксалтофай, было зарегистрировано запор, диспепсия, гастрит, боль в животе, гастроэзофагеальной рефлюксной болезни, вздутие живота,
Реакции в месте инъекции.
В 2,6% пациентов, получавших Ксалтофай, наблюдались реакции в месте инъекции (включая гематому в месте инъекции, боль, кровоизлияние, эритема, узелки, отек, обесцвечивание, зуд, гиперемия и уплотнения в месте инъекции) . Как правило, эти реакции были легкой степени тяжести, временными и обычно исчезали при продолжении лечения.
Липодистрофия.
В месте инъекции может возникать липодистрофия (включая липогипертрофию, липоатрофии). Постоянная смена места инъекции в пределах одного участка введения лекарственного средства способствует уменьшению риска возникновения таких реакций.
Повышенная частота сердечных сокращений.
В ходе клинических исследований лекарственного средства Ксалтофай наблюдалось увеличение частоты сердечных сокращений на 2-3 удара в минуту по сравнению с показателем перед началом лечения. В ходе исследования "LEADER" по применению лираглутид (что является составной лекарственного средства Ксалтофай) не наблюдалось длительного клинически значимого влияния повышенной частоты сердечных сокращений на риск возникновения кардиоваскулярных явлений (см. Раздел «Фармакологические»).
Срок годности Ксалтофай
2 года.
Условия хранения Ксалтофай
К первому использования: хранить в холодильнике (при температуре 2-8 ° C). Хранить слишком близко от морозильной камеры. Не замораживать. Для защиты от воздействия солнечного света хранить шприц-ручку с надетым колпачком.
После первого использования: лекарственное средство можно хранить в течение 21 дня при температуре не выше 30 ° C или в холодильнике (при температуре 2-8 ° C). Лекарственное средство следует утилизировать через 21 день после первого использования. Не замораживать. Для защиты от воздействия солнечного света хранить шприц-ручку с надетым колпачком.
Хранить в недоступном для детей месте.
Несовместимость.
При добавлении веществ к лекарственному средству Ксалтофай может происходить распад его действующих веществ.
Лекарственное средство Ксалтофай нельзя добавлять в инфузионные растворы.
Это лекарственное средство нельзя смешивать с другими лекарственными средствами.
Упаковка
По 3 мл раствора в картридже (стекло типа I) с поршнем (с галобутилу) и пробкой (с галобутилу / полиизопрена), который содержится в предварительно заполненной многодозовых одноразовой шприц-ручке в картонной коробке. По 1, 3 или 5 предварительно наполненных шприц-ручек в картонной коробке
Категория отпуска
По рецепту.
Производитель
А / Т Ново Нордиск.
Местонахождение производителя
Ново Алле, Багсваерд, 2880, Дания.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Ксалтофай только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- АО Ново Нордиск
- http://www.drlz.com.ua - Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Ксалтофай |
| Производитель: | АО Ново Нордиск |
| Форма выпуска: | раствор для инъекций, 100 МЕ / мл и 3,6 мг / мл, 3 мл в картридже, который содержится в предварительно заполненной многодозовых одноразовой шприц-ручке, по 1, 3 или 5 предварительно заполненных шприц-ручек в картонной коробке |
| Регистрационное удостоверение: | UA/18253/01/01 |
| Дата начала: | 17.08.2020 |
| Дата окончания: | 17.08.2025 |
| МНН: | Insulin degludec and liraglutide |
| Условия отпуска: | по рецепту |
| Состав: | 1 мл 100 ЕД инсулина деглюдек * и 3,6 мг лираглутид *. / 1 предварительно заполнена шприц-ручка содержит 3 мл, что эквивалентно 300 ЕД инсулина деглюдек и 10,8 мг лираглутид // * Произведенные по технологии рекомбинантной ДНК в Saccharomyces cerevisiae |
| Фармакологическая группа: | Лекарственные средства, применяемые при сахарном диабете. Инсулины и аналоги длительного действия для инъекций. |
| Код АТХ: | A10AE56 |
| Заявитель: | А / Т Ново Нордиск |
| Страна заявителя: | Дания |
| Адрес заявителя: | Ново Алле, Багсваерд, 2880, Дания |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Да |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Комбинированный |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| A | Средства, влияющие на пищеварительную систему и метаболизм |
| A10 | Противодиабетические препараты |
| A10A | Инсулин и его аналоги |
| A10AE | Инсулины и аналоги для инъекций, длительного действия |
| A10AE56 | Инсулин деглюдек и лираглутид |