- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Теравас инструкция по применению
Официальная инструкция лекарственного препарата Теравас таблетки 250 мг, 500 мг. Описание и применение Teravas, аналоги и отзывы. Инструкция Теравас таблетки утвержденная компанией производителем.
Состав
действующее вещество:
1 таблетка содержит дивалпроекс натрия в пересчете на вальпроевой кислоты 250 мг или 500 мг.
Вспомогательные вещества:
таблетки пролонгированного действия по 250 мг целлюлоза микрокристаллическая лактоза моногидрат, гипромеллоза; гидроксиэтилцеллюлоза; кремния диоксид пленочная оболочка Opadry white OY- 58900 (состав оболочки: гипромеллоза, титана диоксид (Е 171), полиэтиленгликоль).
таблетки пролонгированного действия по 500 мг целлюлоза микрокристаллическая лактоза моногидрат, гипромеллоза; гидроксиэтилцеллюлоза; кремния диоксид пленочная оболочка Opadry grey 20А57646 (состав оболочки: гидроксипропилметилцеллюлоза, гипромеллоза, титана диоксид (Е 171), железа оксид черный (Е172), железа оксид желтый (Е172)).
Лекарственная форма
Таблетки пролонгированного действия.
Основные физико-химические свойства:
таблетки пролонгированного действия по 250 мг: белые или почти белые, округлой формы со скошенным краем, двояковыпуклые покрытые оболочкой таблетки с тиснением "R" на одной стороне и «533» - на другой;
таблетки пролонгированного действия по 500 мг серые, овальной формы со скошенным краем, двояковыпуклые покрытые оболочкой таблетки с тиснением "R" на одной стороне и «534» - на другой.
Фармакологическая группа
Противоэпилептические средства.
Код ATX N03A G01.
Фармакологические свойства
Фармакологические.
механизм действия
В желудочно-кишечном тракте дивалпроекс натрия распадается на ионы препарату. Механизмов, с помощью которых вальпроат осуществляет терапевтический эффект, не установлено. Есть предположение, что его активность при эпилепсии связана с повышением концентрации гамма аминобутировая кислоты (ГАБК) в мозге.
Взаимосвязь между концентрацией в плазме крови и клинической ответом не подтвержден. Одним из факторов является нелинейное, зависящее от концентрации связывание препарату с белками, которое влияет на клиренс препарата. Таким образом, мониторинг общего количества препарату в плазме крови не может обеспечить надежного показателя биологически активных видов препарату.
Поскольку связывание препарату с белками плазмы крови зависит от концентрации, свободная фракция увеличивается примерно от 10% при 40 мкг / мл до 18,5% при 130 мкг / мл. Более высокие, чем ожидалось свободные фракции оказываются у людей пожилого возраста, у пациентов с гиперлипидемией и у пациентов с заболеваниями печени и почек.
эпилепсия
Терапевтическим диапазоном при эпилепсии вообще считается 50-100 мкг / мл общего препарату, однако у некоторых пациентов удается достичь контроля над терапевтическим эффектом при более низкой или высокой концентрации в плазме крови.
маниакальный синдром
В плацебо-контролируемых клинических исследованиях острого маниакального синдрома у пациентов было достигнуто клинического ответа при остаточных концентрациях препарата в плазме крови в пределах от 85 до 125 мкг / мл.
Фармакокинетика.
Абсорбция / биодоступность
Биодоступность дивалпроекс натрия, таблетки пролонгированного действия в виде однократной дозы после приема пищи составляла примерно 90% относительно внутривенной инфузии.
При условии приема одинаковых общих суточных доз биодоступность дивалпроекс натрия, таблетки пролонгированного действия меньше, чем в дивалпроекс натрия, таблетки с модифицированным высвобождения. Прием дивалпроекс натрия, таблетки пролонгированного действия 1 раз в сутки натощак и после еды приводил к средней биодоступности 89% относительно аналогичного общей суточной дозы дивалпроекс натрия, таблетки с модифицированным высвобождением, предназначенного для двух-, трех- и четырехкратного приема в сутки. Среднее время достижения максимальной плазменной концентрации вальпроата (Сmах) после приема дивалпроекс натрия, таблетки пролонгированного действия составлял от 4 до 17 часов. После нескольких приемов дивалпроекс натрия, таблетки пролонгированного действия в режиме 1 раз в сутки колебания между максимальной и минимальной концентрациями препарату в плазме крови было на 10-20% ниже,
распределение
Н Связывание с белками
Связывание вальпроата с белками плазмы зависит от концентрации, а свободная фракция увеличивается примерно от 10% при концентрации 40 мкг / мл до 18,5% при 130 мкг / мл соответственно. Связывания белков с вальпроатом уменьшается у людей пожилого возраста, у пациентов с хроническими заболеваниями печени, у пациентов с нарушениями функции почек и при приеме других лекарственных средств (например, аспирина). И наоборот, вальпроат может вытеснять определенные лекарственные средства, которые связываются с белками (например, фенитоин, карбамазепин, варфарин и толбутамид).
Распределение в ЦНС
Концентрация вальпроата в спинномозговой жидкости (СМР) приближается к концентрации несвязанного препарату в плазме крови (примерно 10% от общей концентрации).
метаболизм
Вальпроат почти полностью метаболизируется в печени. У взрослых пациентов при монотерапии 30-50% введенной дозы обнаруживается в моче в виде глюкуронидного конъюгата. Другой основной путь метаболизма - митохондриальное р-окисления, на которое обычно приходится более 40% дозы. Как правило, менее 15-20% дозы выводится с помощью других окислительных механизмов. Менее 3% введенной дозы выводится в неизмененном виде с мочой.
Соотношение между дозой и общей концентрацией вальпроата является нелинейным; концентрация не увеличивается пропорционально дозе, а, скорее, увеличивается в меньшей степени благодаря насыщенному связыванию с белками плазмы крови. Кинетика незв связанного лекарственного средства является линейной.
Выведение
Средний клиренс и объем распределения общей дозы вальпроата составляет 0,56 л / ч / 1,73 м2 и 11 л / 1,73 м2 соответственно. Средний клиренс и объем распределения свободной фракции вальпроата составляет 4,6 л / ч / 1,73 м2 и 92 л / 1,73 м. Средний конечный период полувыведения препарату в режиме монотерапии составлял от 9 до 16 часов после приема от 250 до 1000 мг.
Приведенные данные применяются, прежде всего, для пациентов, не принимающих лекарственные средства, влияющие на ферментные системы печеночного метаболизма. Например, у пациентов, принимающих ферментно-стимулирующие протиепилентични лекарственные средства (карбамазепин, фенитоин и фенобарбитал), наблюдается более быстрое выведение вальпроата. В связи с такими изменениями в процессе клиренса препарату целесообразно усиление мониторинга концентраций в плазме крови каждый раз, когда к лечению добавляются или отменяются другие противоэпилептические препараты.
Отдельные группы пациентов.
Пациенты пожилого возраста
Способность пациентов пожилого возраста (возрастной диапазон: 68-89 лет) по элиминации препарату снижается по сравнению со взрослыми пациентами младшего возраста (возрастной диапазон: 22-26 лет). Собственный клиренс уменьшается на 39%; свободная фракция увеличивается на 44%. Таким образом, у пациентов пожилого возраста целесообразно уменьшение первой дозы препарата.
Гендерный влияние
Никаких различий показателей «площадь поверхности тела относительно несвязанного клиренса» у мужчин и женщин (4,8 ± 0,17 и 4,7 ± 0,07 л / ч на 1,73 м2 соответственно) не обнаружено.
Влияние расовой принадлежности
Влияние расы на кинетику препарату не изучались.
заболевания печени
Заболевания печени ухудшают способность организма выводить вальпроат. По данным одного исследования клиренс свободного вальпроата был снижен на 50% у пациентов с циррозом печени и на 16% у 4 пациентов острым гепатитом по сравнению со здоровыми добровольцами. В данном исследовании период полувыведения препарату вырос с 12 до 18 часов. Болезни печени также связаны со снижением концентрации альбумина и увеличением несвязанных фракций препарату (увеличение в 2-2,6 раза). Соответственно, мониторинг общих концентраций может быть ошибочным, поскольку у пациентов с заболеваниями печени свободные концентрации могут быть существенно повышенными, тогда как общая концентрация может оказаться в пределах нормы.
заболевания почек
У пациентов с почечной недостаточностью (клиренс креатинина <10 мл / мин) наблюдалось незначительное снижение (27%) в клиренсе несвязанного препарату; однако гемодиализ обычно снижает концентрацию вальпроата примерно на 20%. Поэтому в случае пациентов с почечной недостаточной нет необходимости в коррекции дозы. Связывания белков у таких пациентов существенно снижается; таким образом, мониторинг общей концентрации может быть ложным.
Клинические характеристики
Теравас Показания
маниакальный синдром
Лечение острых маниакальных и смешанных эпизодов, связанных с биполярным расстройством, с психотическими проявлениями или без них.
эпилепсия
Монотерапия и вспомогательная терапия при лечении взрослых пациентов и детей от 10 лет при сложных парциальных припадках, возникающих отдельно или в связи с другими видами судом. Лекарственное средство также показан в качестве монотерапии и вспомогательной терапии при лечении простых и сложных абсансов у взрослых пациентов и детей от 10 лет и старше, а также в качестве вспомогательной терапии при лечении взрослых пациентов и детей от 10 лет и старше с различными типами приступов , которые включают абсансы.
мигрень
Профилактика мигренеподобной головной боли.
Противопоказания
Заболевания печени или значительная дисфункция печени.
Повышенная чувствительность к натриевой соли вальпроевой кислоты или любого другого компонента лекарственного средства (см. Раздел «Состав»).
Пациенты с известными нарушениями цикла образования мочевины.
Для профилактики мигренеподобной головной боли у беременных женщин или женщин, планирующих беременность (см. Раздел «Применение в период беременности или кормления грудью»).
Женщинам репродуктивного возраста, не пользуются эффективными средствами контрацепции, за исключением случаев, когда такой препарат является важным для контроля состояния их здоровья.
Известны митохондриальные расстройства, вызванные мутациями в митохондриальной ДНК гамма полимеразы (POLG: например, синдром Альперса-Гуттенлохера).
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Влияние одновременно введенных лекарственных средств на клиренс вальпроата
Лекарственные средства, влияющие на уровень экспрессии печеночных ферментов, в частности те, что повышают уровни глюкуронозилтрансферазы (например, ритонавир), могут. увеличить клиренс вальпроата. Например, фенитоин, карбамазепин и фенобарбитал (или примидон) аджта удваивать клиренс вальпроата. Таким образом, у пациентов, получающих лечение в режиме монотерапии, как правило, длительный период полураспада и более высокие концентрации по сравнению с пациентами, которые получают, политерапию противоэпилептическими лекарственными средствами.
Наоборот, можно ожидать, что препараты, которые являются ингибиторами изоферментов цитохрома Р450, например, антидепрессанты, мало влияют на клиренс вальпроата, поскольку микросомальное опосредованное окисления цитохрома Р450 является относительно незначительным вторичным метаболическим путем по сравнению с глюкуронидация и бета-окислением.
Через эти изменения в процессе клиренса препарату целесообразно увеличение мониторинга концентрации вальпроата и сопутствующих лекарственных средств, когда назначают или отменяют фермент-индуцирующих лекарственные средства.
Следующий список содержит информацию о возможном влиянии нескольких общепринятых лекарственных средств на фармакокинетику вальпроата. Этот список не является исчерпывающим и не может быть таковым, так как постоянно появляются сообщения о новых взаимодействия.
аспирин
Исследование, включавшее одновременное применение аспирина в жаропонижающих дозах (11-16 мг / кт) с вальпроатом у детей, выявило снижение связывания с белками и ингибирование метаболизма вальпроата. Свободная фракция препарату увеличивалась в 4 раза при сопутствующего приема ацетилсалициловой кислоты по сравнению с приемом одного только препарату. Путь В- окисления, состоящий из 2-Е-вальпроевой кислоты, С-ОН-вальпроевой кислоты и 3 кетовальпроевои кислоты, снижался с 25% от общего количества выведенных метаболитов в случае наличия одного препарату до 8,3% при наличии аспирина . Независимо от того, известно о зафиксированном в ходе данного исследования взаимодействие у взрослых, следует соблюдать осторожность при одновременном применении вальпроата и аспирина.
Антибиотики группы карбапенемов
Клинически значимое снижение концентрации вальпроевой кислоты в сыворотке крови наблюдается у пациентов, принимающих антибиотики группы карбапенемов (например, эртапенем, имипенем, меропенем и др.), Что может привести к потере контроля над приступами. Механизм данного взаимодействия не исследован. Следует часто контролировать концентрацию вальпроевой кислоты в сыворотке крови после начала приема карбапенему. В случае существенного снижения концентрации вальпроевой кислоты в плазме крови или ухудшении контроля над приступами следует рассмотреть альтернативную антибактериальное или противосудорожное терапию.
Естрогеновмисни гормональные контрацептивы
Естрогеновмисни гормональные контрацептивы могут увеличивать клиренс вальпроата, что может привести к уменьшению концентрации вальпроата и, возможно, увеличение частоты приступов. Врачи, которые назначают лечение, должны контролировать концентрацию вальпроата в сыворотке крови и клинический ответ при назначении или отмене лекарственных средств, содержащих эстроген.
Фелбамат
В исследовании, включавшем одновременное применение фельбамата с вальпроатом в дозе 1200 мг / сут у пациентов с эпилепсией, было выявлено увеличение среднего показателя максимальной концентрации вальпроата на 35% (от 86 до 115 мкг / мл) по сравнению с вальпроатом в режиме монотерапии. Увеличение дозы фельбамата до 2400 мг / сут збшьшило средний показатель максимальной концентрации вальпроата до 133 мкг / мл (ще на 16%). Может возникнуть необходимость в снижении дозы вальпроата при начале приема фельбамата.
рифампицин
В результате исследования, которое включало применение однократной дозы вальпроата (7 мг / кг) через 36 часов после 5 суток суточного дозирования рифампина (600 мг), было выявлено увеличение клиренса при пероральном приеме вальпроата на 40%. При одновременном применении с рифампином может потребоваться коррекция дозы вальпроата.
Лекарственные средства, с которыми или нет взаимодействия ", или возможна клинически важна взаимодействие
Антациды
В результате исследования, которое предусматривало одновременное применение 500 мг вальпроата с широко используемыми антацидами (Маалокс, Тризогель и Титралак - 160 милиграмеквивалент дозы), не было обнаружено никакого влияния на степень поглощения препарату.
хлорпромазин
В результате исследования, которое включало применение 100-300 мг / сут хлорпромазина пациентам с шизофренией, которые уже получали вальпроат (200 мг дважды в сутки), было обнаружено увеличение на 15% уровня вальпроата в плазме крови.
галоперидол
В результате исследования, которое включало применение 6-10 мг / сут галоперидола пациентам с шизофренией, которые уже получали вальпроат (200 мг дважды в сутки), не было отмечено никаких значимых изменений в общих уровнях препарату в плазме крови.
Циметидин и ранитидин
Циметидин и ранитидин не влияют на клиренс вальпроата.
Влияние вальпроата на другие лекарственные средства
Выявлено, что вальпроат является слабым ингибитором некоторых изоферментов цитохрома Р450, эпоксидной гидразы и глюкуронозилтрансферазы.
Ниже указана информация о потенциальном воздействии одновременного применения вальпроата на фармакокинетику или фармакодинамику нескольких широко применяемых лекарственных средств. Этот список не является исчерпывающим, так как постоянно появляются сообщения о новых взаимодействия. Препараты, в отношении которых наблюдается потенциально важно взаимодействие
Амитриптилин / Нортриптилин
В результате приема одной дозы амитриптилина 50 мг перорально при применении вальпроата (500 мг дважды в сутки) установлено снижение на 21% клиренса амитриптилина в плазме крови и уменьшение суммарного клиренса нортриптилином на 34%. Получено редкие постмаркетингови сообщение об одновременном применении вальпроата и амитриптилина, что приводило к повышению уровня амитрипталину. Одновременное применение вальпроата и амитриптилина редко было связано с токсическим воздействием. При одновременном приеме вальпроата с амитриптилином следует проводить мониторинг уровня амитриптилина. Также нужно учитывать снижение дозы амитриптилина / нортриптилином при применении вальпроата.
Карбамазепин / карбамазепин-10,11-эпоксид
Уровни карбамазепину в сыворотке крови снижались на 17%, а карбамазепину-10,11-эпоксида увеличивались на 45% при одновременном применении вальпроата и карбамазепину пациентам с эпилепсией.
Клоназепам
Одновременное применение вальпроата и клоназепама может привести абсансной-статус у пациентов с приступами абсансных типа в анамнезе.
диазепам
Вальпроат вытесняет диазепам из его участков связывания в альбумине плазмы крови и подавляет его метаболизм. Одновременное применение вальпроата (1500 мг в сутки) здоровым добровольцам увеличивало свободную фракцию диазепама (10 мг) на 90%. При наличии препарату клиренс плазмы и объем распределения свободного диазепама снижался на 25% и 20% соответственно. Период полувыведения диазепама оставался неизменным после добавления препарату.
этосуксимида
Вальпроат подавляет метаболизм Этосуксимид. Применение однократной дозы препарата этосуксимида в дозе 500 мг с вальпроатом (от 800 до 1600 мг в сутки) здоровым добровольцам сопровождалось увеличением периода полураспада этосуксимида на 25% и уменьшением его общего клиренса на 15% по сравнению с этосуксимида в режиме монотерапии. В случае пациентов, получающих вальпроат и этосуксимида, особенно вместе с другими антиконвульсантами, следует следить за изменениями концентрации обоих препаратов в сыворотке крови.
Ламотриджин
В ходе исследования стационарного типа с участием здоровых добровольцев период полувыведения ламотриджина увеличивался с 26 до 70 часов при одновременном применении вальпроата (увеличение на 165%). В случае одновременного применения вальпроата дозу ламотриджина следует уменьшать. Сообщалось о серьезных кожных реакций (синдром Стивенса-Джонсона и токсический эпидермальный некролиз) при одновременном применении ламотриджина и вальпроата. Подробно о дозу ламотриджина при одновременном применении вальпроата смотри в Инструкции по медицинскому применению ламотриджина.
Фенобарбитал
Установлено, что вальпроат угнетает метаболизм фенобарбитала. Одновременное применение вальпроата (250 мг дважды в сутки в течение 14 дней) с фенобарбиталом здоровым добровольцам приводило к увеличению периода полувыведения на 50% и снижение клиренса фенобарбитала в плазме крови на С% (однократный прием 60 мг). Фракция дозы фенобарбитала, что выделялась в неизмененном виде, увеличивалась на 50% при применении вальпроата.
Имеющиеся данные о серьезном угнетение ЦНС с или без повышения плазменных концентраций барбитурата или вальпроата. Следует тщательно следить за проявлениями неврологической токсичности у всех пациентов, которые одновременно получают терапию барбитуратов. По возможности следует определить плазменную концентрацию барбитурата и в случае необходимости - уменьшить дозу барбитуратов.
Примидон, что метаболизируется до барбитурата, может иметь подобную взаимодействие с вальпроатом.
фенитоин
Вальпроат вытесняет фенитоин из его участков связывания в альбумине плазмы крови и подавляет его метаболизм. Одновременный прием вальпроата (400 мг три раза в сутки) с фенитоином (250 мг) здоровыми добровольцами был ассоциирован с увеличением свободной фракции фенитоина на 60%. Общий клиренс и очевидный объем распределения фенитоина увеличивался на 30% при наличии препарату. Клиренс и прогнозируемый объем распределения свободного фенитоина уменьшался на 25%.
У пациентов с эпилепсией были сообщения о эпилептические припадки, возникающие при сочетании вальпроата и фенитоина. Дозировка фенитоина следует регулировать в соответствии с клинической ситуации.
Пропофол
Одновременное применение вальпроата и пропофола может привести к увеличению уровня пропофола в крови. При одновременном применении вальпроата следует уменьшить дозу пропофола. Обеспечить тщательный мониторинг пациентов на случай проявления признаков повышенной седативного действия или кардиореспираторной недостаточности.
Руфинамид
По результатам популяционного фармакокинетического анализа, вальпроат уменьшал клиренс руфинамиду. Концентрации руфинамиду увеличивались на <16% - 70% в зависимости от концентрации вальпроата (с более высоким ростом у детей, получавших лечение высокими дозами вальпроата или с повышенными концентрациями препарату в плазме крови). Перед назначением вальпроата пациентам, у которых предварительно достигнуто стабильное состояние на фоне приема руфинамиду, следует начинать лечение вальпроатом низкими дозами и титровать до клинически эффективной дозы. Подобным образом следует начинать лечение у пациентов, принимающих вальпроат, с дозы руфинамиду ниже 10 мг / кг в сутки (дети) или 400 мг в сутки (взрослые).
толбутамид
По результатам экспериментов in vitro, несвязанная фракция толбутамиду была увеличена с 20% до 50% при добавлении к образцам плазмы крови, взятых у пациентов, получавших лечение вальпроатом. Клиническая релевантность данного замещения неизвестна ..
Варфарин
В исследовании in vitro вальпроат увеличивал несвязанную фракцию варфарина до 32,6%. Терапевтическая релевантность данного явления неизвестна; однако следует проводить мониторинг тестов свертывания крови при назначении терапии вальпроатом у пациентов, принимающих антикоагулянты.
Зидовудин
У шести пациентов с серопозитивных ВИЧ-инфекцией, после приема вальпроата (250 или 500 мг каждые 24 часа) клиренс зидовудина (100 мг каждые 24 часа) снижался на 38%; период полувыведения зидовудина не менялся.
Лекарственные средства, с которыми или нет взаимодействия, или возможна клинически важна взаимодействие
Ацетаминофен
Вальпроат не влиял на любые фармакокинетические параметры ацетаминофена при одновременном назначении пациентам с эпилепсией.
Клозапин
При одновременном применении вальпроата с клозапином в психотических пациентов взаимодействие не установлено.
литий
Одновременное назначение препарату (500 мг дважды в сутки) и лития карбоната (300 мг три раза в сутки) здоровым добровольцам мужского пола не влияло на стационарную кинетику лития.
Лоразепам
Одновременное применение вальпроата (500 мг дважды в сутки) и лоразепама (1 мг дважды в сутки) здоровым добровольцам мужского пола сопровождалось уменьшением клиренса лоразепама на 17%.
Оланзапин
При одновременном применении оланзапина с вальпроатом нет необходимости в коррекции дозы оланзапина. Одновременное назначение препарату (500 мг дважды в сутки) и оланзапина (5 мг) здоровым добровольцам приводило К 15% снижение Стах и 35% снижение площади под фармакокинетической кривой (AUC) оланзапина.
Пероральные стероидные контрацептивы
В результате однократного приема этинилэстрадиола (50 мкг) / левоноргестрела (250 мкг) шести женщинам, которые получали лечение вальпроатом (200 мг дважды в сутки) в течение 2 месяцев не обнаружено ни одной фармакокинетического взаимодействия.
Топирамат
Одновременное применение вальпроата и топирамата было ассоциировано с гипераммониемией с и без энцефалопатии. Одновременное назначение топирамата и вальпроата также было связано с гипотермией у пациентов, получавших любой из этих лекарственных средств в режиме монотерапии. Целесообразно контролировать уровень аммония в крови пациентов, у которых сообщали о начале гипотермии.
Особенности применения
гепатотоксичность
Общая информация о гепатотоксичности
Печеночная недостаточность, возникает у пациентов, получающих лечение вальпроатом, может приводить к летальному исходу. Такие случаи обычно случались в течение первых 6 месяцев лечения. Серьезной или летальной гепатотоксичности могут предшествовать такие неспецифические симптомы как недомогание, слабость, летаргия, отек лица, анорексия и рвота. У больных эпилепсией, также может наблюдаться потеря контроля над приступами. Следует обеспечивать тщательный надзор за пациентами о возникновении таких симптомов. Печеночные пробы (плазма) следует проводить перед началом терапии и через несколько интервалов позже, особенно в течение первых 6 месяцев лечения. Однако медицинские работники не должны в полной мере опираться на биохимические показатели плазмы крови, поскольку эти тесты могут иметь отклонения от нормы во всех случаях.
Следует соблюдать осторожность при применении препаратов препарату пациентам с болезнями печени в анамнезе. Пациенты, принимающие несколько антиконвульсантов, дети, те, кто страдает от тяжелых судорожных приступов, сопровождающихся умственной отсталостью и те, кто страдает органическим заболеванием головного мозга, относятся к группе риска.
Опыт показывает, что у детей до 2 лет значительно повышен риск развития гепатотоксичности, которая может приводить к летальному исходу, особенно у тех, кто имеет вышеуказанные состояния. Когда дивалпроекс натрия, таблетки пролонгированного действия назначать такой группе пациентов, его следует применять с максимальной осторожностью и в режиме монотерапии. Следует взвешивать преимущества терапии в отношении рисков. Практика применения в последовательно старших возрастных группах пациентов с эпилепсией свидетельствует о том, что частота летальной гепатотоксичности с возрастом значительно уменьшается.
Пациенты с известным или потенциальным митохондриальным заболеванием
Дивалпроекс натрия, таблетки пролонгированного действия противопоказан пациентам с известными митохондриальными нарушениями, вызванных мутациями POLG, и детям до 2 лет, у которых подозревают митохондриальные расстройства. Острую печеночную недостаточность и связанную с нарушением работы печени летальность, что индуцированные вальпроатом, было зарегистрировано у пациентов с наследственными нейрометаболической синдромами, вызванными мутациями в митохондриальной ДНК гамма-полимеразы (POLG, например, синдром Альперса-Хуттенлохера) с большей частотой проявления сравнению с пациентами без таких синдромов. Большинство зарегистрированных случаев печеночной недостаточности у пациентов с этими синдромами обнаружено у детей и подростков.
Следует предполагать наличие расстройств, связанных с POLG, у пациентов с подобными заболеваниями в семейном анамнезе или признаками расстройств, подобных связанных с POLG, включающих, но не ограничены энцефалопатией невыясненной этиологии, рефрактерной эпилепсией (фокальной, миоклонические) , проявлениями эпилептического статуса, задержкой развития, психомоторной деградацией, аксонных сенсомоторной нейропатии, миопатические мозжечковой атаксией, офтальмоплегия или осложненной мигренью с затылочной аурой. Диагностику мутаций POLG следует проводить согласно действующих клинических рекомендаций по диагностической оценки таких расстройств. Мутации А467Т и W748S оказываются примерно в 2 / з пациентов с аутосомно-рецессивным расстройствами, связанными с POLG.
У пациентов в возрасте от 2 лет, у которых подозревают наследственное митохондриальное заболевание, дивалпроекс натрия, таблетки пролонгированного действия следует применять только тогда, когда другие антиконвульсанта оказались неэффективными. При применении дивалпроекс натрия, таблетки пролонгированного действия в группе пациентов более старшего возраста следует обеспечивать тщательное наблюдение по развитию острого повреждения печени путем регулярного клинического обследования и мониторинга печеночных проб плазмы крови.
Следует немедленно прекратить прием лекарственного средства при подозреваемой или очевидной дисфункции печени. В некоторых случаях наблюдалось прогрессирование дисфункции печени, несмотря на прекращение приема препарата.
Врожденные пороки развития
Вальпроаты могут вызвать вредное воздействие на плод при применении беременной женщиной .. Данные реестра беременных показывают, что прием вальпроата матерью может вызвать дефекты нервной трубки и другие структурные патологии (например, черепно-лицевые дефекты, аномалии сердечно-сосудистой системы, гипоспадии, деформации конечностей). Частота врожденных пороков развития у детей, рожденных матерями, которые принимали вальпроаты, примерно в 4 раза превышает частоту среди детей, рожденных женщинами с эпилепсией, которые получали другие противосудорожные препараты в режиме монотерапии. Доказательства позволяют предположить, что прием фолиевой кислоты до зачатия и в течение 1 триместра беременности снижает риск развития врожденных дефектов нервной трубки в общей популяции.
Снижение уровня IQ после внутриилньоутробного влияния
Вальпроаты могут вызвать снижение показателей IQ (коэффициент интеллекта), как следствие влияния на внутриутробное развитие. Опубликованные эпидемиологические исследования показали, что дети, которые подверглись воздействию вальпроата во внутриутробном состоянии, имеют более низкие когнитивные показатели, чем дети, которые подвергались внутриутробному воздействию других противоэпилептических лекарственных средств или не претерпели никакого влияния противоэпилептических препаратов. Согласно данным исследований было установлено, что дети, которые испытали влияние терапии вальпроатом в пренатальном периоде, имеют более низкие показатели IQ в возрасте 6 лет по сравнению с детьми, которые испытали влияние терапии другими противоэпилептическими лекарственными средствами в режиме монотерапии ': ламотриджин, карбамазепин и фснитоин. Неизвестно, когда в период беременности наступают когнитивные эффекты у детей под действием вальгироату.
Хотя все имеющиеся исследования имеют методологические ограничения, весомость доказательств подтверждает вывод о том, что внутриутробная действие вальпроата может привести к снижению уровня интеллекта у детей.
Вальпроат противопоказан в период беременности женщинам, которые принимают препарат для профилактики мигренозной головной боли. Женщинам с эпилепсией или биполярным расстройством, которые уже беременны или планируют беременность, не следует принимать вальпроат, при условии если иное лечение не позволяет достичь адекватного контроля над симптомами или неприемлемо по другим причинам. У таких женщин преимущества лечения вальпроатом в период беременности могут преобладать риски.
Применение женщинам репродуктивного возраста
В связи с риском снижения уровня интеллекта и основных врожденных пороков развития плода (в т.ч. дефектов нервной трубки), которые могут возникнуть в самом начале беременности, нельзя назначать вальпроат женщинам репродуктивного возраста, за исключением случаев, когда такое лекарственное средство является важным для контроля состояния их здоровья. Это особенно важно, если рассматривать назначение препарату при состоянии, обычно не связан с постоянной травматизацией или угрозой летального исхода (например, мигрень). При применении вальпроата женщины имеют использовать эффективные средства контрацепции.
Женщинам репродуктивного возраста необходимы регулярные консультации по относительных рисков и преимуществ применения вальпроата в период беременности. Это особенно важно для женщин, планирующих беременность, и для девушек в начале полового созревания. Следует рассмотреть альтернативные варианты лечения для таких пациенток.
Для предотвращения серьезных нападений не надо внезапно прекращать прием вальпроата, поскольку это может спровоцировать эпилептический статус, что приведет к гипоксии организма матери и плода и угрозы жизни.
Имеющиеся данные позволяют предположить, что прием фолиевой кислоты до зачатия и в течение первого триместра беременности снижает риск развития врожденных дефектов нервной трубки в общей популяции. Неизвестно, уменьшается риск дефектов нервной трубки или снижение уровня интеллекта у младенцев, рожденных женщинами, которые получают вальпроат, при условии приема фолиевой кислоты. Пациентам, принимающим вальпроат, следует рекомендовать принимать диетические добавки фолиевой кислоты как до зачатия, так и в период беременности.
Панкреатит
Выявлены случаи опасного для жизни панкреатита как у детей, так и у взрослых, принимающих вальпроат. Некоторые случаи были описаны как геморрагические с быстрым прогрессированием от начальных симптомов до наступления летального исхода. Некоторые случаи возникали сразу после начала приема препарата, а некоторые после нескольких лет применения. Частота на основе сообщенных случаев превышает ожидаемую в общей популяции. Сообщалось о случаях рецидива панкреатита после повторного назначения препарату. Следует предупреждать пациентов и тех, кто за ними доглиядае. что боль в животе, тошнота, рвота и / или анорексия могут быть симптомами панкреатита, которые вимагают ь скорой медицинской оценки. Если установлен диагноз «панкреатит», прием дивалпроекс натрия, таблетки пролонгированного действия обычно прекращают в установленном порядке.
Нарушение цикла образования мочевины Дивалпроекс натрия, таблетки пролонгированного действия противопоказан пациентам с известными нарушениями цикла образования мочевины (орнитиновый цикл). Сообщалось о гиперамониемичну энцефалопатию, иногда с летальным исходом, зарегистрированную после начала терапии вальпроатом у пациентов с нарушениями цикла мочевины, группу необычных генетических аномалий, особенно дефицит орнитин-транскарбамилазы. Перед началом лечения дивалпроекс натрием, таблетки, пролонгированного действия следует рассмотреть оценку орнитинового цикла в следующих случаях:
1) пациенты с энцефалопатией невстаповленого генеза или комой в анамнезе, энцефалопатией, связанной с содержанием белка, энцефалопатией, связанной с беременностью или послеродовой энцефалопатией, умственной отсталостью невстаповленого генеза, с анамнезом повышенного содержания аммония или глютамина в плазме крови
2) пациенты с циклическим рвотой и летаргией, эпизодической сильной раздражительностью, атаксией, низким содержанием азота мочевины в плазме крови или с непереносимостью белков;
3) пациенты с семейным анамнезом расстройств цикла образования мочевины или семейным анамнезом невыясненной детской летальности (особенно у представителей мужского пола)
4) пациенты с другими признаками или симптомами нарушения орнитинового цикла. Пациентам, у которых развиваются симптомы гиперамониемичних энцефалопатии неустановленного генеза во время терапии вальпроатом, следует обеспечить немедленное лечение (в том числе прекращения приема вальпроата) и проверить наличие основных расстройств цикла мочевины.
Суицидальное поведение и мысли
Противоэпилептические лекарственные средства, в том числе дивалпроекс натрия, таблетки пролонгированного действия, увеличивают риск возникновения суицидальных мыслей или поведения у пациентов, принимающих такие лекарственные средства по поводу любых показаний. Состояние пациентов, получающих лечение любым противоэпилептическим лекарственным средством по поводу любого показания, должно быть под контролем относительно появления или прогрессирования депрессии, суицидальных мыслей или поведения и / или каких-либо необычных изменений настроения или поведения.
Повышенный риск возникновения суицидальных мыслей или поведения при приеме противоэпилептического лекарственного средства наблюдали через одну неделю после начала применения противоэпилептических препаратов, который сохранялся в течение длительности исследуемого лечения. Поскольку продолжительность большинства исследований, включенных в анализ, не превышала 24 недели, нельзя оценить риск возникновения суицидальных мыслей или поведения за пределами 24 недель.
Относительный риск суицидальных мыслей или поведения был большим в клинических испытаниях при эпилепсии, чем в клинических исследованиях при психиатрических и других состояниях, но абсолютные различия риска были подобными при эпилепсии и психиатрических показаниях.
При рассмотрении назначения дивалпроекс натрия, таблетки пролонгированного действия или любого другого противоэпилептического лекарственного средства следует взвешивать риск возникновения суицидальных мыслей и поведения с риском болезни без лечения. Эпилепсия и многие другие заболевания, при которых назначают противоэпилептические лекарственные средства, сами по себе связаны с заболеваемостью и летальностью, а также повышенным риском возникновения суицидальных мыслей и поведения. В случае возникновения суицидальных мыслей и поведения во время терапии врачу следует учитывать, может возникновения этих симптомов у любого конкретного пациента быть связанным с болезнью, лечится.
Пациенты, ухаживающий персонал и семьи должны быть проинформированы о том, что противоэпилептические лекарственные средства увеличивают риск возникновения суицидальных мыслей и поведения. Они должны быть уведомлены о необходимости быть готовыми к возникновению или ухудшение признаков и симптомов депрессии, каких-либо необычных изменений настроения или поведения или возникновения суицидальных мыслей, поведения или мыслей о нанесении себе травмы. Следует немедленно сообщать медицинских работников о подозрительном поведении.
Кровотечения и другие гемопоэтические расстройства
Вальпроат связан с дозозависимым тромбоцитопенией. В клиническом исследовании препарату в режиме монотерапии при эпилепсии у пациентов, получавших дозы в среднем около 50 мг / кг / сут, по крайней мере один показатель тромбоцитов составлял ≤75х10 9 / л. Примерно половина этих пациентов прекратили лечение, при этом уровень тромбоцитов вернулся к норме. В остальных пациентов количество тромбоцитов нормализовалась в процессе продленного лечения. В данном исследовании вероятность тромбоцитопении существенно возросла при общей концентрации вальпроата ≥110 мкг / мл (женщины) или ≥135 мкг / мл (мужчины). Терапевтическую преимущество, что может сопровождать более высокие дозы следует взвешивать с вероятностью возникновения большего количества побочных реакций. Применение вальпроата также связано с уменьшением других клеточных линий и миелодисплазией.
Несмотря на сообщения о цитопении, ингибирование вторичной фазы агрегации тромбоцитов и аномальные показатели коагуляции (например, низкий уровень фибриногена, нарушение коэффициента коагуляции, приобретенная болезнь фон Виллебранда), перед началом терапии рекомендуют проводить полный анализ крови и периодически проверять показатели коагуляции. Пациентам, получающим дивалпроекс натрия, таблетки пролонгированного действия, рекомендуется проведение обязательного контроля показателей крови и коагуляционных тестов перед плановым хирургическим вмешательством и в период беременности. Наличие кровотечения, гематом или нарушения гемостаза / коагуляции является показанием к снижению дозы или отмены терапии.
гипераммониемия
Сообщалось о гипераммониемия, связанную с терапией вальпроатом; она может существовать независимо от нормальных функциональных печеночных проб. В случае пациентов с проявлениями сонливости и рвоты неустановленной этиологии или изменениями психического состояния следует рассмотреть гиперамониемичну энцефалопатией и определить уровень аммония. Гипераммониемия также следует рассматривать у пациентов с гипотермией. При повышении уровня аммония применения в.альпроату следует прекратить. Необходимо принять соответствующие меры для лечения гипераммониемии. Такие пациенты должны пройти обследование по основным расстройств цикла мочевины.
Бессимптомные повышения аммония являются более распространенными и при наличии нуждаются в тщательном мониторинге уровня аммония в плазме крови. Если повышение сохраняется, следует рассмотреть прекращения приема вальпроата.
Гипераммониемия и енцефалонатия, связанные с одновременным применением топирамата
Одновременное применение топирамата и вальпроата связано с гипераммониемией с или без энцефалопатии у пациентов, получавших любой из этих лекарственных средств в режиме монотерапии. Клинические симптомы гиперамониемичнои энцефалопатии часто включают резкие изменения уровня сознания и / или когнитивной функции по летаргией или рвотой. Гипотермия также может быть проявлением гипераммониемии. В большинстве случаев симптомы и признаки уменьшаются при отмене любого препарата. Такая побочная реакция не связана с фармакокинетическим взаимодействием. Пациенты с врожденными нарушениями метаболизма или снижением активности митохондрий печени могут иметь повышенный риск возникновения гипераммониемии с или без энцефалопатии. Хотя это не исследовано, взаимодействие топирамата с вальпроатом может обострять имеющиеся нарушения или «демаскировать» расстройство у лиц со склонностью к таким нарушениям. В случае пациентов с летаргией и рвотой неустановленной этиологии или изменениями психического состояния целесообразно рассмотреть гиперамониемичну энцефалопатией и определить уровень аммония.
гипотермия
Сообщалось о гипотермию, которая определяется как нежелательное снижение температуры тела до <35 ° С (95 ° F), в связи с терапией вальпроатом как в сочетании с гипераммониемией, так и в случае его отсутствия. Такая побочная реакция также может наблюдаться у пациентов при одновременном приеме топирамата с вальпроатом после начала лечения топираматом или после увеличения суточной дозы топирамата. Следует рассмотреть прекращения приема вальпроата при наличии гипотермии, что может проявляться в виде различных клинических нарушений, в том числе вялости, спутанности сознания, коме и значительных изменений в других основных системах органов, таких как сердечно-сосудистая и дыхательная системы. Клиническое ведение и оценка должны включать определение уровня аммония в крови.
Реакция на лекарственное средство с эозинофилией и системными проявлениями (DRESS / Полиорганные реакции гиперчувствительности
Реакцию на лекарственное средство с эозинофилией и системными проявлениями (DRESS), также известную как полиорганная гиперчувствительность, зарегистрировано у пациентов, принимавших вальпроат. DRESS может иметь летальный исход или представлять опасность для жизни. DRESS, как правило, хотя не обязательно, проявляется в виде лихорадки, сыпи и / или лимфаденопатии в сочетании с поражением другой системы органов, например с гепатитом, нефритом, гематологическими отклонениями, миокардитом или миозит, который иногда напоминает острую вирусную инфекцию. Часто выявляется эозинофилия. Поскольку это расстройство имеет различные проявления, могут быть поражены другие системы органов, не указанные в данном разделе. Важно отметить, что ранние проявления повышенной 'чувствительности, такие как лихорадка или лимфаденопатия, могут иметь место даже при отсутствии сыпи. Следует немедленно провести осмотр больного при наличии таких признаков или симптомов. Прием препарату следует прекратить, а в случае невозможности определения альтернативной этиологии признаков или симптомов не восстанавливать его прием.
Взаимодействие с карбапснемовимы антибиотиками
Карбапенемы антибиотики (например, эртапенем, имипенем, меропенем, список не полный) могут снижать концентрацию вальпроата в сыворотке крови к субтерапевтической уровней, что приведет к потере контроля над приступами. Следует часто проверять концентрацию вальпроата в сыворотке крови после начала лечения Карбапенемы. В случае существенного снижения концентрации вальпроата в плазме крови или ухудшении контроля над приступами следует рассмотреть альтернативную антибактериальное или противосудорожное терапию.
Сонливость у пациентов пожилого возраста
В двойном слепом многоцентровом испытании препарату у пациентов пожилого возраста с деменцией (средний возраст = 83 лет), дозу была увеличена на 125 мг / сут до целевой дозы 20 мг / кг / сут. Значительно большая часть пациентов, принимавших вальпроат, имела сонливость по сравнению с плацебо, и, хотя это не было статистически значимым, также наблюдали большую часть пациентов с дегидратацией. Прекращение приема препарата вследствие сонливости также были значительно выше, чем в группе плацебо. У некоторых пациентов с сонливостью (примерно половина) наблюдалось снижение потребления пищи и уменьшение массы тела. У пациентов, имевших вышеуказанные признаки, установлена тенденция к более низкой начальной концентрации альбумина, снижение клиренса препарату и более высокого содержания азота мочевины в плазме крови. У пациентов пожилого возраста дозу следует увеличивать медленнее и регулярно контролировать потребление жидкости и пищи, обезвоживания, сонливость и другие побочные реакции. У пациентов со снижением потребления пищи или жидкости и в случае чрезмерной сонливости следует рассмотреть снижение дозы или отмены вальпроата.
Мониторинг концентрации лекарственного средства в плазме крови
Поскольку вальпроат может взаимодействовать с одновременно назначаемыми лекарственными средствами, способными к индукции ферментов, рекомендуется проводить периодические определения концентрации вальпроата и сопутствующих лекарственных средств в плазме крови в течение раннего периода терапии.
Влияние на содержание кетонов и исследование функции щитовидной железы
Вальпроат частично выводится с мочой в виде кето-метаболита, что может привести к ложной интерпретации теста на содержание кетонов в моче.
Сообщалось об изменениях результатов исследования функции щитовидной железы вследствие приема вальпроата. Клиническое значение этого факта неизвестно.
Влияние на репликацию BИЛ и ЦМВ
Согласно некоторым исследованиям in vitro, вальпроат может стимулировать репликацию ВИЧ и ЦМВ при определенных экспериментальных условиях. Клинические последствия неизвестны. Кроме того, релевантность данных выводов in Vitro неопределенной для пациентов, которые получают максимально супрессивную антиретровирусную терапию. Однако эти данные следует учитывать при интерпретации результатов регулярного мониторинга вирусной нагрузки у ВИЧ-положительных пациентов, принимающих вальпроат, или во время клинического наблюдения за пациентами с ЦМВ.
Остатки лекарственного средства в каловых массах
Редко сообщали об остатках лекарственного средства в кале. У некоторых пациентов были анатомические (в т.ч. илеостомия или колостомия) или функциональные заболевания желудочно-кишечного тракта с сокращенными интервалами желудочно-кишечного транзита. В некоторых отчетах вопрос остатков лекарственного средства имело место в контексте диареи. Рекомендуется контролировать уровень вальпроата в плазме крови пациентов, у которых обнаружены остатки лекарственного средства в каловых массах, и следить за клиническим состоянием пациентов. При наличии клинических показаний можно рассмотреть альтернативное лечение.
Пациенты с недостаточностью лактазы, галактоземии или синдромом нарушения всасывания глюкозы / галактозы
Данное лекарственное средство содержит в своем составе лактозу. Не принимать пациентам с недостаточностью лактазы, галактоземии или синдромом нарушения всасывания глюкозы / галактозы.
Применение дивалпроекс натрия у детей изучали в клинических исследованиях. В двух двойных слепых плацебо-контролируемых исследованиях по оценке эффективности дивалпроексу пролонгированного действия для показаний «мания» и «мигрень» эффективности не установлено ни при лечении мигрени, ни при лечении мании. Наиболее распространенными побочными реакциями, связанными с лекарственным средством (сообщено о> 5% и вдвое больше у показателя плацебо), зарегистрированными в контролируемом педиатрическом исследовании мании, были тошнота, боль в верхней части живота, сонливость, повышение уровня аммония, гастрит и сыпь . Остальные испытаний касались долгосрочных исследований безопасности. В этих клинических испытаниях безопасность и переносимость дивалпроекс натрия у детей показали, что они сравнению с показателями у взрослых.
Пациенты пожилого возраста
Одного пациента старше 65 лет не были привлечены к участию в клинических испытаниях с маниакального синдрома, связанного с биполярными расстройствами.
В имеющихся исследованиях у пациентов пожилого возраста с деменцией обнаружено сонливость, связанную с применением лекарственного средства, частота возникновения которой была несколько выше у пациентов с дегидратацией. Потребность в прекращении приема препарата в связи с сонливостью возникала чаще, чем в группе плацебо. У таких пациентов нужно уменьшить начальную дозу, а в случае чрезмерной сонливости следует рассмотреть снижение дозы или отмены препарата.
Существует недостаточно информации для определения безопасности и эффективности вальпроата для профилактики мигрени у пациентов старше 65 лет.
Способность пациентов пожилого возраста (возрастной диапазон: 68-89 лет) по элиминации препарату снижается по сравнению со взрослыми пациентами младшего возраста (возрастной диапазон: 22-26 лет).
Применение в период беременности или кормления грудью
В связи с риском снижения уровня интеллекта, дефектов нервной трубки и других основных врожденных пороков развития плода, которые могут возникнуть очень рано период беременности, не следует назначать вальпроат женщинам репродуктивного возраста, за исключением случаев, когда терапевтическая польза от применения препарата превышает риски (по степени риска для плода).
Беременность категория D по эпилепсии и маниакальных эпизодов, связанных с биполярным расстройством.
Беременность категория X по профилактике мигренеподобной головной боли.
Резюме о риске для развития плода
Независимо от влияния лекарственного средства начальная частота врожденных дефектов каждой беременности составляет около 3%, риск прерывания беременности - около 15%, или риск возникновения других неблагоприятных последствий. Применение вальпроата женщиной во время беременности по любым показаниям повышает риск возникновения врожденных пороков развития, в частности дефектов нервной трубки, а также аномалий, включающих другие системы организма (например, черепно-лицевые дефекты, сердечно-сосудистые пороки, гипоспадию, аномалии конечностей). Наибольший риск развития основных структурных аномалий в I триместре; однако другие серьезные дефекты развития могут иметь место при использовании вальпроата в течение всего периода беременности. Частота врожденных пороков развития у детей, рожденных матерями с эпилепсией, которые принимали вальпроат в период беременности,
Имеющиеся данные свидетельствуют, что дети, которые подверглись воздействию вальпроата во внутриутробном состоянии, имеют более низкие когнитивные показатели, чем дети, которые подвергались внутриутробному воздействию как другой протиепилептичногьо лекарственного средства, так и при отсутствии противоэпилептических лекарственных средств.
Обсервационные исследования показали, что влияние препаратов вальпроата в период беременности повышает риск расстройств аутистического спектра. Согласно исследованию риск для детей, родившихся от матерей, принимавших препараты вальпроата в период беременности, в 2,9 раза превышал риск (95% доверительный интервал [СИ]: 1,7-4,9) развития расстройств аутистического спектра по сравнению с детьми, рожденными матерями, не пидхвалися влияния вальпроата в период беременности. Абсолютный риск расстройств аутистического спектра составлял 4,4% у детей в результате воздействия вальпроата и 1,5% у детей, которые не подвергались воздействию вальпроата. Поскольку исследования было обсервационным по своему дизайну, выводы о причинно-следственная связь между внутриутробным воздействием вальпроата и повышенным риском расстройства аутистического спектра нельзя считать окончательным.
Согласно имеющимся данным исследований на животных установлено, что у потомства с пренатальным влиянием вальпроата пороки развития подобные тех же показателей с участием людей, и продемонстрировано нейроповединкови нарушения.
Клинические аспекты
• Дефекты нервной трубки - это врожденная аномалия, тесно связана с приемом вальпроата беременной. Риск spina bifida (незаращение дужек позвонков) после внутриутробного воздействия вальпроата в целом оценивается как 1-2% по сравнению с оценкой общего популяционного риска spina bifida, что составляет примерно 0,06-0,07% (6-7 случаев на 10000 новорожденных).
• Вальпроат может привести к снижению коэффициента интеллекта (IQ) у детей, чьим матерям назначали вальпроат в период беременности.
• Из-за риска уменьшения коэффициента интеллекта (IQ), дефектов нервной трубки и других побочных эффектов для плода, которые могут возникнуть на ранних сроках беременности, рекомендуется следующее:
- Вальпроат не следует назначать женщине репродуктивного возраста, если это лекарственное средство не является необходимым для лечения состояния ее здоровья. Это особенно важно, если рассматривать назначение препарату при состоянии, обычно не связан с постоянной травматизацией или риском летального исхода (например, мигрень)
- Вальпроат противопоказан в период беременности женщинам, которые применяют препарат для профилактики мигренеподобной головной боли
- Вальпроат не следует применять для лечения женщин с эпилепсией или биполярным расстройством, которые уже беременны или планируют забеременеть, если другие методы лечения не обеспечили надлежащего контроля над симптомами или были по другим причинам неприемлемыми. У таких женщин преимущества лечения вальпроатом в период беременности могут все еще преобладать риски. При лечении беременной или женщины репродуктивного возраста нужно внимательно рассмотреть потенциальные риски, преимущества лечения, а также обеспечить надлежащее консультирование.
• Для предотвращения серьезных нападений женщинам с эпилепсией не следует внезапно прекращать прием вальпроата, поскольку это может спровоцировать возникновение эпилептического статуса, что повлечет гипоксию организма матери и плода и угрозе жизни. Даже незначительные судороги могут представлять опасность для эмбриона или плода развивается. Однако прекращения приема препарата. Может рассматриваться до и в период беременности в отдельных случаях, если тяжесть и частота возникновения заболевания не представляет серьезной угрозы для пациента.
• Беременным женщинам, которые принимают вальпроат, следует предложить имеющуюся пренатальную диагностику для выявления дефектов нервной трубки и других пороков развития.
• Доказательные данные позволяют предположить, что прием фолиевой кислоты до зачатия и в течение первого триместра беременности снижает риск развития врожденных дефектов нервной трубки в общей популяции. Неизвестно, уменьшается риск дефектов нервной трубки или снижение уровня интеллекта у младенцев, рожденных женщинами, которые получают вальпроат, при условии приема фолиевой кислоты. Пациентам, принимающим вальпроат, нужно постоянно рекомендовать диетические добавки фолиевой кислоты как до зачатия, так и в период беременности.
• У беременных, принимающих вальпроат, могут развиться нарушения свертывания крови, в т.ч. тромбоцитопения, гипофибриногенемия и / или уменьшения других коагуляционных факторов, который может привести к геморрагических осложнений у новорожденного, включая летальный исход. Если вальпроат применять в период беременности, следует тщательно контролировать параметры свертывания крови у матери. В случае выявления нарушений со свертыванием в организме матери такие параметры также необходимо контролировать у новорожденного.
• У пациентов, принимающих вальпроат, может развиться печеночная недостаточность. После применения вальпроата в период беременности также сообщали о случаях печеночной
недостаточности с летальным исходом у новорожденных, подвергшихся внутриутробному воздействию вальпроата.
• Сообщалось о гипогликемии у новорожденных, чьи матери принимали вальпроат в период беременности.
Имеющиеся исследования показали, что дети, которые подверглись воздействию вальпроата во внутриутробном периоде, имеют более низкие когнитивные показатели, чем дети, которые подвергались внутриутробному воздействию как другого противоэпилептического лекарственного средства, так и при отсутствии противоэпилептического лекарственного средства. Поскольку женщины в имеющихся исследованиях получали противоэпилептические лекарственные средства в период беременности, нельзя было оценить, риск снижения уровня интеллекта связан с определенным периодом времени в период беременности.
Хотя все имеющиеся исследования имеют методологические ограничения, весомость доказательств подтверждает взаимосвязь внутриутробной действия вальпроата с последующими неблагоприятными последствиями для когнитивного развития.
Имеющиеся данные о случаях летальной печеночной недостаточности у детей, чьи матери принимали вальпроат в период беременности.
Период кормления грудью
Вальпроат проникает в грудное молоко. Следует соблюдать осторожность при назначении вальпроата женщине, которая кормит грудью.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Лекарственное средство влияет на способность управлять транспортными средствами или другими механизмами в связи с возможным развитием побочных реакций. Препарат может замедлять мышления и двигательные навыки.
Способ применения Теравас и дозы
Теравас является лекарственным средством с пролонгированным высвобождением, предназначенной для приема 1 раз в сутки. Таблетки следует глотать целиком, не разламывать и не разжевывая.
маниакальный синдром
Рекомендованная начальная доза составляет 25 мг / кг / сутки 1 раз в сутки. Следует увеличивать дозу как можно скорее для достижения низкой терапевтической дозы, которая дает желаемый клинический эффект или желаемый диапазон концентрации в плазме крови. Максимальная рекомендованная доза составляет 60 мг / кг / сут.
эпилепсия
Поскольку дозировка лекарственного средства титруется в сторону повышения, это может иметь влияние на концентрацию клоназепама, диазепама, этосуксимида, ламотриджина, толбутамиду, фенобарбитала, карбамазепина и / или фенитоина (см. Раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
Сложные парциальные приступы
Для взрослых и детей старше 10 лет.
Монотерапия (начальная терапия)
Систематических исследований дивалпроекс натрия, таблетки пролонгированного действия в качестве начальной терапии не проводили. Пациентам следует начать лечение с 10 до 15 мг / кг / сут. Для достижения оптимально клинического ответа дозу нужно увеличивать на 5-10 мг / кг / нед. Как правило, оптимальная клинический ответ достигается при суточных дозах ниже 60 мг / кг / сут. Если удовлетворительная клиническая ответ не достигнута, необходимо проверить уровень концентрации препарата в плазме крови для определения того, находится ли он в общепринятом терапевтическом диапазоне (от 50 до 100 мкг / мл). Рекомендации по безопасности использования вальпроата в дозах, превышающих 60 мг / кг / сут, отсутствуют. Вероятность тромбоцитопении значительно увеличивается при общей концентрации вальпроата в сыворотке крови (определяется перед применением первой суточной дозы) более 110 мкг / мл у женщин и 135 мкг / мл у мужчин. Преимущество усиленного контроля над приступами при более высоких дозах следует сравнивать с возможностью большего количества побочных реакций.
Переход на монотерапии
Пациенты должны начинать лечение с 10 до 15 мг / кг / сут. Для достижения оптимального клинического ответа дозу нужно увеличивать на 5-10 мг / кг / нед. Как правило, оптимальная клинический ответ достигается при суточных дозах ниже 60 мг / кг / сут. Если удовлетворительная клиническая ответ не достигнута, необходимо проверить уровень вальпроата в плазме для определения того, находится ли он в общепринятом терапевтическом диапазоне (от 50 до 100 мкг / мл). Рекомендации по безопасности использования вальпроата в дозах, превышающих 60 мг / кг / сут, отсутствуют.
Доза сопутствующего противоэпилептического лекарственного средства может обычно уменьшаться примерно на 25% каждые 2 недели. Такое уменьшение можно начинать в начале применения дивалпроекс натрия, таблетки пролонгированного действия или позже, через 1-2 недели в случае признаков возникновения приступов при условии уменьшения дозы. Скорость и продолжительность прекращения приема сопутствующего противоэпилептического лекарственного средства могут быть очень разными; во время этого периода нужно обеспечить тщательное наблюдение за пациентами по увеличению частоты приступов.
Вспомогательная терапия
Теравас можно добавлять в схему лечения пациента в дозе от 10 до 15 мг / кг / сут. Для достижения оптимального клинического ответа дозу нужно увеличивать на 5-10 мг / кг / нед. Как правило, оптимальная клинический ответ достигается при суточных дозах ниже 60 мг / кг / сут. Если удовлетворительная клиническая ответ не достигнута, необходимо проверить уровень концентрации препарата в плазме крови для определения того, находится ли он в общепринятом терапевтическом диапазоне (от 50 до 100 мкг / мл). Рекомендации по безопасности использования вальпроата в дозах, превышающих 60 мг / кг / сут, отсутствуют.
В исследовании вспомогательной терапии при сложных парциальных припадках, в котором пациенты получали либо карбамазепин, или фенитоин дополнительно к препарату, никакой необходимости в корректировке дозы карбамазепина или фенитоина не было. Однако, поскольку вальпроат может взаимодействовать с этими или другими противоэпилептическими лекарственными средствами при одновременном применении, а также с другими лекарственными средствами, рекомендуется проводить периодические определения концентрации в плазме крови сопутствующих противоэпилептических лекарственных средств в течение раннего курса терапии.
Простой и сложный абсансной
Рекомендованная начальная доза составляет 15 мг / кг / сут, которую с интервалом в одну неделю следует увеличивать по 5-10 мг / кг / сут, пока не будет достигнут контроль над приступами или побочные реакции не будут препятствовать дальнейшему увеличению. Максимальная рекомендованная доза составляет 60 мг / кг / сут.
Полную корреляцию между суточной дозой, концентрацией в сыворотке крови и терапевтическим ч. В эффектом не установлено. Однако для большинства пациентов с абсансами терапевтической считается концентрация вальпроата в плазме крови от 50 до 100 мкг / мл. Состояние некоторых пациентов следует контролировать при более низкой или высокой концентрации в сыворотке крови.
Поскольку доза дивалпроекс натрия, таблетки пролонгированного действия титруется в сторону повышения, это может иметь влияние на концентрацию фенобарбитала и / или фенитоина в крови.
Нельзя внезапно прекращать прием противоэпилептических лекарственных средств пациентам, принимающим препарат с целью предупреждения серьезных нападений, в результате большой вероятности провоцирующего эпилептического статуса с сопровождающей гипоксией и угрозой для жизни.
мигрень
Теравас показан для профилактики мигренозной головной боли.
Рекомендованная начальная доза составляет 500 мг 1 раз в сутки в течение 1 недели, после чего увеличивается до 1000 мг 1 раз в сутки. Несмотря на отсутствие оценки другого дозирования дивалпроекс натрия, таблетки пролонгированного действия при мигренях кроме 1000 мг 1 раз в сутки, диапазон эффективных доз дивалпроекс натрия, таблетки с модифицированным высвобождением у этих пациентов составляет 500-1000 мг в сутки. Как и в случае с другими препаратами препарату, выбор дозы дивалпроекс натрия, таблетки пролонгированного действия должен быть индивидуальным для каждого пациента. Может возникнуть необходимость в коррекции дозы. Если пациент нуждается корректировок меньших доз, чем те, что доступны в случае с дивалпроекс натрием, таблетки пролонгированного действия, вместо этого нужно применять дивалпроекс натрия, таблетках с модифицированным высвобождением.
Переход от дивалпроекс натрия, таблетки с модифицированным высвобождением к дивалпроекс натрия, таблетки пролонгированного действия
Взрослым и детям> 10 лет с эпилепсией, которые ранее получали дивалпроекс натрия, таблетки с модифицированным высвобождением, следует принимать дивалпроекс натрия, таблетки пролонгированного действия 1 раз в сутки в дозе в 8-20% выше, чем общая суточная доза дивалпроекс натрия, таблетки с модифицированным высвобождением (таблица 1). Для пациентов, которые получают общую суточную дозу дивалпроекс натрия, таблетки с модифицированным высвобождением, которые нельзя напрямую перевести на дивалпроекс натрия, таблетки пролонгированного действия, может быть принято решение увеличить общую суточную дозу лекарственного средства дивалпроекс натрия, таблетки с модифицированным высвобождением, которую получает пациент , до следующей большей дозы, прежде чем перейти на соответствующую общую суточную дозу дивалпроекс натрия, таблетки пролонгированного действия.
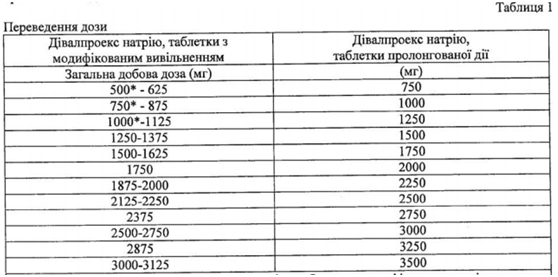
* Общие данные суточной дозы дивалпроекс натрия, таблетки с модифицированным высвобождением нельзя непосредственно перевести на общую суточную дозу дивалпроекс натрия, таблетки пролонгированного действия, выше на 8-20%, поскольку необходима концентрация дозирования дивалпроекс натрия, таблетки пролонгированного действия отсутствует. Может быть принято решение увеличить общую суточную дозу дивалпроекс натрия, таблетки с модифицированным высвобождением, которую получает пациент, до следующей большей дозы, прежде чем перейти на соответствующую общую суточную цозу дивалпроекс натрия, таблетки пролонгированного действия.
Не существует достаточно данных для рекомендации коэффициента перехода для пациентов с дозами дивалпроекс натрия, таблетки с модифицированным высвобождением более 3,125 мг / сут. Концентрация Cmin препарату в плазме крови для дивалпроекс натрия, таблетки пролонгированного действия в среднем эквивалентна дивалпроекс натрия, таблетки с модифицированным высвобождением, но может меняться у пациентов после перевода. Если удовлетворительного клинического ответа не достигнуто, следует проверить уровни концентрации препарата в плазме крови для определения того, находятся ли они в общепринятом терапевтическом диапазоне (от 50 до 100 мкг / мл).
Общие рекомендации дозирования
Дозировка для пожилых людей
В результате уменьшения клиренса несвязанного препарату и, возможно, большей чувствительности к сонливости у людей пожилого возраста, начальную дозу для таких пациентов следует уменьшить. Достижения начальных доз ниже 250 мг у людей пожилого возраста возможно только при условии приема дивалпроекс натрия, таблетки с модифицированным высвобождением. Дозировка следует увеличивать медленнее и регулярно контролировать потребление жидкости и пищи, обезвоживания, сонливость и другие побочные реакции. У пациентов со сниженным потреблением пищи или жидкости и в случае чрезмерной сонливости следует рассмотреть снижение дозы или отмены вальпроата.
Конечная терапевтическая доза должна достигаться на основе как переносимости, так и клинического ответа.
Дозозависимы побочные реакции
Частота побочных эффектов (особенно повышение уровня ферментов печени и тромбоцитопения) может зависеть от дозы. Вероятность тромбоцитопении существенно возрастает при общей концентрации вальпроата ≥110 мкг / мл у женщин или ≥135 мкг / мл у мужчин. Преимущество усиленного контроля над приступами при более высоких дозах следует сравнивать с возможностью возникновения большего количества побочных реакций.
Раздражение желудочно-кишечного тракта
Пациентам с раздражением желудочно-кишечного тракта лучше принимать препарат с пищей или медленно увеличивать дозы с начального низкого уровня.
Соблюдение режима дозирования
Пациенты должны быть проинформированы о важности приема лекарственного средства Теравас ежедневно в соответствии с назначением. Если пациент пропускает прием дозы лекарственного средства, его следует принять как можно скорее, даже если почти наступило время для следующей дозы. Если пропускается прием дозы, пациент не должен удваивать следующую дозу.
Дозирование для пациентов, принимающих руфинамид
Пациентам, у которых стабилизировалось состояние на фоне приема руфинамиду перед назначением вальпроата, следует начинать лечение вальпроатом при низкой дозе и титровать до клинически эффективной дозы.
Дети
Можно применять детям в возрасте от 10 лет и старше в качестве монотерапии и вспомогательной терапии для лечения составляющая частичных эпилептических приступов в качестве монотерапии и адъювантной терапии при лечении простых и сложных малых эпилептических приступов (абсансов) в качестве дополнительной терапии при различных типах припадков, включая абсансы (см. раздел «Способ применения и дозы»).
Передозировка
Передозировка вальпроатом может привести к сонливости, блокады сердца, глубокой комы и гипсрнатриемии 'Сообщалось о летальных последствиях; однако некоторые пациенты выздоравливали с уровнями препарату до 2120 мкг / мл.
В случаях передозировки фракция лекарственного средства, связанного с белком, высока. Гемодиализ или гемодиализ в сочетании с гемоперфузию может обеспечивать значительное вывода лекарственного средства. Польза от промывки желудка или рвота отличается в зависимости от времени после приема препарата. Следует принять общих поддерживающих мер с особым вниманием к поддержания адекватного выведения мочи.
Как сообщалось, налоксон обеспечивает обратимый характер антидепрессантов ЦНС при передозировке препарату. Поскольку налоксон может теоретически также изменить противоэпилептические эффекты вальпроата, его следует применять с осторожностью у пациентов с эпилепсией.
Побочные эффекты
В данном разделе описаны следующие серьезные побочные реакции:
- печеночная недостаточность
- врожденные пороки развития;
- снижение уровня коэффициента интеллекта (IQ) в результате воздействия во внутриутробном периоде;
— панкреатит;
- гиперамониемична енцефалопатил;
- суицидальное поведение и суицидальные мышления;
- кровотечения и другие гемопоэтические расстройства;
- гипотермия;
- реакция на лекарственное средство с эозинофилией и системными проявлениями (DRESS) / Полиорганные реакции гиперчувствительности;
- сонливость у пациентов пожилого возраста.
Поскольку клинические исследования проводят в очень разнообразных условиях, частоту побочных реакций, наблюдаемых в ходе клинических исследований лекарственного средства, нельзя напрямую сравнивать с показателями частоты в клинических исследованиях другого лекарственного средства, и это может не отражать частоту, наблюдается на практике.
маниакальный синдром
Частота случаев, возникающих при лечении, была установлена на основании комбинированных имеющихся данных плацебо-контролируемых исследований дивалпроекс натрия, таблетки пролонгированного действия при лечении маниакальных эпизодов, связанных с биполярным расстройством. Побочные реакции в> 5% пациентов, получавших дивалпроекс натрия, таблетки пролонгированного действия, в ходе исследований острого маниакального синдрома: сонливость, диспепсия, тошнота, рвота, диарея, головокружение, боль, боль в животе, случайная травма, астения, фарингит.
Следующие дополнительные побочные реакции зарегистрировано в более чем 1% пациентов, получавших дивалпроекс натрия, таблетки пролонгированного действия в ходе контролируемых клинических исследований.
Общие расстройства: боли в спине, озноб, озноб с лихорадкой, повышение уровня лекарственного средства, гриппоподобный синдром, инфекция, грибковая инфекция, ригидность мышц шеи.
Со стороны сердечно-сосудистой системы: аритмия, артериальная гипертензия, гипотензия, ортостатическая гипотензия.
Со стороны пищеварительной системы: запор ,, сухость во рту, дисфагия, недержание каловых масс, метеоризм, гастроэнтерит, глоссит, кровоточивость десен, язвы ротовой полости.
Со стороны системы крови и лимфатической системы: анемия, увеличение времени кровотечения, экхимозы, лейкопения.
Со стороны метаболизма и питания: гипопротеинемия, периферические отеки.
Со стороны костно-мышечной системы: артроз, миалгия.
Со стороны нервной системы: нарушение походки, тревожность, кататоническая реакция, дизартрия, галлюцинации, гипертония, гипокинезия, психоз, усиление рефлексов, нарушение сна, отсроченная дискинезия, тремор.
Со стороны дыхательной системы, органов грудной клетки и средостения: икота, ринит.
Со стороны кожи и подкожной клетчатки: дискоидная красная волчанка, нодозная эритема, фурункулез, макулопапульний сыпь, зуд, сыпь, себорея, потоотделение, везикульозно- буллезная сыпь.
Со стороны органов зрения, органов чувств: конъюнктивит, сухость глаз, нарушение зрения, боли в области глаз, фотофобия, дисгевзия.
Со стороны мочевыделительной системы: цистит, инфекция мочевыводящих путей, нарушения менструального цикла, вагинит.
эпилепсия
На основании имеющегося исследования адъювантной терапии для лечения сложных парциальных припадков дивалпроекс натрием, таблетки с модифицированным высвобождением, как правило, хорошо переносится, причем большинство побочных реакций имели легкий и средней степени тяжести. Непереносимость была основной причиной прекращения лечения у пациентов, принимавших дивалпроекс натрия, таблетки с модифицированным высвобождением, по сравнению с пациентами из группы плацебо.
Побочные реакции, зарегистрированные в> 5% пациентов, получавших вальпроат в ходе плацебо контролируемого исследования адъювантной терапии сложных парциальных приступов.
Общие расстройства: головная боль, астения, лихорадка.
Со стороны пищеварительного тракта: тошнота, рвота, боль в животе, диарея, анорексия, диспепсия, запоре.
Со стороны нервной системы: сонливость, тремор, головокружение, диплопия, амблиопия / нечеткость зрения, атаксия, нистагм, эмоциональная лабильность, патологическое мышление, амнезия.
Со стороны дыхательной системы, органов грудной клетки и средостения: гриппоподобный синдром, инфекция, бронхит, ринит.
Прочее: алопеция, потеря массы тела.
Поскольку пациенты также принимали другие противоэпилептические лекарственные средства, в большинстве случаев невозможно определить, могут ли следующие побочные реакции касаться только дивалпроекс натрия, таблетки с модифицированным высвобождением или комбинации дивалпроекс натрия, таблетки с модифицированным высвобождением с другими противоэпилептическими лекарственными средствами.
Побочные реакции, зарегистрированные в> 5% пациентов из группы приема высоких доз в контролируемом исследовании препарату для монотерапии сложных парциальных приступов.
Общие расстройства: астения.
Со стороны пищеварительного тракта: тошнота, диарея, рвота, боль в животе, анорексия, диспепсия.
Со стороны системы крови и лимфатической системы: тромбоцитопения, экхимозы.
Со стороны метаболизма и питания: увеличение массы тела, периферические отеки.
Со стороны нервной системы: тремор, сонливость, головокружение, бессонница, нервозность, амнезия, нистагм, депрессия.
Со стороны дыхательной системы, органов грудной клетки и средостения: инфекция, фарингит, одышка.
Со стороны кожи и подкожной клетчатки: алопеция.
Со стороны органа зрения: амблиопия / нечеткость зрения.
Со стороны органов слуха: шум в ушах.
Поскольку пациенты также принимали другие противоэпилептические лекарственные средства во время первой части исследования, во многих случаях невозможно определить, могут ли следующие побочные реакции касаться только дивалпроекс натрия, таблетки с модифицированным высвобождением или комбинации вальпроата с другими противоэпилептическими лекарственными средствами.
Следующие дополнительные побочные реакции отмечались более чем в 1%, но менее чем в 5% в пациентов, получавших вальпроат в контролируемых исследованиях сложных парциальных приступов.
Общие нарушения: боль в спине, боль в грудной клетке, недомогание.
Со стороны сердечно-сосудистой системы: тахикардия, артериальная гипертензия, тахикардия.
Со стороны пищеварительного тракта: увеличение аппетита, метеоризм, гематемезис, отрыжка, панкреатит, периодентальний абсцесс.
Со стороны системы крови и лимфатической системы: петехии.
Со стороны метаболизма и питания: повышение уровней ACT, АЛТ.
Со стороны костно-мышечной системы: миалгия, резкие сокращения мышц, артралгия, судороги в ногах, миастения.
Со стороны нервной системы: тревожность, спутанность сознания, нарушение походки, парестезии, гипертония, потеря координации, аномальные мысли, расстройство личности.
Со стороны дыхательной системы, органов грудной клетки и средостения: синусит, увеличение кашля, пневмония, носовое кровотечение.
Со стороны кожи и подкожной клетчатки: сыпь, зуд, сухость кожи.
Со стороны органов зрения, органов чувств, органов слуха и равновесия: дисгевзия, расстройства зрения, глухота, средний отит.
Со стороны мочевыделительной системы: недержание мочи, вагинит, дисменорея, аменорея, частое мочеиспускание.
мигрень
Исходя из имеющихся данных двух плацебо-контролируемых клинических исследований и долговременного продолжения, вальпроат, как правило, хорошо переносится. Большинство побочных реакций оценивались как легкие или средние по степени тяжести. Из пациентов, которые принимали вальпроат в исследованиях, 17% прекратили прием вследствие непереносимости. С учетом длительного дополнительного исследования, побочными реакциями, были алопеция (6%), тошнота и / или рвота (5%), увеличение массы тела (2%), тремор (2%), сонливость (1%), повышенный уровень ACT и / или АЛТ (1%), депрессия (1%).
Побочные реакции, сообщенные> 5% пациентов, принимавших дивалпроекс натрия, таблетки пролонгированного действия в ходе исследования мигрени с большей частотой, чем пациенты, которые принимали плацебо.
Со стороны пищеварительного тракта: тошнота, диспепсия, диарея, рвота, боль в животе.
Со стороны нервной системы: сонливость.
Прочее: инфекция.
Следующие дополнительные побочные эффекты отмечались в более чем 1%, но не более 5% пациентов, получавших дивалпроекс натрия, таблетки пролонгированного действия, и с большей частотой, чем плацебо, в ходе клинического исследования по профилактике мигрени.
Общие расстройства: случайная травма, инфекция.
Со стороны пищеварительного тракта: увеличение аппетита, заболевания зубов.
Со стороны метаболизма и питания: отек, увеличение массы тела.
Со стороны нервной системы: нарушение походки, головокружение, гипертония, бессонница, нервозность, тремор, вертиго.
Со стороны дыхательной системы, органов грудной клетки и средостения: фарингит, ринит.
Со стороны кожи и подкожной клетчатки: сыпь.
Со стороны органов слуха и равновесия: шум в ушах.
Ниже приведены те побочные реакции, о которых сообщали пациенты в ходе плацебо контролируемых исследований, где уровень заболеваемости в группе вальпроата превышал более 5% по сравнению с группой плацебо.
Со стороны пищеварительного тракта: тошнота, диспепсия, диарея, рвота, боль в животе, повышение аппетита.
Со стороны нервной системы: астения, сонливость, головокружение, тремор.
Другое: увеличение массы тела, боль в спине, алопеция.
Следующие дополнительные побочные реакции зарегистрировано в более чем 1% пациентов, но не более чем у 5% пациентов, получавших вальпроат в ходе контролируемых клинических исследований.
Общие нарушения: боль в груди.
Со стороны сердечно-сосудистой системы: вазодилатация.
Со стороны пищеварительного тракта: запор, сухость во рту, метеоризм и стоматит.
Со стороны системы крови и лимфатической системные: экхимозы.
Со стороны метаболизма и питания: периферический отек.
Со стороны опорно-двигательного аппарата: судороги в икрах.
Со стороны нервной системы: аномальные мысли, спутанность сознания, парестезии, расстройства речи и нарушения мышления.
Со стороны дыхательной системы, органов грудной клетки и средостения: одышка и синусит.
Со стороны кожи и подкожной клетчатки: зуд.
Со стороны мочеполовой системы: метроррагия.
Следующие побочные реакции были обнаружены во время послерегистрационного применения дивалпроекс натрия, таблетки с модифицированным высвобождением. Поскольку об этих реакции сообщают добровольно по популяции неопределенного размера, не всегда возможно достоверно оценить их частоту или установить причинно-следственную связь с воздействием препаратов.
Со стороны кожи и подкожной клетчатки: изменения текстуры волос, изменения цвета волос, фотосенсибилизация, мультиформная эритема, токсический эпидермальный некролиз, болезни ногтя и ногтевого ложа, синдром Стивенса-Джонсона.
Со стороны психики: эмоциональное огорчение, психоз, агрессия, психомоторная гиперактивность, враждебность, нарушение внимания, нарушение способности к обучению и ухудшение поведения.
Со стороны нервной системы: было несколько сообщений о острое или подострое уменьшение когнитивной способности и изменения поведения (апатия или раздражительность) с псевдоатрофии мозга при визуализации, связанной с лечением вальпроатом. Когнитивно-поведенческие изменения и церебральная псевдоатрофии быть частично или полностью обратимы после отмены вальпроата.
Сообщалось об острой или подострой энцефалопатии без повышения уровня аммония, повышенного уровня препарату или нейровизуализационных изменений. После отмены вальпроата энцефалопатия исчезала частично или полностью.
Со стороны опорно-двигательного аппарата: переломы, снижение минеральной плотности костей, остеопения, остеопороз и слабость.
Со стороны системы крови и лимфатической системы: относительный лимфоцитоз, макроцитоз, лейкопения, анемия, в т.ч. макроцитов с дефицитом фолатов или без него, угнетение функции костного мозга, панцитопения, апластическая анемия, агранулоцитоз и острая периодическая порфирия.
Со стороны эндокринной системы: нерегулярные менструации, вторичная аменорея, гиперандрогенизма, гирсутизм, повышенный уровень тестостерона, увеличение молочной железы, галакторея, отек околоушной железы, поликистоз яичников, снижение концентрации карнитина, гипонатриемия, гиперглицинемия и неадекватная секреция АДГ.
Редко сообщали о синдроме Фанкони, возникающее преимущественно у детей.
Со стороны метаболизма и питания: увеличение массы тела.
Со стороны репродуктивной системы: аспермия, азооспермия, уменьшение количества сперматозоидов, снижение подвижности сперматозоидов, мужское бесплодие и патологическая морфология сперматозоидов.
Со стороны мочевыделительной системы: энурез и инфекция мочевыводящих путей.
Со стороны органов слуха и равновесия: потеря слуха.
Прочее: аллергическая реакция, анафилаксия, задержка развития, боль в костях, брадикардия и кожный васкулит.
Срок годности Теравас
2 года.
Условия хранения Теравас
Хранить при температуре не выше 25 ° С.
Хранить в недоступном для детей месте.
Упаковка
По 100 таблеток в контейнере. По 1 контейнеру в картонной коробке.
Категория отпуска
По рецепту.
Производитель
Д-р Редди'с лаборатории Лимитед.
Местонахождение производителя
Участок № 41, с. Бачупали, Бачупали Мандал, округ Медчал Малкайгири, Телангана 500090, Индия (IND).
Сообщить о побочной реакции или отсутствии эффективности при применении лекарственного средства Вы можете по телефонам (круглосуточно): +380 44 207 51 97 или +380 50 414 39 39.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Теравас только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- http://www.drreddys.ua - ООО «Др. Реддис Лабораториз»
- http://www.drlz.com.ua - Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Теравас |
| Производитель: | ООО «Др. Реддис Лабораториз» |
| Форма выпуска: | таблетки пролонгированного действия по 250 мг или 500 мг, по 100 таблеток в контейнере; по 1 контейнеру в картонной коробке |
| Регистрационное удостоверение: | UA/18012/01/01, UA/18012/01/02 |
| Дата начала: | 06.05.2020 |
| Дата окончания: | 05.06.2025 |
| МНН: | Valproic acid |
| Условия отпуска: | по рецепту |
| Состав: | 1 таблетка содержит дивалпроекс натрия в пересчете на вальпроевой кислоты 250 мг или 500 мг |
| Фармакологическая группа: | Противоэпилептические средства. |
| Код АТХ: | N03AG01 |
| Заявитель: | ООО «Др. Реддис Лабораториз» |
| Страна заявителя: | Индия |
| Адрес заявителя: | 8-2-337, Роуд № 3, Банджара Хиллз, Хайдерабад, Телангана - 500034, Индия |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Нет |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Моно |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| N | Средства, действующие на нервную систему |
| N03 | Противоэпилептические средства |
| N03A | Противоэпилептические средства |
| N03AG | Производные жирных кислот |
| N03AG01 | Кислота вальпроевая |

