- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Рековель инструкция по применению
Официальная инструкция лекарственного препарата Рековель раствор 12 мкг/0,36 мл, 36 мкг/1,08 мл, 72 мкг/2,16 мл. Описание и применение Rekovel', аналоги и отзывы. Инструкция Рековель раствор утвержденная компанией производителем.
Состав
действующее вещество: фолитропин дельта;
1 мл раствора для инъекций содержит 33,3 мкг фолитропин дельта,
1 предварительно наполненая шприц-ручка содержит:
12 мкг фолитропин дельта в 0,36 мл раствора для инъекций или
36 мкг фолитропин дельта в 1,08 мл раствора для инъекций, или
72 мкг фолитропин дельта в 2,16 мл раствора для инъекций.
вспомогательные вещества: фенол; полисорбат 20; L-метионин; натрия сульфат, декагидрат; натрия фосфат, додекагидрат; фосфорная кислота концентрированная; натрия гидроксид вода для инъекций.
Лекарственная форма
Раствор для инъекций.
Основные физико-химические свойства: прозрачный и практически свободен от видимых частиц раствор.
Фармакологическая группа
Гормоны половых желез и препараты, применяемые при патологии половой сферы. Гонадотропные гормоны.
Код ATH G03G A10.
Фармакологические свойства
Фармакологические.
Фолитропин дельта является рекомбинантным ФСГ (ФСГ) человека, производится в линии клеток человека PER.C6 по технологии рекомбинантной ДНК. Последовательности аминокислот двух субъединиц ФСГ в фолитропин дельта идентичны последовательностям эндогенного ФСГ человека. Поскольку фолитропин дельта производится в линии клеток человека PER.C6, профиль гликозилирования отличается от такового у фолитропин альфа и фолитропин бета.
механизм действия
Важнейшим эффектом, который достигается при парентеральном введении ФСГ, является развитие множественных созревших фолликулов.
фармакодинамические эффекты
После ежедневного введения равных по МО доз лекарственного средства Рековель и фолитропин альфа, как определено в биологическом анализе в условиях in vivo на крысах (анализ по Стилмен - Поле (Steelman-Pohley)), более выраженная реакция яичников (по уровням эстрадиола, ингибина В и по объему фолликулов) наблюдалась после введения лекарственного средства Рековель, чем фолитропин альфа. Поскольку биологический анализ на крысах может не в полной мере отражать мощность действия ФСГ, входящий в состав лекарственного средства Рековель, у людей, лекарственное средство Рековель дозируется в мкг, а не в МО.
Количество пригодных для взятия ооцитов увеличивается с дозой лекарственного средства Рековель и сывороточной концентрацией антимюллерового гормона (АМГ). И наоборот, увеличение массы тела приводит к уменьшению количества пригодных для взятия ооцитов (клинически значимым только при дозах лекарственного средства Рековель менее 12 мкг).
Клинические эффективность и безопасность
Исследование ESTHER-1 было рандомизированное, слепым для исследователя, контролируемым исследованием с участием 1326 пациенток, которым выполнялось оплодотворения in vitro(Экстракорпоральное оплодотворение (ЭКО)) / Интрацитоплазматические инъекции спермы (ИЦИС). В этом исследовании индивидуальный режим дозирования лекарственного средства Рековель с определением суточной дозы для каждой пациентки и фиксацией дозы для всего периода стимуляции без корректировки (см. Раздел «Способ применения и дозы») сравнивали с фолитропин альфа с дозировкой по массе тела, начальная доза 11 мкг (150 МЕ) для первых пяти дней с последующей корректировкой со дня 6 стимуляции в зависимости от развития фолликулов по протоколу антагониста гонадотропин-рилизинг-гормона (ГнРГ). Возраст пациенток составил до 40 лет включительно, пациентки имели регулярные менструальные циклы, считались овуляторные. Пересадка одной бластоцисты в день 5 было обязательным, за исключением пациенток в возрасте 38-40 лет, которым выполнялась пересадка двух бластоцист при отсутствии бластоцисты надлежащего качества. Двумя копервиннимы конечными точками были частота беременности, продолжавшейся, и частота имплантации, которая длилась, в новом цикле, которые определялись как минимум один внутриматочное жизнеспособный плод через 10-11 недель после пересадки и количество внутриматочных жизнеспособных плодов через 10-11 недель после пересадки, деленная на количество пересаженных бластоцист, соответственно.
Исследование показало, что лекарственное средство Рековель имел по крайней мере такую же эффективность, как фолитропин альфа, по частоте беременности, продолжавшейся, и по частоте имплантации, что длительная (см. Табл. 1).
Таблица 1. Частота беременности, продолжавшейся, и частота имплантации, которая длилась, в исследовании ESTHER-1
показатель | Рековель, индивидуальный режим дозирования (N = 665) | фолитропин альфа (N = 661) | Разница [95% ДИ] |
Частота беременности, продолжавшейся | 30,7 % | 31,6 % | -0,9 % [-5,9 %; 4,1 %] |
Частота имплантации, которая длилась | 35,2 % | 35,8 % | -0,6 % [-6,1 %; 4,8 %] |
Популяция: все рандомизированные пациентки, получавших лечение.
Влияние режима дозирования лекарственного средства Рековель по уровню АМГ также оценивался в вторичных конечных точках, таких как реакция яичников и управления риском синдрома гиперстимуляции яичников (СГЯ).
В общей популяции исследования среднее количество пригодных для взятия ооцитов составила 10,0 ± 5,6 при применении лекарственного средства Рековель (N = 636) по индивидуальным режимом дозирования и 10,4 ± 6,5 при применении фолитропин альфа (N = 643) в начальной дозе 150 МЕ с последующей корректировкой дозы.
Среди пациенток с уровнем АМГ ≥ 15 пмоль / л реакция яичников при применении лекарственного средства Рековель (N = 355) и фолитропин альфа (N = 353) была следующей: среднее количество пригодных для взятия ооцитов 11,6 ± 5,9 и 13,3 ± 6,9 и доля пациенток с ≥ 20 ооцитов 10,1% (36/355) и 15,6% (55/353) соответственно.
В овуляторных пациенток с поликистозных яичников частота возникновения раннего СГЯ средней и тяжелой степени и / или превентивных вмешательств через раннее развитие СГЯ составила 7,7% при применении лекарственного средства Рековель и 26,7% при применении фолитропин альфа.
Безопасность / иммуногенность
Антитела к ФСГ определялись перед лечением и после лечения у пациенток, получавших до трех повторных циклов терапии лекарственным средством Рековель (665 пациенток в цикле 1 и 252 пациентки в цикле 2 в исследовании ESTHER-1 и 95 пациенток в цикле 3 в исследовании ESTHER-2 ). Частота возникновения антител к ФСГ после терапии лекарственным средством Рековель составила 1,1% в цикле 1, 0,8% - в цикле 2 и 1,1% - в цикле 3. Эти показатели частоты были подобны показателя частоты антител к ФСГ, что определялся до начала терапии лекарственным средством Рековель в цикле 1 и составлял 1,4%, и сопоставимым с показателями частоты антител к ФСГ после лечения фолитропин альфа. Во всех пациенток с антителами к ФСГ титры были ниже порог чувствительности или очень низкими и без нейтрализующей способности.
Отсутствует опыт применения лекарственного средства Рековель в клинических исследованиях по протоколу длительного введения агониста ГнРГ.
Фармакокинетика.
Фармакокинетический профиль фолитропин дельта исследовали у здоровых женщин и у пациенток, которым выполняли контролируемую стимуляцию яичников в рамках ЭКО / цикла ИЦИС. После повторяющихся ежедневных подкожных инъекций лекарственного средства Рековель равновесное состояние достигается в течение 6-7 дней с концентрацией, в 3 раза превышает концентрацию после введения первой дозы. Циркулирующие уровни фолитропин дельта обратно пропорциональны массе тела, обосновывает индивидуальное дозирование по массе тела. Фолитропин дельта характеризуется более выраженной терапевтическим действием, чем фолитропин альфа.
всасывания
При ежедневном подкожном введении лекарственного средства Рековель максимальная концентрация в сыворотке крови достигается через 10:00. Биодоступность составляет около 64%.
распределение
Видимый объем распределения после подкожного введения составляет около 25 л, а объем распределения в равновесном состоянии после внутривенного введения - 9 л. В пределах диапазона терапевтических доз экспозиция фолитропин дельта растет пропорционально дозе.
вывод
После подкожного и внутривенного введения видимый клиренс фолитропин дельта составляет 0,6 л / ч и 0,3 л / ч соответственно. Терминальный период полувыведения после однократного и многократного подкожного введения составляет 40 часов и 28 часов соответственно. Видимый клиренс фолитропин дельта низкий, 0,6 л / ч после многократных подкожных введений, что обеспечивает выраженное терапевтическое действие. Фолитропин дельта прогнозируемо выводится из организма подобно другим фолитропин, то есть преимущественно почками. В неизменном виде с мочой выводится примерно 9% фолитропин дельта.
Клинические характеристики
Рековель Показания
Контролируемая стимуляция яичников для развития множественных фолликулов у женщин в рамках проведения вспомогательных репродуктивных технологий (ВРТ), таких как экстракорпоральное оплодотворение (ЭКО) или цикл Интрацитоплазматическая инъекций спермы (ИЦИС).
Противопоказания
- Повышенная чувствительность к действующему веществу или к любому из вспомогательных веществ, перечисленных в разделе «Состав»;
- опухоли гипоталамуса или гипофиза
- увеличение яичников или кисты, не связанные с синдромом поликистозных яичников;
- гинекологические кровотечения неизвестной этиологии
- карцинома яичников, матки или молочных желез.
Случаи, которые делают невозможным достижение цели лечения лекарственным средством Рековель:
- первичная недостаточность яичников;
- врожденные пороки половых органов, несовместимые с беременностью;
- фиброидни опухоли матки, несовместимые с беременностью.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Исследование взаимодействия с лекарственным средством Рековель не проводились. О клинически значимые взаимодействия с другими лекарственными средствами при терапии лекарственным средством Рековель не сообщалось, такие взаимодействия не ожидается.
Особенности применения
Лекарственное средство Рековель содержит действующее вещество с мощной гонадотропной действием, что может привести побочные реакции от легкой до тяжелой степени, поэтому этот препарат должны назначать только врачи, которые хорошо знакомы с проблемами бесплодия и методами его лечения.
Терапия гонадотропинами требует определенных затрат времени со стороны врачей и других медицинских работников, а также наличия соответствующих средств контроля. Безопасность и эффективность применения лекарственного средства Рековель предусматривает регулярный контроль овариальной реакции с использованием только ультразвукового исследования или в сочетании с определением уровня эстрадиола в сыворотке крови. Дозу лекарственного средства Рековель подбирают индивидуально каждой пациентке для достижения реакции яичников с благоприятным профилем безопасности / эффективность. Возможны межиндивидуальные колебания ответа на введение ФСГ от слабого ответа на ФСГ в одних пациенток к чрезмерной у других.
Перед началом лечения бесплодное супругов следует обследовать для выявления имеющихся и возможных противопоказаний к беременности. В частности, пациентов следует обследовать по гипотиреоза и гиперпролактинемии и назначить соответствующее специфическое лечение.
Для подбора дозы Рековеля рекомендуется использовать результаты определения АМГ с помощью иммуноанализа ELECSYS AMH Plus от Roche, поскольку использовалась стандартизация анализа АМГ по данным тестом в ходе исследований.
У пациенток, которым выполняется стимуляция роста фолликулов, возможно увеличение яичников и существует риск развития синдрома гиперстимуляции яичников. Четкое соблюдение дозы и режима введения лекарственного средства Рековель, а также тщательный контроль терапии уменьшат частоту возникновения таких явлений.
Синдром гиперстимуляции яичников (СГЯ)
Некоторое увеличение размеров яичников является ожидаемым следствием контролируемой стимуляции яичников. Это явление наиболее распространено у пациенток с синдромом поликистозных яичников и обычно проходит без соответствующего лечения. В отличие от неосложненного увеличения яичников, СГЯ является состоянием, которое может проявляться с нарастанием степени тяжести. Он включает значительное увеличение яичников, высокие уровни половых стероидных гормонов в сыворотке крови и увеличение сосудистой проницаемости, что может приводить к накоплению жидкости в брюшной, плевральной и редко в перикардиальной полостях.
Очень важным для снижения риска СГЯ является тщательный и регулярный контроль развития фолликулов. В тяжелых случаях СГЯ могут наблюдаться следующие симптомы: боль, дискомфорт и ощущение растяжения в брюшной полости, значительное увеличение яичников, увеличение массы тела, одышка, олигурия и симптомы со стороны желудочно-кишечного тракта, включая тошноту, рвоту и диарею. При клиническом обследовании могут быть выявлены гиповолемия, сгущение крови, электролитный дисбаланс, асцит, гемоперитонеум, плевральный выпот, гидроторакс или острый респираторный дистресс-синдром. Очень редко тяжелый СГЯ может осложняться искажением яичников или тромбоэмболических явлений, таким как эмболия легочной артерии, ишемический инсульт и инфаркт миокарда.
Если не применяется хорионический гонадотропин человека (ХГЧ) для стимуляции окончательного созревания фолликулов, чрезмерная реакция яичников на лечение гонадотропином редко усиливается к СГЯ. Кроме того, синдром может иметь более тяжелое и длительное течение с наступлением беременности. Поэтому при наличии признаков гиперстимуляции яичников будет целесообразным отложить введение ХГЧ и рекомендовать пациентке воздержаться от половых сношений или применять барьерные средства контрацепции в течение не менее 4 дней. СГЯ может быстро прогрессировать (в течение периода от 24 часов до нескольких дней) и становиться серьезным медицинским явлением. Чаще всего он возникает после прекращения гормонального лечения. Также, как следствие гормональных изменений во время беременности, возможно позднее развитие СГЯ.
тромбоэмболические явления
У женщин с недавним или существующим тромбоэмболических заболеваний или у женщин с общепринятыми факторами риска тромбоэмболических явлений, такими как индивидуальный или семейный анамнез, тяжелое ожирение (индекс массы тела> 30 кг / м2) или тромбофилия, может быть повышен риск венозных и артериальных тромбоэмболических явлений в время или после лечения гонадотропинами. Лечение гонадотропинами может привести к дальнейшему росту риска обострения или появления вышеупомянутых явлений. У таких женщин следует оценивать пользу применения гонадотропина по сравнению с рисками. Однако следует отметить, что собственно беременность, а также СГЯ тоже увеличивают риск развития тромбоэмболических явлений.
искажения яичников
При проведении циклов ВРТ сообщалось о случаях искажения яичников. Это может быть связано с другими факторами риска, такими как СГЯ, беременность, предварительное оперативное вмешательство на органах брюшной полости, искажения яичников в анамнезе, предыдущие имеются ли кисты яичников или поликистозных яичников. Поражение яичника вследствие ухудшения кровообращения можно минимизировать благодаря ранней диагностике и немедленному устранению перекруту.
многоплодная беременность
Многоплодная беременность несет повышенный риск неблагоприятных последствий для матери и в перинатальный период. У пациенток, которым проводятся процедуры ВРТ, риск многоплодной беременности связан главным образом с количеством пересаженных эмбрионов, их качеством и возрастом пациентки, однако беременность двумя плодами в редких случаях может развиться после пересадки одного эмбриона. Перед началом лечения пациенток следует информировать о потенциальном риске многоплодной беременности.
прерывание беременности
У пациенток, которым проводится контролируемая стимуляция яичников в рамках ВРТ, частота прерывания беременности в результате выкидыша или аборта выше, чем после естественного оплодотворения.
внематочная беременность
У женщин с заболеванием маточных труб в анамнезе риск внематочной беременности независимо от того, она наступила в результате спонтанного оплодотворения, или лечения бесплодия. Сообщалось, что после проведения ВРТ распространенность внематочной беременности выше, чем в общей популяции.
Новообразования репродуктивной системы
Зарегистрированы случаи как доброкачественных, так и злокачественных новообразований яичников и других органов репродуктивной системы у женщин, которым было применено несколько режимов лечения бесплодия. Еще не выяснено, лечение гонадотропинами увеличивает риск развития таких опухолей у бесплодных женщин.
врожденные пороки
Распространенность врожденных пороков после проведения ВРТ может быть несколько выше, чем после спонтанного оплодотворения. Считают, что это является следствием разницы в характеристиках родителей (например материнский возраст, качество спермы) и многоплодной беременности.
Другие медицинские состояния
Медицинские состояния, является противопоказанием для беременности, также следует оценивать до начала лечения лекарственным средством Рековель.
Нарушение функции почек и печени
Применение лекарственного средства Рековель не исследовалась у пациентов с умеренным / тяжелым нарушением функции почек или печени.
содержание натрия
Лекарственное средство Рековель содержит менее 1 ммоль натрия (23 мг) в одной дозе, то есть фактически свободным от натрия.
Применение в период беременности или кормления грудью
Беременность.
Рековель не показан во время беременности. После клинического применения контролируемой стимуляции яичников гонадотропинами о тератогенном риск не сообщалось. Данные по случайного применения лекарственного средства Рековель беременным женщинам отсутствуют. В исследованиях на животных продемонстрирована репродуктивная токсичность лекарственного средства Рековель в дозах, превышающих рекомендованную максимальную дозу для человека. Значимость этих данных для клинического применения лекарственного средства Рековель ограничено.
Кормления грудью.
Рековель не показан во время кормления грудью.
Репродуктивная функция.
Рековель показан при бесплодии (см. Раздел «Показания»).
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Рековель не влияет или оказывает незначительное влияние на способность управлять транспортными средствами и работать с другими механизмами.
Способ применения Рековель и дозы
Лечение следует начинать под наблюдением врача, имеющего опыт лечения нарушений репродуктивной функции.
дозировка
Дозировка лекарственного средства Рековель индивидуален для каждой пациентки и имеет целью получение реакции яичников с благоприятным профилем безопасности / эффективность, то есть достижения развития достаточного количества пригодных для взятия ооцитов и уменьшение количества вмешательств для предотвращения СГЯ. Рековель дозируется в мкг (см. Раздел «Фармакологические»). Режим дозирования является специфическим для лекарственного средства Рековель и доза в мкг не может быть применена для других гонадотропинов.
Для первого цикла лечения индивидуальную суточную дозу следует определять по сыворотке уровнем АМГ и массой тела пациентки. Дозу следует рассчитывать на основе недавно определенного уровня АМГ (т.е. в течение последних 12 месяцев) с помощью диагностического теста Roche: иммуноанализ ELECSYS AMH Plus (см. Раздел «Особенности применения»). Индивидуальную суточную дозу следует применять в течение всего периода стимуляции. Для женщин с уровнем АМГ <15 пмоль / л суточная доза составляет 12 мкг независимо от массы тела. Для женщин с уровнем АМГ ≥ 15 пмоль / л доза снижается с 0,19 до 0,10 мкг / кг соответственно к повышению концентрации АМГ (см. Табл. 2). Дозу округлить до стократной 0,33 мкг, чтобы она совпадала со шкалой дозировки на шприц-ручке. Максимальная суточная доза для первого цикла лечения составляет 12 мкг.
Для расчета дозы лекарственного средства Рековель массу тела следует измерять непосредственно перед началом стимуляции. При измерении массы тела пациентка должна снять обувь и верхнюю одежду.
Таблица 2. Режим дозирования
Уровень АМГ (пмоль / л) | <15 | 15—16 | 17 | 18 | 19—20 | 21—22 | 23—24 | 25—27 | 28—32 | 33—39 | ≥ 40 |
Фиксированная суточная доза лекарственного средства Рековель | 12 | 0,19 | 0,18 | 0,17 | 0,16 | 0,15 | 0,14 | 0,13 | 0,12 | 0,11 | 0,10 |
мкг | мкг / кг | ||||||||||
Концентрация АМГ выражается в пмоль / л и должно быть округлена до ближайшего целого числа. Если концентрация АМГ выраженная в нг / мл, перед применением это значение следует перевести в пмоль / л путем умножения на 7,14 (нг / мл × 7,14 = пмоль / л).
мкг - микрограмма.
Лечение лекарственным средством Рековель следует начинать на 2-й или 3-й день после начала менструального кровотечения; лечение должно продолжаться до достижения соответствующего развития фолликулов (≥ 3 фолликулов ≥ 17 мм), в среднем происходит на 9-й день лечения (диапазон 5-20 дней). Доза 250 мкг рекомбинантного ХГЧ, или 5000 МЕ ХГЧ, назначается для стимуляции окончательного созревания фолликулов. Следует прекратить лечение лекарственным средством Рековель и не выполнять стимуляцию окончательного созревания фолликулов с помощью ХГЧ пациенткам с избыточным развитием фолликулов (≥ 25 фолликулов ≥ 12 мм).
Для последующих циклов лечения суточную дозу лекарственного средства Рековель следует оставлять без изменения корректировать, руководствуясь реакцией яичников пациентки в предыдущем цикле. Если в предыдущем цикле была достигнута соответствующая реакция яичников без развития СГЯ, следует применять такую же дозу. В случае недостаточной реакции яичников в предыдущем цикле дозу следующего цикла следует увеличить на 25% или 50% в зависимости от степени наблюдаемой реакции. В случае чрезмерной реакции яичников в предыдущем цикле суточную дозу в следующем цикле следует уменьшить на 20% или 33% в зависимости от степени наблюдаемой реакции. Пациенткам, у которых развился СГЯ или существовал риск развития СГЯ в предыдущем цикле, суточную дозу в следующем цикле следует уменьшить на 33% по сравнению с дозой, при применении которой наблюдался СГЯ или риск его возникновения.
Пациенты с нарушением функции почек и печени
Безопасность, эффективность и фармакокинетику лекарственного средства Рековель у пациентов с нарушением функции почек или печени в клинических исследованиях целенаправленно не изучали. Ограниченные данные не указывают на необходимость применения иного режима дозирования лекарственного средства Рековель для этой популяции пациентов.
Пациентки с синдромом поликистозных яичников с ановуляторными расстройствами
Применение лекарственного средства женщинам с ановуляцией и синдромом поликистозных яичников не исследовалась. Клинические исследования проводились с участием пациенток с овуляцией и с синдромом поликистозных яичников.
Пациенты пожилого возраста
Соответствующие показания для применения лекарственного средства Рековель пациентам пожилого возраста отсутствуют.
способ применения
Рековель предназначен для подкожного введения, преимущественно в область стенки брюшной полости. Первую инъекцию следует выполнять под непосредственным наблюдением медицинского работника. Пациентки должны быть обучены правильному пользованию шприц-ручкой Рековель и выполнению инъекций. Самостоятельное введение лекарственного средства могут проводить только должным образом обученные пациентки, в случае необходимости имеют возможность проконсультироваться с врачом.
ИНСТРУКЦИЯ
по использованию предварительно наполненной шприц-ручки Рековель
Прежде чем выполнять первую инъекцию, медицинский работник должен показать Вам, как правильно приготовить и вводить лекарственное средство Рековель.
Не пытайтесь инъекцию, пока медицинский работник не покажет Вам, как правильно это сделать.
Перед использованием предварительно наполненной шприц-ручки Рековель и каждый раз перед началом использования новой шприц-ручки полностью прочитайте эту инструкцию. Она может содержать новую информацию. Тщательно придерживайтесь этой инструкции, даже если ранее Вы уже применяли подобную шприц-ручку. Неправильное использование этой шприц-ручки может привести к введению несоответствующей дозы лекарственного средства.
Обратитесь к медицинскому работнику, если у Вас есть какие-либо вопросы по выполнению инъекции лекарственного средства Рековель.
Предварительно наполнена шприц-ручка Рековель является одноразовой шприц-ручкой с видмирюваною дозой, может использоваться для ввода более 1 дозы лекарственного средства Рековель. Эта шприц-ручка имеется с 3 различными дозировками:
- 12 мкг / 0,36 мл
- 36 мкг / 1,08 мл
- 72 мкг / 2,16 мл.
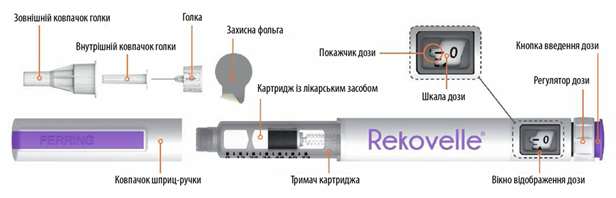
Строение предварительно наполненной шприц-ручки Рековель
важная информация
- Предварительно наполнена шприц-ручка Рековель и иглы предназначены для использования только одним человеком, их не следует передавать другим людям.
- Это шприц-ручку следует использовать только по медицинским показаниям и четко следовать указаниям, предоставленных медицинским работником.
- Если у Вас полная или частичная потеря зрения и Вы не можете прочитать шкалу дозы на шприц-ручке, не используйте эту шприц-ручку без посторонней помощи. Введение возможно с помощью человека, который хорошо видит и обученная применять эту шприц-ручку.
- Если у Вас есть вопросы, прежде чем вводить Рековель, обратитесь к медицинскому работнику.
Информация о предварительно наполненную шприц-ручку Рековель
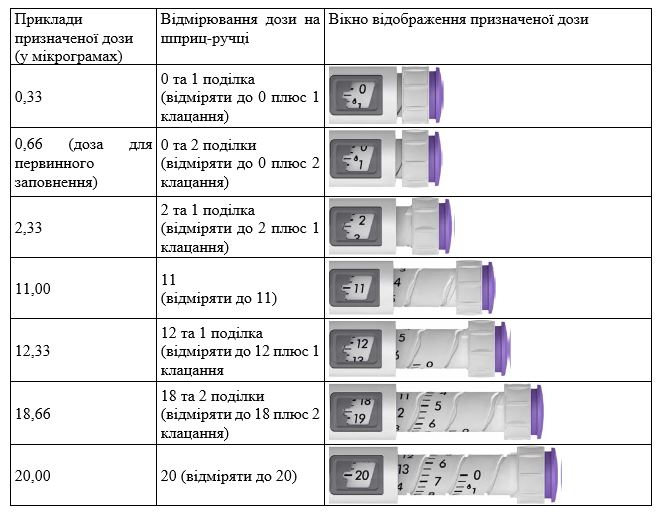
На этой шприц-ручке может быть отмерено доза от 0,33 мкг до 20 мкг лекарственного средства Рековель с делениями для увеличения на 0,33 мкг. См. «Примеры отмеривания дозы».
- Шкала дозы этого шприц-ручки имеет нумерацию от 0 до 20 мкг.
- Каждый номер отделяется двумя делениями. Каждое деление соответствует увеличению видмирюванои дозы на 0,33 мкг.
- При вращении регулятора для отмеривания дозы будет слышно щелчок и ощущение сопротивления при каждом увеличении дозы, что позволяет отмерить корректную дозу.
очистка
- Если необходимо, наружная поверхность шприц-ручки может быть очищена тканью, смоченной водой.
- Нельзя класть эту шприц-ручку в воду или любую другую жидкость.
хранение
- Это шприц-ручку следует всегда хранить с надетым колпачком шприц-ручки и с отсоединенной иглой.
- Не применять эту шприц-ручку после окончания срока годности ( «Приди. До»), указанного на этикетке шприц-ручки.
- Не хранить шприц-ручку в условиях воздействия экстремальных температур, прямых солнечных лучей или при очень низких температурах, например в автомобиле или морозильной камере.
- Хранить шприц-ручку в месте, недоступном для детей и любого лица, не обучена пользоваться этой шприц-ручкой.
Перед применением:
- Хранить шприц-ручку в холодильнике при температуре от 2 до 8 ° C. Не замораживать.
- Хранение шприц-ручки в холодильнике (при температуре от 2 до 25 ° C) может длиться до 3 месяцев, включая период применения. Выбросить (утилизировать) шприц-ручку через 3 месяца, если она не была использована.
После первого применения (период применения):
- Это шприц-ручку можно хранить в течение периода до 28 дней при температуре от 2 до 25 ° C.
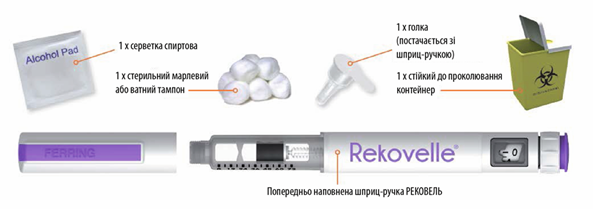
Материалы, необходимые для инъекции лекарственного средства Рековель
Перед применением (шаг 1)
Шаг 1:
- Вымыть руки.
- Осмотреть шприц-ручку, убедиться, что она не повреждена. Не использовать шприц-ручку, если она повреждена.
- Осмотреть шприц-ручку (картридж), убедиться, что лекарственное средство прозрачный и не содержит частиц. Не использовать шприц-ручку, если лекарственное средство в картридже содержит частицы или непрозрачен.
- Убедиться, что у Вас соответствующая шприц-ручка с соответствующим дозировкой.
- Проверить дату окончания срока годности на этикетке шприц-ручки.
Подключение иглы (шаги со 2-го по 6-й)
важно:
- Всегда использовать новую иглу для каждой инъекции.
- Использовать только одноразовые иглы, поставляемых с шприц-ручкой.
Шаг 2:
- Снять колпачок шприц-ручки.
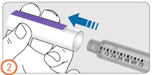
Шаг 3:
- Снять защитную фольгу с иглы.
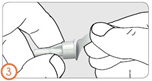
Шаг 4:
- Подсоединить иглу.
- Признаком надежного подключения иглы является щелчок.
- Также можно навинтить иглу. Ощущение легкого сопротивления свидетельствует, что игла надежно подключена.
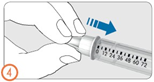
Шаг 5:
- Снять внешний колпачок иглы.
- Не выбрасывать внешний колпачок. Он понадобится для утилизации иглы после инъекции лекарственного средства.
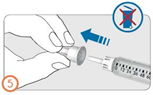
Первичное заполнение (шаги с 7-го по 9-й)
- Перед первым применением шприц-ручки необходимо удалить пузырьки воздуха из картриджа (выполнить первичное заполнение), что необходимо для получения корректной дозы лекарственного средства.
- Первичное заполнение выполняется только перед первым использованием шприц-ручки.
- Выполнять шаги с 7-го по 9-й, даже если пузырьков воздуха не видно.
- Если шприц-ручка уже применялась, следует перейти к шагу 10.
Шаг 7:
- Вращать регулятор дозы по часовой стрелке, пока указатель дозы не будет указывать на символ «капля».
- Если отмерено неправильную дозу для первичного заполнения, ее можно откорректировать без потери лекарственного средства, обращая регулятор дозы в любом направлении, пока указатель дозы не будет указывать на символ «капля».
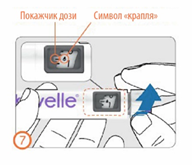
Шаг 8:
- Удерживать шприц-ручку иглой вверх.
- Постучать пальцем по держателю картриджа, чтобы пузырьки воздуха поднялись вверх, в верхнюю часть картриджа.
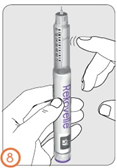
Шаг 9:
- Отпуская шприц-ручку иглой вверх (не в сторону лица), полностью нажать кнопку введения дозы, пока указатель дозы не указывает число «0».
- Убедиться, что капля жидкости появилась на конце иглы.
- Если капля (капли) не явился, повторить шаги с 7-го по 9-й (первичное заполнение), пока капля не появится.
- Если после 5 попыток капля не появилась, удалить иглу (см. Шаг 13), подсоединить новую иглу (см. Шаги с 3-го по 6-й) и повторить первичное заполнение (см. Шаги с 7-го по 9-й).
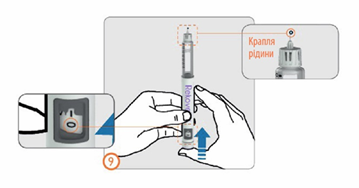
Отмеривание дозы (шаг 10)
См. табл. 3 Примеры отмеривания дозы.
Шаг 10:
- Вращать регулятор дозы по часовой стрелке, пока указатель дозы не будет указывать на назначенную дозу в окне отображения дозы.
- Дозу можно откорректировать в сторону увеличения или уменьшения без потери лекарственного средства, обращая регулятор дозы в любом направлении, пока указатель дозы не будет указывать на корректную дозу.
- Не будет нажата на кнопку введения дозы при отмеривания дозы, чтобы избежать потери лекарственного средства.
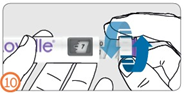
Введение разделенной дозы:
- Может потребоваться более одной шприц-ручка для введения назначенной дозы.
- Если не удается отмерить полную дозу, это означает, что в шприц-ручке остается недостаточно лекарственного средства. Нужно вводить разделенную дозу или выбросить (утилизировать) текущую шприц-ручку и использовать новую, чтобы выполнить инъекцию.
См. ниже раздел «Введение разделенной дозы лекарственного средства Рековель» для примеров расчета и записи разделенной дозы.
Введение дозы (шаги с 11-го по 12-й)
важно:
- Не использовать шприц-ручку, если лекарственное средство содержит частицы или непрозрачен.
- Перед выполнением инъекции ознакомиться с шагами 11 и 12.
- Это лекарственное средство следует вводить путем инъекции только под кожу (подкожно) в область живота.
- Изменение места введения при каждой инъекции снизит риск реакций со стороны кожи, таких как покраснение и раздражение.
- Не выполнять инъекцию в область, что болит (чувствительная), с ушибом, покраснением, отверждением, шрамом или растяжением.
Шаги 11 и 12:
- Протереть кожу в месте инъекции спиртовой салфеткой для чистки. Не касаться этого участка, пока не будет выполнена инъекция.
- Держать шприц-ручку так, чтобы во время инъекции было видно окно отображения дозы.
- Зажать кожу и ввести иглу в кожу под прямым углом, как научил медицинский работник. Не касаться кнопки введения дозы.
- После введения иглы поместить большой палец на кнопку введения дозы.
- Полностью нажать кнопку введения дозы и содержать.
- Удерживать кнопку введения дозы нажатой и после того, как указатель дозы указывать на «0», подождать 5 секунд (медленно считать до 5), чтобы убедиться, что введено всю дозу.
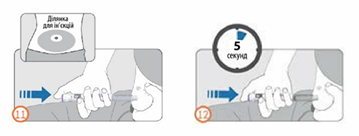
- После удерживание кнопки введения дозы нажатой в течение 5 секунд отпустить ее. Затем медленно удалить иглу из места инъекции, извлекая ее из кожи под прямым углом.
- Если в месте инъекции появляется кровь, слегка прижать к месту инъекции марлевую салфетку или ватный тампон.
Примечание:
- Не наклонять шприц-ручку во время инъекции и удаления из кожи.
- Наклон шприц-ручки может привести к сгибанию или отламывания иглы.
- Если сломана игла остается в теле, следует немедленно обратиться за медицинской помощью.
Утилизация иглы (шаг 13)
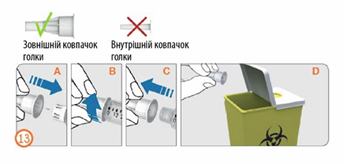
Шаг 13:
- Осторожно надеть на иглу внешний колпачок иглы, сильно нажимая на него (A).
- Откручивать иглу против часовой стрелки для ее отсоединения от шприц-ручки (B + C).
- Осторожно утилизировать использованную иглу (D).
- См. ниже раздел «Утилизация».
Примечание:
- После каждого использования следует всегда утилизировать иглу. Эти иглы предназначены только для одноразового использования.
- Не хранить шприц-ручку с подсоединенной иглой.
Надевание колпачка шприц-ручки (шаг 14)
Шаг 14:
- Тщательно надеть на шприц-ручку колпачок шприц-ручки для защиты между инъекциями.
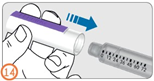
Примечание:
- Колпачок на шприц-ручку нельзя надеть поверх иглы.
- Если вводится разделена доза пустую шприц-ручку следует выбросить (утилизировать).
- Если используется новая шприц-ручка для введения всей назначенной дозы вместо того, чтобы вводить разделенную дозу, следует выбросить (утилизировать) шприц-ручку, в которой недостаточно лекарственного средства для полной дозы.
- Если шприц-ручка не используется, на нее нужно надеть колпачок шприц-ручки.
Утилизация
иглы:
Сразу после использования поместить иглу в устойчивый к проколу контейнер, например в контейнер для использованных острых предметов. Не выбрасывать (Не утилизировать) контейнер с использованными острыми предметами с бытовым мусором.
При отсутствии контейнера для использованных острых предметов возможно использование бытового контейнера, который:
- изготовлен из прочного пластика;
- может быть плотно закрыт стойкой к прокалывания крышкой без возможности попадания острых предметов наружу;
- имеет стабильное вертикальное положение во время эксплуатации;
- является герметичным;
- должным образом маркированным о опасные отходы в контейнере.
Когда контейнер для использованных острых предметов будет почти полный, необходимо утилизировать его в соответствии с местными требованиями.
Предварительно наполненные шприц-ручки Рековель:
- выбросить (утилизировать) использованы шприц-ручки в соответствии с местными требованиями.
Примеры отмеривания дозы
Примеры отмеривания дозы с использованием предварительно наполненной шприц-ручки Рековель
В таблице ниже (табл. 3) приводятся примеры предназначенных доз, способ их отмеривания и вид окна отображения предназначенных доз.
Таблица 3. Примеры отмеривания дозы
Введение разделенной дозы лекарственного средства Рековель
Если не удается отмерить всю назначенную дозу, это означает, что в шприц-ручке остается недостаточно лекарственного средства. Необходимо ввести часть назначенной дозы, используя текущую шприц-ручку, и остальные назначенной дозы, используя новую шприц-ручку (введение разделенной дозы). Также можно выбросить (утилизировать) текущую шприц-ручку и использовать новую шприц-ручку, чтобы ввести всю назначенную дозу в 1 инъекции. Если принято решение вводить разделенную дозу, следует следовать этим инструкциям и записать введенную дозу лекарственного средства в дневнике разделение доз (см. Табл. 4).
- В колонке А приведены примеры назначенной дозы. Необходимо вписать свою назначенную дозу в столбик А.
- В колонке В приведены примеры дозы остается в шприц-ручке (соответствует дозе, которую можно отмерить).
- Необходимо вписать в столбик В дозу остается в шприц-ручке. Выполнить инъекцию дозы остается в шприц-ручке.
- Приготовить новую шприц-ручку и провести первичное заполнение (шаги с 1-го по 9-й).
- Рассчитать и вписать в столбик С дозу остается для ввода, отняв от числа в столбце А число в столбце В. При необходимости использовать калькулятор для проверки расчета.
- Если необходимо, см. «Примеры отмеривания дозы».
- Дозы следует округлять до ближайшего видмирюваного значения: X, 00, X, 33 или X, 66 мкг. Например, если число в колонке C составляет 5,34, доза остается, округляется до 5,33. Если число в столбце C составляет 9,67, доза остается, округляется до 9,66.
- Если есть вопросы по расчету разделение дозы, следует обратиться к медицинскому работнику.
- Ввести дозу, остается (число в столбце C), используя новую шприц-ручку, чтобы завершить ввод назначенной дозы.
Таблица 4. Дневник разделение дозы
А назначенная доза | B Доза остается в шприц-ручке (Доза, на которую указывает указатель дозы в окне отображения дозы) | C = A минус B Доза вводится новой шприц-ручкой (Доза, на которую указывает указатель дозы в окне отображения дозы) |
11,33 | 4,00 (4) | 7,33 (7 и 1 деление (отмерить 7 плюс 1 щелчок)) |
12,66 | 12,33 (12 плюс 1 щелчок) | 0,33 (0 и 1 деление (отмерить 0 плюс 1 щелчок)) |
11,00 | 3,00 (3) | 8,00 (8 (отмерить 8)) |
12,00 | 6,66 (6 и 2 деления (6 плюс 2 щелчка)) | Округлить 5,34 до 5,33 (5 и 1 деление (отмерить 5 плюс 1 щелчок)) |
18,33 | 8,88 (8 и 2 деления (8 плюс 2 щелчка)) | Округлить 6,67 до 9,66 (9 и 2 деления (отмерить 9 плюс 2 щелчка)) |
Дети
Соответствующие показания для применения лекарственного средства Рековель детям отсутствуют.
Передозировка
Эффекты передозировки неизвестны, однако существует риск развития СГЯ (см. Раздел «Особенности применения»).
Побочные эффекты
Краткое описание профиля безопасности
Во время лечения лекарственным средством Рековель чаще всего сообщалось о таких побочных реакциях, как головная боль, тазовый дискомфорт, СГЯ, тазовая боль, тошнота, боль в области придатков матки и утомляемость. Частота этих побочных реакций может снижаться при повторных циклах лечения, как это наблюдалось в клинических исследованиях.
Перечень побочных реакций в форме таблицы
В таблице ниже (табл. 5) приведены побочные реакции у пациенток, получавших лечение лекарственным средством Рековель в клинических исследованиях, по классу системы органов MedDRA и частотой определялась следующим образом: часто (от ≥ 1/100 до <1/10) и нечасто (от ≥ 1/1 000 до <1/100). В каждой группе по частоте побочные реакции приведены в порядке уменьшения серьезности.
Таблица 5. Побочные реакции в базовых клинических исследованиях
Системы органов | Часто (От ≥ 1/100 до <1/10) | Нечасто (От ≥ 1/1 000 до <1/100) |
Со стороны психики | изменения настроения | |
Со стороны нервной системы | Головная боль | сонливость головокружение |
Со стороны желудочно-кишечного тракта | тошнота | диарея рвота Запор Дискомфорт в животе |
Со стороны репродуктивной системы и молочных желез | СГЯ тазовая боль Боль в области придатков матки Тазовий дискомфорт | вагинальное кровотечение Боль в молочных железах Нагрубание молочных желез |
Общие нарушения и состояние в месте введения | утомляемость |
Описание отдельных побочных реакций
СГЯ является неотъемлемым риском при стимуляции яичников. Известные симптомы со стороны желудочно-кишечного тракта, связанные с СГЯ, включают боль, дискомфорт и ощущение растяжения в брюшной полости, тошнота, рвота и диарея. Искажения яичников и тромбоэмболические явления редки осложнениями стимуляции яичников (см. Раздел «Особенности применения»).
Образование антител к ФСГ является потенциальным риском терапии гонадотропинами (см. Раздел «Фармакологические»).
Сообщение о подозреваемых побочные реакции
Сообщение о подозреваемых побочные реакции после регистрации лекарственного средства важны. Это позволяет осуществлять постоянный мониторинг соотношения польза / риск применения этого лекарственного средства. Медицинских работников просят сообщать обо всех подозреваемых побочные реакции через национальную систему сообщений.
Срок годности Рековель
3 года.
Срок годности после первого применения: 28 дней при условии хранения при температуре не выше 25 ° C.
Условия хранения Рековель
Хранить в холодильнике (2-8 ° C). Не замораживать.
Хранить в недоступном для детей месте.
К первому применения хранить в оригинальной упаковке для защиты от света.
Лекарственное средство можно вынуть из холодильника и, не охлаждая его снова, хранить при температуре не выше 25 ° C до 3 месяцев, включая период после первого применения.
После чего лекарственное средство необходимо утилизировать.
Упаковка
12 мкг / 0,36 мл раствора для инъекций
Стеклянный многодозовых картридж объемом 3 мл (стекло типа I) с поршнем с бромбутилового каучука и обжимной алюминиевой крышкой с вкладышем из каучука, помещенный в шприц-ручку. По 1 шприц-ручке в комплекте с 3 стерильными иглами для инъекций (из нержавеющей стали) в картонной коробке.
36 мкг / 1,08 мл раствора для инъекций
Стеклянный многодозовых картридж объемом 3 мл (стекло типа I) с поршнем с бромбутилового каучука и обжимной алюминиевой крышкой с вкладышем из каучука, помещенный в шприц-ручку. По 1 шприц-ручке в комплекте с 6 стерильными иглами для инъекций (из нержавеющей стали) в картонной коробке.
72 мкг / 2,16 мл раствора для инъекций
Стеклянный многодозовых картридж объемом 3 мл (стекло типа I) с поршнем с бромбутилового каучука и обжимной алюминиевой крышкой с вкладышем из каучука, помещенный в шприц-ручку. По 1 шприц-ручке в комплекте с 9 стерильными иглами для инъекций (из нержавеющей стали) в картонной коробке.
Категория отпуска
По рецепту.
Производитель
Ферринг ГмбХ
(Ответственный за выпуск серии, контроль качества (химический и точность дозирования)).
Местонахождение производителя
Витланд 11 24109 Киль, Германия.
Заявитель.
Ферринг Фармацевтикалз А/С.
Местонахождение заявителя.
Кай Фискерс Плас 11, 2300 Копенгаген С, Дания.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Рековель только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- Веттер Фарма-Фертигунг ГмбХ и Ко. КГ
- http://www.drlz.com.ua - Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Рековель |
| Производитель: | Веттер Фарма-Фертигунг ГмбХ и Ко. КГ |
| Форма выпуска: | раствор для инъекций 12 мкг / 0,36 мл, 36 мкг / 1,08 мл или 72 мкг / 2,16 мл, в стеклянном многодозовых картриджи объемом 3 мл с поршнем и обжимной крышкой, который помещен в шприц- ручку; по 1 шприц-ручке в комплекте с 3 стерильными иглами для инъекций (из нержавеющей стали) в картонной коробке |
| Регистрационное удостоверение: | UA/17969/01/01, UA/17969/01/02, UA/17969/01/03 |
| Дата начала: | 06.03.2020 |
| Дата окончания: | 03.06.2025 |
| МНН: | Follitropin delta |
| Условия отпуска: | по рецепту |
| Состав: | 1 мл раствора для инъекций содержит 33,3 мкг фолитропин дельта; / 1 предварительно наполнена шприц-ручка содержит 12 мкг фолитропин дельта в 0,36 мл раствора для инъекций |
| Фармакологическая группа: | Гормоны половых желез и препараты, применяемые при патологии половой сферы. Гонадотропные гормоны. |
| Код АТХ: | G03GA10 |
| Заявитель: | Ферринг Фармацевтикалз А / С |
| Страна заявителя: | Дания |
| Адрес заявителя: | Кай Фискерс Плас 11, 2300 Копенгаген С, Дания |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Да |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Моно |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| G | Средства, влияющие на мочеполовую систему и половые гормоны |
| G03 | Гормоны половых желез и препараты, применяемые при патологии половой сферы |
| G03G | Гонадотропины и другие стимуляторы овуляции |
| G03GA | Гонадотропные гормоны |
| G03GA10 | Фолитропин дельта |