- Общая характеристика
- МНН
- Описание
- Состав
- Форма выпуска
- Фармакотерапевтическая группа
- Фармакологические свойства
- Показания к применению
- Способ применения и дозировка
- Побочные действия
- Противопоказания
- Передозировка
- Меры предосторожности
- Дети
- Период беременности
- Управление автомобилем
- Взаимодействие
- Условия и срок хранения
- Упаковка
- Правила отпуска
- Информация о производителе
Элигард инструкция по применению
Официальная инструкция лекарственного препарата Элигард лиофилизат 7,5 мг, 22,5 мг, 45 мг. Описание и применение Eligard, аналоги и отзывы. Инструкция Элигард лиофилизат утвержденная компанией производителем.
Общая характеристика
Международное непатентованное наименование
Leuprorelin.
Описание
Шприц А(растворитель)
Дозировка 7,5 мг : От светло-желтой до светло-желтой с коричневатым оттенком прозрачная, вязкая жидкость, без видимых посторонних частиц. Допускается наличие пузырьков воздуха.
Дозировки 22,5 мг и 45 мг: От бесцветной до светло-желтой, прозрачная, вязкая жидкость, без видимых посторонних частиц. Допускается наличие пузырьков воздуха.
Шприц Б(лиофилизат лейпрорелина ацетата)
Лиофилизат от белого до почти белого цвета, без видимых посторонних частиц.
Восстановленный раствор
Дозировка 7,5 мг: от светло-желтой до светло-желтой с коричневатым оттенком вязкая жидкость без видимых посторонних частиц. Допускается наличие пузырьков воздуха. Дозировки 22,5 мг и 45 мг: от бесцветной до светло-желтого цвета вязкая жидкость без видимых посторонних частиц. Допускается наличие пузырьков воздуха.
Состав лекарственного средства
1 шприц А содержит:
активное вещество: нет
вспомогательные вещества:
растворитель, состоящий из:
| Название компонента | Дозировка7,5 мг | Дозировка22,5 мг | Дозировка45 мг |
| Сополимер поли-D,L-лактид-ко-гликолид: ПЛГХ (50:50) | 117 мг | - | - |
| ПЛГ (75:25) | - | 206 мг | - |
| ПЛГ (85:15) | - | - | 217 мг |
| N-метил-2-пирролидон | 226 мг | 251 мг | 217 мг |
1 шприц Б содержит:
активное вещество: лейпрорелина ацетат*
дозировка 7,5 мг: 10,6 мг (эквивалентно 9,83 мг лейпрорелина)
дозировка 22,5 мг: 29,2 мг (эквивалентно 27,1 мг лейпрорелина)
дозировка 45 мг:59,2 мг (эквивалентно 54,9 мг лейпрорелина)
вспомогательные вещества: нет
*Избыток лейпрорелина ацетата компенсирует потери в шприце и игле.
Восстановленный раствор (вводимая доза) содержит 7,5 мг, 22,5 мг или 45 мг лейпрорелина ацетата.
Форма выпуска
Лиофилизат для приготовления раствора для подкожного введения.
Фармакотерапевтическая группа
Противоопухолевое средство, гонадотропин-рилизинг гормона аналог.
Код ATX: L02A Е02.
Фармакологические свойства
Фармакодинамика. Лейпрорелин является синтетическим непептидным аналогом естественного гонадотропин-рилизинг-гормона (ГнРГ), который при длительном применении ингибирует секрецию гипофизарного гонадотропина и подавляет тестикулярный стероидогенез у мужчин. Аналог обладает большей эффективностью, чем естественный гормон и его воздействие обратимо при прекращении лечения. Однако, агонист обладает большей активностью, чем естественный гормон и время до восстановления уровня тестостерона у пациентов может варьироваться.
Назначение лейпрорелина сначала приводит к повышению уровня циркулирующего лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ), в результате чего временно повышается уровень гонадных стероидов, тестостерона и дигидротестостерона у мужчин. При продолжительном применении лейпрорелина уровень ЛГ и ФСГ снижается. У мужчин уровень тестостерона снижается до кастрационного уровня (≤ 50 нг/дл) в течение 3-5 недель после начала лечения. Средний уровень тестостерона через 6 месяцев лечения составляет 6,1 (± 0,4) нг/дл для дозировки 7,5 мг; 10,1 (± 0,7) нг/дл для дозировки 22,5 мг и 10,4 (± 0,53) нг/дл для дозировки 45 мг. Эти значения сопоставимы с уровнем тестостерона после выполнения билатеральной орхиэктомии.
Все пациенты, принимавшие участие в базовом клиническом исследовании препарата Элигард 7,5 мг, достигли кастрационного уровня тестостерона на 6-й неделе; 94% достигли этого уровня к 28 дню и 98% к 35 дню. У подавляющего большинства пациентов уровни тестостерона были ниже 20 нг/дл, хотя полноценное преимущество данных низких уровней тестостерона пока еще не было установлено. Уровень ПСА снизился на 94% в течение шести месяцев.
Все пациенты, получавшие полную дозу лейпрорелина 22,5 мг в базовом клиническом исследовании, достигли кастрационного уровня на 5-й неделе; 99% достигли этого уровня к 28 дню. У подавляющего большинства пациентов уровни тестостерона были ниже 20 нг/дл, хотя полноценное преимущество данных низких уровней тестостерона пока еще не было установлено. Уровень ПСА снизился на 98% в течение шести месяцев.
Все, кроме одного пациента, получавшие полную дозу лейпрорелина 45 мг в базовом клиническом исследовании, достигли кастрационного уровня на 4-й неделе. У подавляющего большинства пациентов уровни тестостерона были ниже 20 нг/дл, хотя полноценное преимущество данных низких уровней тестостерона пока еще не было установлено. Уровень ПСА снизился на 97% в течение шести месяцев.
Долгосрочные исследования показали, что постоянная терапия поддерживает концентрацию тестостерона ниже кастрационного уровня на протяжении до 7 лет и по всей видимости на неопределенный срок.
Фармакокинетика
После первой инъекции через 4-8 часов средний уровень концентрации лейпрорелина (Сmах), определяемой в сыворотке крови, повышается до 25,3 нг/дл, 127 нг/дл и 82 нг/дл при применении лейпрорелина в дозе 7,5 мг, 22,5 мг и 45 мг соответственно.
После первоначального повышения (фаза плато составляет от 2 до 28 дней для дозировки 7,5 мг; от 3 до 84 дней для дозировки 22,5 мг, от 3 до 168 дней для дозировки 45 мг) уровень лейпрорелина в сыворотке оставался относительно стабильным (0,28-1,67 нг/мл для дозировки 7,5 мг и 0,2-2 нг/мл для дозировок 22,5 и 45 мг). Данные о накоплении вещества при повторных инъекциях отсутствуют.
Средний объем распределения лейпрорелина в состоянии равновесия после внутривенного однократного введения у здоровых добровольцев мужского пола составлял 27 литров. Связывание с белками плазмы крови человека в лабораторных условиях колебалось в пределах от 43% до 49%.
При введении 1 мг лейпрорелина ацетата внутривенно здоровым добровольцам мужчинам выяснилось, что при применении двухкамерной модели средний клиренс составил 8,34 л/ч с конечным периодом полувыведения приблизительно 3 часа.
Исследования по выведению препарата Элигард не проводились.
Исследования по лекарственному метаболизму препарата Элигард не проводились.
Элигард Показания к применению
Лечение гормонозависимого распространённого рака предстательной железы и лечения локализованного рака предстательной железы высокого риска и местнораспространенного рака предстательной железы в сочетании с лучевой терапией.
Способ применения Элигард и дозировка
Введение препарата Элигард должно осуществляться под руководством медицинского работника, имеющего соответствующий опыт для оценки эффекта лечения.
Элигард назначают в виде подкожной инъекции один раз в месяц при дозировке 7,5 мг, один раз в три месяца при дозировке 22,5 мг и один раз в шесть месяцев при дозировке 45 мг. Введенный раствор образует депо препарата, обеспечивающее постоянное высвобождение лейпрорелина в течение указанного периода.
Как правило, терапия распространённого рака предстательной железы с использованием Элигарда предусматривает длительное лечение и не должна прекращаться при наступлении улучшения или ремиссии.
Препарат Элигард можно использовать в качестве неоадъювантной или адъювантной терапии в сочетании с лучевой терапией у пациентов с локализованным раком высокого риска и местно-распространённым раком простаты.
Реакцию на лечение препаратом следует контролировать путем наблюдения за клиническими проявлениями болезни и измерения уровня простатспецифического антигена (ПСА) в сыворотке крови. В клинических исследованиях показано, что в большинстве случаев у пациентов без орхидэктомии уровень тестостерона повышается в течение первых трех дней лечения и затем снижается в течение 3-4 недель ниже уровней медицинской кастрации. Кастрационный уровень тестостерона поддерживается при длительном применении лекарственного средства (достигается уровня тестостерона <1%). Если ответ пациента на лечение недостаточный, желательно проверить, достиг ли уровень тестостерона кастрационного уровня или продолжает находиться на нем.
Отсутствие клинической эффективности может наблюдаться при неправильном приготовлении, восстановлении и введении препарата; в случае предполагаемой или известной ошибки необходимо оценить уровни тестостерона.
У пациентов с метастатическим кастрационно-резистентным раком предстательной железы, не подвергавшихся хирургической кастрации и получающих агонисты ГнРГ, такие как лейпрорелин, лечение агонистами ГнРГ может быть продолжено на фоне применения ингибиторов биосинтеза андрогенов или ингибиторов андрогенных рецепторов.
Коррекция доз для особых популяций пациентов
Клинических данных по применению Элигарда у больных с печёночной или почечной недостаточностью нет.
Рекомендации по приготовлению раствора для введения
Важно: При неправильном приготовлении раствора для подкожного введения могут наблюдаться случаи отсутствия клинической эффективности. Перед использованием продукт достают из холодильника и в течение 30 минут выдерживают при комнатной температуре. Сперва подготовьте пациента к введению препарата, а затем приступите к приготовлению раствора в соответствии с ниже представленными рекомендациями.
Важно:
Следующие шаги касаются только дозировок 7,5 мг и 22,5 мг! Шаги для дозировки 45 мг представлены ниже в отдельном разделе.
Шаг 1. Откройте внешнюю упаковку (оторвите фольгу от уголка, место отрыва обозначено) и извлеките содержимое упаковки А (рисунок 1.1) и упаковки Б (рисунок 1.2), положите на стерильную поверхность. Выбросьте пакетики с влагопоглотителем.
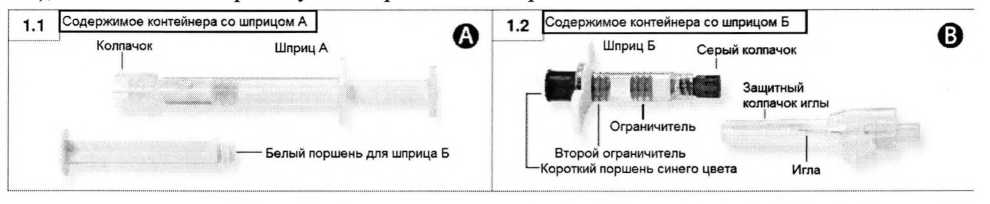
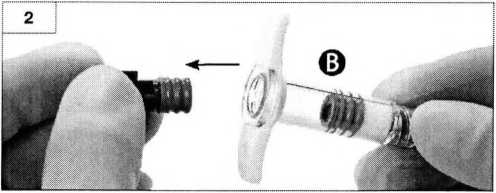
Шаг 2. Выньте из шприца Б (не выкручивать) короткий поршень синего цвета со вторым ограничителем серого цвета (рисунок 2).
Не смешивайте продукт с двумя ограничителями внутри шприца.
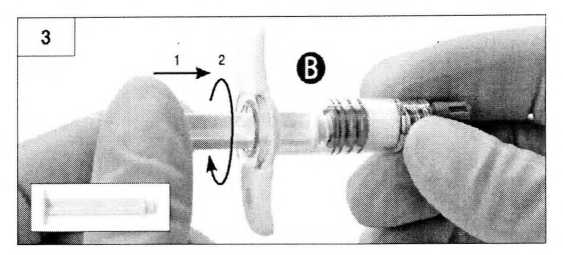
Шаг 3. Аккуратно выньте белый поршень из упаковки со шприцем А и вставьте его в ограничитель серого цвета шприца Б (рисунок 3).
Шаг 4. Снимите серый резиновый колпачок со шприца Б и отложите шприц (рисунок 4).
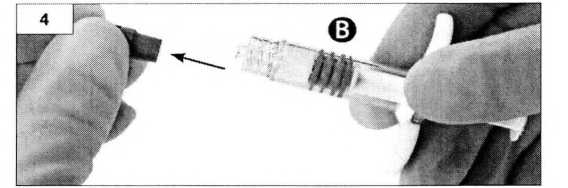
Шаг 5. Держите шприц А вертикально, чтобы избежать протечки, а затем открутите прозрачный колпачок со шприца А (рисунок 5).
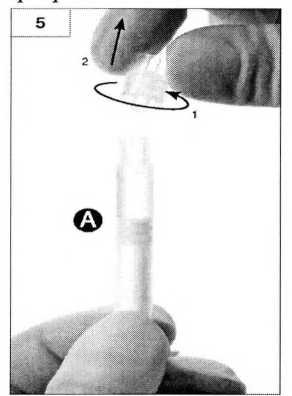
Шаг 6. Соедините два шприца вместе, надавливая и вкручивая шприц Б в шприц А до полной фиксации (рисунки 6а, 6b). Не закручивайте шприцы слишком плотно.
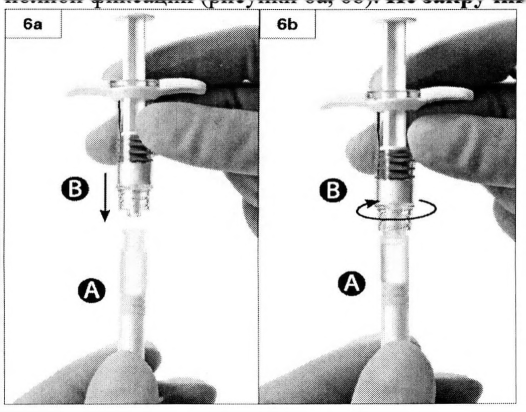
Шаг 7. Переверните соединённые шприцы и держите шприцы вертикально (шприц Бснизу) до момента полного ввода содержимого лейпрорелина ацетата из шприца А в шприц Б (рисунок 7).
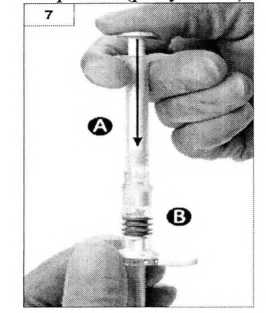
Шаг 8. Тщательно перемешайте содержимое обоих шприцев, держа их в горизонтальном положении и поочередно осторожным движением нажимая на поршень то одного то другого шприца (приблизительно 60 раз, что занимает около 60 секунд), для получения однородного раствора (рисунок 8). Не наклонять шприцы (следует обратить внимание, что это может привести к вытеканию жидкости, поскольку шприцы могут частично открутиться).
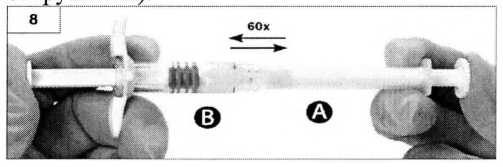
После тщательного смешивания вязкий раствор приобретёт цвет от светло-жёлтого до светло-жёлтого с коричневым оттенком (для дозировки7,5 мг) или от бесцветной до светло-жёлтого цвета (для дозировки 22,5 мг).
Важно: Необходимо использовать раствор сразу после приготовления, поскольку его вязкость со временем увеличивается. Замораживать готовый продукт запрещено.
Помните: Продукт нужно смешивать так, как описано в инструкции; встряхивание не обеспечит надлежащего перемешивания.
Шаг 9. Держите шприцы вертикально, шприц Б - снизу. Шприцы должны быть четко закреплены. Нажимая на поршень шприца А, и слегка подтягивая поршень шприца Б, переместите все содержимое в шприц Б (рисунок 9).
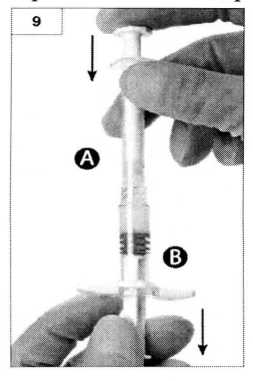
Шаг 10. Открутите шприц А, продолжая нажимать на поршень шприца (рисунок 10). Убедитесь, что содержимое не вытекает из шприца, поскольку в данном случае вы не сможете закрепить иглу надлежащим образом.
Помните: наличие маленьких пузырьков воздуха допустимо. Пожалуйста, не пытайтесь удалять пузырьки из шприца Б на этом этапе, поскольку это может привести к потере продукта.
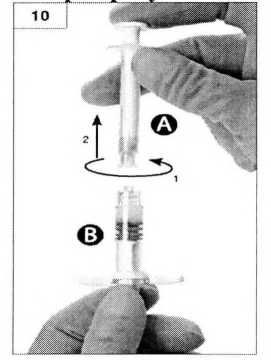
Шаг 11.
•Держите шприц Б вертикально и удерживайте белый поршень во избежание потери препарата
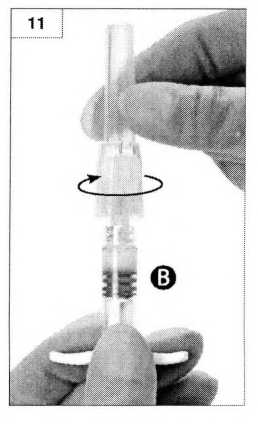
•Откройте упаковку со стерильной иглой (отогнув бумажную этикетку) и извлеките иглу. •Присоедините безопасную иглу к шприцу Б, удерживая шприц и аккуратно поворачивая иглу по часовой стрелке приблизительно на три четверти оборота до полной фиксации (рис. 11).
Не перекручивайте иглу, поскольку это может привести к образованию трещин на переходнике иглы и последующей утечке препарата во время инъекции.
Если переходник иглы сломан, имеет видимые повреждения или протекает, препарат использовать не следует.
Замена повреждённой иглы, а также инъекционное введение препарата недопустимы. Весь препарат необходимо утилизировать с соблюдением мер безопасности.
В случае повреждения переходника иглы необходимо использовать новый препарат.
Шаг 12. Перед инъекцией снимите защитный колпачок с иглы (рисунок 12).
Важно: не используйте иглу до установки на шприц.
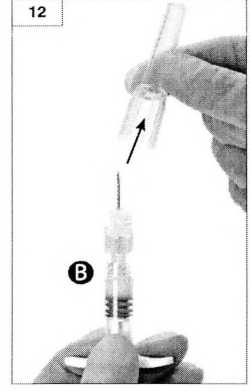
Шаг 13. До начала введения удалите большие пузырьки воздуха из шприца Б. Вводите препарат подкожно. Пожалуйста, убедитесь в том, что введен весь препарат из шприца Б.
Шаг 14. После инъекции, закройте защитную крышку в соответствии с рекомендациями, представленными ниже.
1. Закрытие на плоской поверхности
Нажмите на защитную крышку, рычаг опустите вниз, на плоской поверхности (рисунки 14.1а, b), чтобы закрыть иглу и крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.1b).
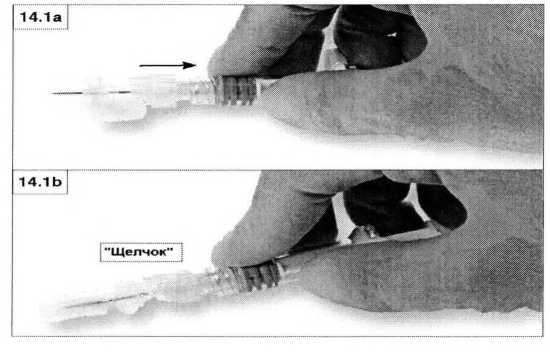
2. Закрытие большим пальцем.
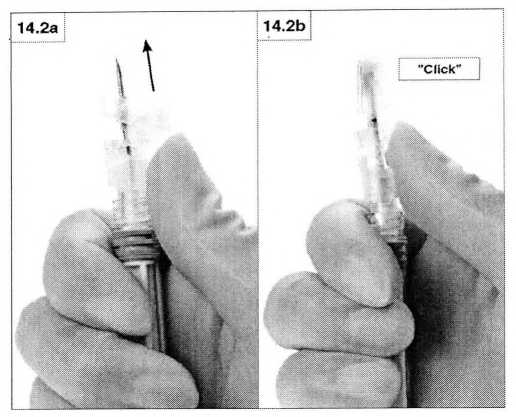
Поместите большой палец на рычаг, слегка нагните его по направлению к кончику иглы (рисунки 14.2а, b), чтобы закрыть иглу и защитную крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.2b).
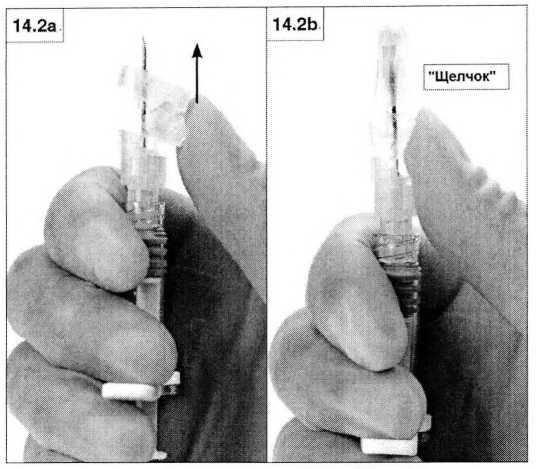
Шаг 15. Как только вы закрыли защитную крышку, немедленно выбросьте иглу ишприц в соответствующий контейнер для острых предметов.
Важно:
Следующие шаги касаются только дозировки 45 мг!
Шаг 1. Откройте внешнюю упаковку (оторвите фольгу от уголка, место отрыва обозначено) и извлеките содержимое упаковки А (рисунок 1.1) и упаковки Б (рисунок 1.2), положите на стерильную поверхность. Выбросьте пакетики с влагопоглотителем.
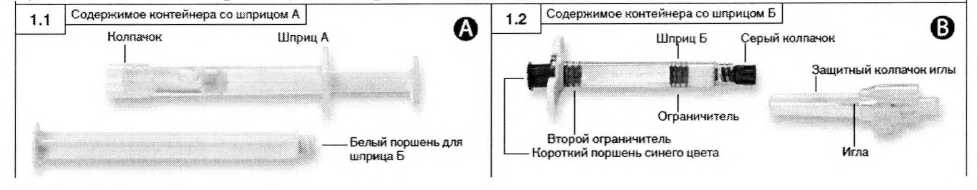
Шаг 2. Выньте из шприца Б (не выкручивать) короткий поршень синего цвета со вторым ограничителем серого цвета (рисунок 2).
Не смешивайте продукт с двумя ограничителями внутри шприца.
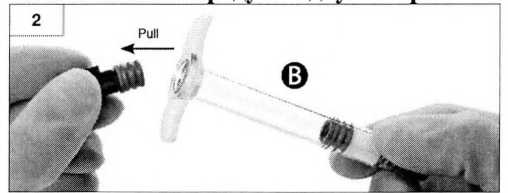
Шаг 3. Аккуратно выньте белый поршень из упаковки со шприцем А и вставьте его в ограничитель серого цвета шприца Б (рисунок 3).
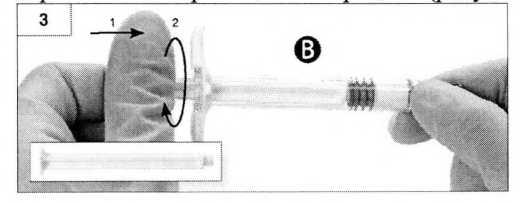
Шаг 4. Снимите серый резиновый колпачок со шприца Б и отложите шприц (рисунок 4).
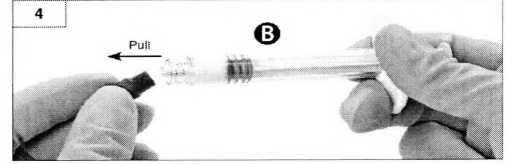
Шаг 5. Держите шприц А вертикально, чтобы избежать протечки, а затем открутите прозрачный колпачок со шприца А (рисунок 5)
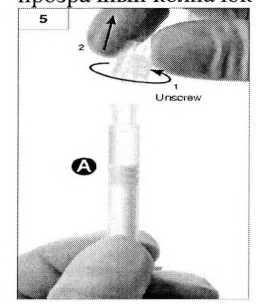
Шаг 6. Соедините два шприца вместе, надавливая и вкручивая шприц Б в шприц А до полной фиксации (рисунки 6а, 6Ь). Не закручивайте шприцы слишком плотно.
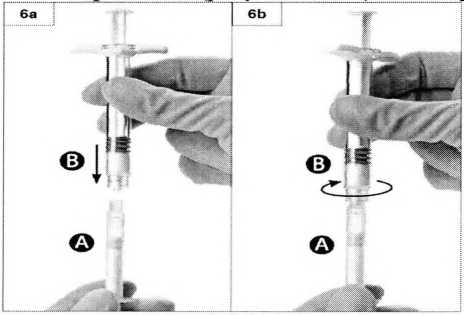
Шаг 7. Переверните соединённые шприцы и держите шприцы вертикально (шприц Б снизу) до момента полного ввода содержимого лейпрорелина ацетата из шприца А в шприц Б (рисунок 7).
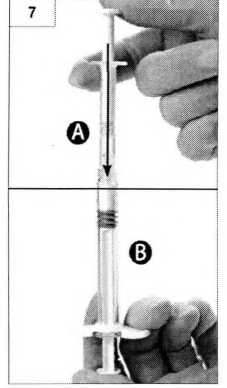
Шаг 8. Тщательно перемешайте содержимое обоих шприцев, держа их в горизонтальном положении и поочередно осторожным движением нажимая на поршень то одного то другого шприца (приблизительно 60 раз, что занимает около 60 секунд), для получения однородного раствора (рисунок 8). Не наклонять шприцы (следует обратить внимание, что это может стать причиной протечки, поскольку шприцы могут частично открутиться).
После тщательного смешивания вязкий раствор приобретёт цвет от бесцветной до светло-жёлтого цвета.
Важно: Необходимо использовать раствор сразу после приготовления, поскольку его вязкость со временем увеличивается. Замораживать Готовый продукт запрещено.
Помните: Продукт нужно смешивать так, как описано в инструкции; встряхивание не обеспечит надлежащего перемешивания.
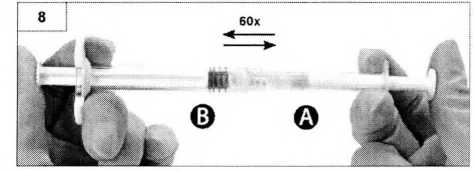
Шаг 9. Держите шприцы вертикально, шприц Б - снизу. Шприцы должны быть четко закреплены. Нажимая на поршень шприца А, и слегка подтягивая поршень шприца Б, переместите все содержимое в шприц Б (рисунок 9).
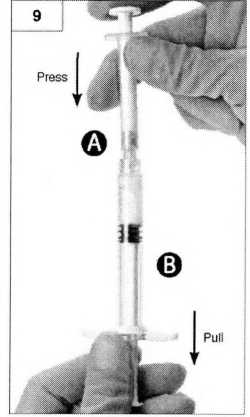
Шаг 10. Открутите шприц А, продолжая нажимать на поршень шприца (рисунок 10). Убедитесь, что содержимое не вытекает из шприца, поскольку вы не сможете закрепить иглу надлежащим образом в случае вытекания.
Помните: наличие маленьких пузырьков воздуха допустимо. Не пытайтесь удалять пузырьки из шприца Б на этом этапе, поскольку это может привести к потере продукта.
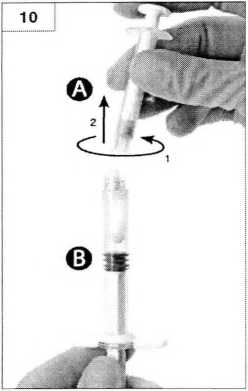
Шаг 11.
Держите шприц Б вертикально и удерживайте белый поршень во избежание потери препарата
Откройте упаковку со стерильной иглой (отогнув бумажную этикетку) и извлеките иглу.
•Присоедините безопасную иглу к шприцу Б, удерживая шприц и аккуратно поворачивая иглу по часовой стрелке приблизительно на три четверти оборота до полной фиксации (рис. 11).
Не перекручивайте иглу, поскольку это может привести к образованию трещин на переходнике иглы и последующей утечке препарата во время инъекции.
Если переходник иглы сломан, имеет видимые повреждения или протекает, препарат использовать не следует.
Замена повреждённой иглы, а также инъекционное введение препарата недопустимы. Весь препарат необходимо утилизировать с соблюдением мер безопасности.
В случае повреждения переходника иглы необходимо использовать новый препарат.
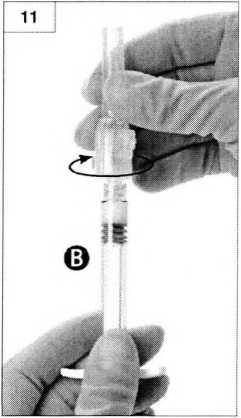
Шаг 12. Перед инъекцией снимите защитный колпачок с иглы (рисунок 12).
Важно: не используйте иглу до установки на шприц.
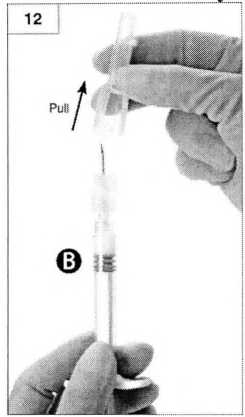
Шаг 13. До начала введения удалите большие пузырьки воздуха из шприца Б. Вводите препарат подкожно. Убедитесь в том, что введен весь препарат из шприца Б.
Шаг 14. После инъекции, закройте защитную крышку в соответствии с рекомендациями, представленными ниже.
1. Закрытие на плоской поверхности
Нажмите на защитную крышку, рычаг опустите вниз, на плоской поверхности (рисунки 14.1а, b), чтобы закрыть иглу и крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.1b).
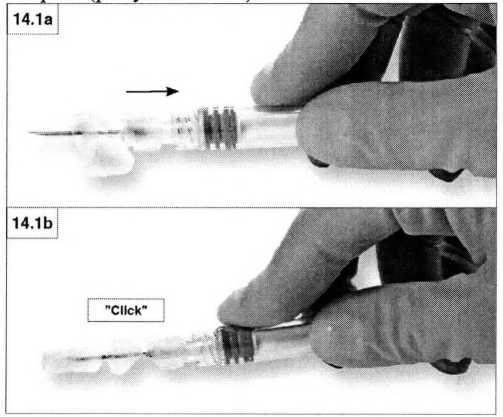
2. Закрытие большим пальцем.
Поместите большой палец на рычаг, слегка нагните его по направлению к кончику иглы (рисунки 14.2а, b), чтобы закрыть иглу и защитную крышку.
Проверьте плотность закрытия (до характерного щелчка). Кончик иглы будет полностью закрыт (рисунок 14.2b).
Шаг 15. Как только вы закрыли защитную крышку, немедленно выбросьте иглу и шприц в соответствующий контейнер для острых предметов.
Информация для работников здравоохранения
Если раствор был приготовлен неправильно, его не следует вводить, поскольку в связи с неправильным приготовлением раствора может наблюдаться отсутствие клинической эффективности.
Побочные действия
Побочные реакции, наблюдаемые при применении Элигарда, в основном обусловлены фармакологическим действием препарата - увеличения и снижение уровней гормона. Наиболее часто сообщалось о чувстве жара/приливов, слабость, тошнота и усталость, и кратковременное местное раздражение в месте инъекции. Чувство жара/приливы встречаются примерно у 58% пациентов.
Нежелательные явления перечислены ниже наблюдались в клинических исследованиях препарата Элигарда у пациентов с распространённым раком предстательной железы. Нежелательные явления классифицированы за частотой встречаемости: очень часто (≥ 1/10), часто (≥ 1/100, < 1/10), нечасто (≥ 1/1 000, но < 1/100), редко (≥ 1/10 000, < 1/1 000) и очень редко (< 1/10 000), частота неизвестна (на основании имеющихся данных оценить невозможно).
| Нежелательные явления в ходе клинических исследований препарата Элигард | |
| Инфекционные и паразитарные заболевания | |
| часто | назофарингит |
| нечасто | инфекция мочевыводящих путей, местная инфекция кожных покровов |
| Нарушения питания и обмена веществ | |
| нечасто | обострение сахарного диабета |
| Психические нарушения | |
| нечасто | нарушения сна, депрессия, снижение либидо |
| Нарушения со стороны нервной системы | |
| нечасто | головокружение, головная боль, гипестезия, бессонница, нарушение вкусовых ощущений, нарушение обоняния, вертиго |
| редко | непроизвольные патологические движения |
| Кардиальные расстройства | |
| неизвестно | удлинение интервала QT (см. раздел «Особые указания», «Взаимодействия с другими лекарственными препаратами и другие формы взаимодействия») |
| Нарушения со стороны сосудистой системы | |
| очень часто | приливы |
| нечасто | гипертензия, гипотония |
| редко | обморок, коллапс |
| Респираторные, торакальные и медиастинальные нарушения | |
| нечасто | ринорея, одышка |
| Нарушения со стороны пищеварительной системы | |
| часто | тошнота, диарея, гастроэнтерит/колит |
| нечасто | запор, сухость во рту, диспепсия, рвота |
| редко | метеоризм, отрыжка |
| Нарушения со стороны кожи и подкожной клетчатки | |
| очень часто | экхимозы, эритема |
| часто | зуд, ночная потливость |
| нечасто | потливость, усиленное потоотделение |
| редко | алопеция, кожный зуд |
| Нарушения со стороны костно-мышечной системы и соединительной ткани | |
| часто | артралгия, фантомная боль, миалгия, дрожь, слабость |
| нечасто | боли в спине, мышечные судороги |
| Нарушения со стороны мочевыделительной системы | |
| часто | нарушение мочеиспускания, затруднения при мочеиспускании, дизурия, ноктурия, олигурия |
| нечасто | спазм детрузора, гематурия, увеличение частоты мочеиспускания, задержка мочеиспускания |
| Нарушения со стороны репродуктивной системы и молочной железы | |
| часто | болезненность молочных желез, тестикулярная артрофия, боль в яичках, гипертрофия молочных желез, эректильная дисфункция, уменьшение размеров полового члена |
| нечасто | гинекомастия, импотенция, тестикулярные нарушения |
| редко | боли в груди |
| Системные нарушения и осложнения в месте введения | |
| очень часто | утомление, жжение в месте введения, парестезия в месте введения |
| часто | недомогание, боль в месте введения, кровоподтек в месте введения, жжение в месте введения |
| нечасто | зуд в месте введения, уплотнение в месте введения, летаргия, болевые ощущения, пирексия |
| редко | образование язвы в месте введения |
| очень редко | некроз в месте введения |
| Нарушения со стороны крови и лимфатической системы | |
| часто | гематологические изменения, анемия |
| Отклонения от нормы, выявленные в лабораторных исследованиях | |
| часто | повышение уровня креатинина фосфокиназы, увеличение времени коагуляции |
| нечасто | увеличение уровня аланинаминотрансферазы, повышение уровня триглицеридов, увеличение протромбинового времени, увеличение веса |
Другие нежелательные явления, которые сообщались при лечении лейпрорелином ацетатом, включают периферические отеки, эмболия легочной артерии, учащенное сердцебиение, боль в мышцах, мышечная слабость, изменение чувствительности кожных покровов, озноб, сыпь, амнезия и расстройства зрения. При продолжительном применении препаратов данного класса отмечали атрофию мышц.
Редко после применения агонистов ГнРГ как длительного, так и короткого действия, сообщалось об инфаркте гипофиза, которая ранее имела место. Также редко сообщались случаи тромбоцитопении и лейкопении. Сообщалось об изменении толерантности к глюкозе.
После введения агониста ГнРГ редко были описаны случаи возникновения судорог (см. раздел «Особые указания»)
Местные побочные реакции, которые возникают после введения Элигард, похожие на местные реакции, которые возникают при подкожном введении. В общем, эти местные побочные реакции, которые происходят после подкожных инъекций, слабые и непродолжительные.
После введения агониста ГнРГ редко были описаны случаи развития анафилактических/анафилактоидных реакций.
Изменения костной ткани
В медицинской литературе сообщалось о снижении плотности костной ткани у мужчин, которым была проведена орхиэктомия или лечившихся аналогами ГнРГ. Вполне вероятно, что длительное лечение лейпрорелином может вызвать рост симптомов остеопороза. По росту риска возникновения переломов - это последствия остеопороза (см. раздел «Особые указания»).
Обострение признаков и симптомов болезни
Лечение лейпрорелином ацетатом может вызывать обострение признаков и симптомов заболевания в течение первых нескольких недель. Могут возникать метастазы в позвоночник и/или закупорка мочевых путей или гематурия, неврологические расстройства, такие как слабость и/или парестезии нижних конечностей или ухудшение мочевых симптомов.
При возникновении у вас каких-либо побочных действий, обратитесь к вашему врачу, аптекарю или медсестре. Это касается любых возможных побочных действий, не указанных в инструкции по медицинскому применению.
Противопоказания Элигард
Повышенная чувствительность к лейпрорелину, другим агонистам ГнРГ или к любому вспомогательному веществу, входящему в состав лекарственной формы.
Хирургическая кастрация (как и другие агонисты ГнРГ, Элигард не вызывает дальнейшего уменьшения уровней тестостерона в сыворотке крови после хирургической кастрации).
Противопоказан женщинам и детям.
В качестве единственного лечения у пациентов с раком предстательной железы со сдавлением спинного мозга или наличием метастазов в позвоночник (см. раздел «Особые указания»).
Передозировка
Данных относительно передозировки у людей не имеется. В случае передозировки больному следует назначить симптоматическое лечение.
Меры предосторожности
Правильное восстановление препарата: При неправильном восстановлении препарата могут наблюдаться случаи отсутствия клинической эффективности. Инструкции по приготовлению и введению препарата и информация об оценке концентраций тестостерона в сыворотке крови в случае предполагаемых или известных ошибок при смешивании представлены в разделах «Способ применения и дозы» и «Рекомендации по приготовлению раствора для введения».
Антиандрогенная терапия может удлинять интервал ОТ:
Перед началом применения препарата врачи должны оценивать соотношение польза-риск, включая возможность возникновения двунаправленной желудочковой тахикардии, у пациентов с удлинением интервала QT в анамнезе или соответствующими факторами риска, а также у пациентов, принимающих препараты, которые могут удлинять интервал QT (см. раздел «Взаимодействие с другими лекарственными препаратами и другие формы взаимодействия»).
Сердечно-сосудистые заболевания: Повышенный риск развития инфаркта миокарда, внезапной сердечной смерти и инсульта были зарегистрированы в связи с использованием агонистов ГнРГ у мужчин. Риск представляется низким на основе данных отношения шансов и должен быть тщательно оценен наряду с сердечно-сосудистыми факторами риска при выборе лечения пациентов с раком предстательной железы. Пациенты, получающие лечение агонистом ГнРГ, должны находиться под наблюдением для выявления симптомов и признаков, указывающих на развитие сердечно-сосудистых заболеваний, и получать лечение в соответствии с современной клинической практикой.
Временное повышение уровня тестостерона: Элигард, как и другие препараты-агонисты ГнРГ, в течение первой недели лечения вызывает кратковременное повышение концентрации тестостерона, дигидротестостерона и кислой фосфатазы в сыворотке крови, в связи с чем у пациентов могут усилиться симптомы или возникнуть новые, такие как боль в костях, неврологические расстройства, гематурия, обструкция мочеточника или инфравезикальная обструкция (см. раздел «Побочное действие»). Эти симптомы обычно проходят при продолжении терапии.
Дополнительное назначение соответствующего антиандрогена за три дня до начала терапии Элигардом и продолжение его приёма в течение первых двух или трёх недель лечения предупреждает последствия первоначального повышения уровня тестостерона. После выполнения кастрации хирургическим путём применение Элигарда не приводит к дальнейшему снижению тестостерона в сыворотке крови.
При применении агонистов ГнРГ сообщалось также о случаях обструкции мочеточника компрессии спинного мозга, что может приводить к параличу с наличием или отсутствием фатальных осложнений. При необходимости следует проводить стандартное лечение этих осложнений.
Изменения плотности костей: Имеются сообщения о снижении плотности костной ткани у мужчин, которым проводилась орхиэктомия или леченных агонистом ГнРГ (см. раздел «Побочное действие»).
Антиандрогенная терапия значительно повышает риск переломов костей в результате возникновения остеопороза. По этому вопросу имеются только ограниченные данные. Переломы вследствие остеопороза наблюдались у 5% пациентов через 22 месяца антиандрогенной терапии лекарственными средствами и у 4% пациентов через 5-10 лет лечения. Риск переломов вследствие остеопороза, как правило, выше риска патологических переломов.
Помимо продолжительного дефицита тестостерона на развитие остеопороза может влиять преклонный возраст, курение, потребление алкоголя, лишний вес и недостаточные физические нагрузки.
Гипофизарная апоплексия: В течение постмаркетингового надзора редко после применения ГнРГ-агонистов отмечались случаи апоплексии гипофиза (клинического синдрома второго по сложности после инфаркта гипофиза), что в большинстве случаев возникали через 2 недели после применения первой дозы, у некоторых пациентов - в течение первого часа.
В данном случае, гипофизарная апоплексия проявляется в виде таких симптомов как головная боль, рвота, нарушение зрения, офтальмоплегия, изменение психического состояния и сердечнососудистой недостаточности и требует немедленного оказания медицинской помощи.
Гипергликемия и сахарный диабет: Гипергликемия и повышенный риск развития диабета были зарегистрированы у мужчин, получающих лечение агонистами ГнРГ. Гипергликемия может быть признаком развития сахарного диабета или ухудшения контроля уровня глюкозы в крови у пациентов с сахарным диабетом. Необходим периодический мониторинг уровня глюкозы и/или гликозилированного гемоглобина (HbAlc) в крови у пациентов, получающих лечение агонистами ГнРГ, и лечение гипергликемии или сахарного диабета в соответствии с современной практикой.
Судороги: В течение пострегистрационного периода поступали сообщения о возникновении судорог у пациентов, получавших лечение лейпрорелина ацетатом при наличии или в отсутствие в анамнезе предрасполагающих факторов. При судорогах следует проводить лечение, основанное на современных клинических рекомендациях.
Другие явления: При применении агонистов ГнРГ сообщалось также о случаях возникновения обструкции мочевыводящих путей и компрессии спинного мозга, что может привести к параличу как с развитием осложнений со смертельным исходом, так и без них. В случае компрессии спинного мозга или развитии нарушения функции почек следует назначать стандартную терапию этих осложнений.
За пациентами с метастазами в позвоночник и/или головной мозг, а также за пациентами с обструкцией мочевых путей должно вестись тщательное наблюдение в течение первых нескольких недель лечения.
Дети
Безопасность и эффективность у детей в возрасте до 18 лет не установлена.
Применение в период беременности и кормления грудью
Противопоказано.
Способность влиять на скорость реакции при управлении транспортом
Не было проведено исследований влияния лекарственного препарата на способность управлять автомобилем и работе с механизмами. Некоторые побочные действия препарата, такие как повышенная усталость, головокружение, нарушения зрения, могут отрицательно влиять на способность к управлению автомобилем и выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Взаимодействие с другими лекарственными средствами
Исследований по изучению фармакокинетического взаимодействия препарата Элигард с другими препаратами не проводилось. О взаимодействии Элигарда с другими лекарственными препаратами не сообщалось.
В связи с тем, что андрогенная депривация может удлинять интервал QT, должно быть тщательно взвешено одновременное применение препарата Элигард с другими препаратами, удлиняющими интервал QT, или препаратами, способными вызывать желудочковую тахикардию типа «пируэт», такими как антиаритмические препараты класса IA (например, хинидин, дизопирамид) или класса III (например, амиодарон, соталол, дофетилид, ибутилид), метадон, моксифлоксацин, нейролептики и др. (см. раздел «Особые указания»).
Условия и срок хранения Элигард
Список Б.
При температуре от 2°С до 8°С в оригинальной упаковке.
Хранить в недоступном для детей месте.
2 года.
После извлечения из холодильника препарат может храниться в оригинальной упаковке при комнатной температуре (не выше 25°С) до 4 недель.
После первого вскрытия кюветы, необходимо сразу же приготовить раствор и ввести его пациенту.
Не использовать препарат по истечении срока годности, указанного на упаковке.
Дата истечения срока годности - последний день текущего месяца.
Упаковка
Два стерильных заранее наполненных шприца из полипропилена или сополимера циклического олефина, в одном (шприц Б) содержится лиофилизат лейпрорелина ацетата (10,6 мг для дозировки 7,5 мг; 29,2 мг для дозировки 22,5 мг; 59,2 мг для дозировки 45 мг), в другом (шприц А) - растворитель (343 мг для дозировки 7,5 мг; 457 мг для дозировки 22,5 мг; 434 мг для дозировки 45 мг). Содержимое двух шприцев представляет собой комбинированную систему.
Шприц А вместе с поршнем для шприца Б и пакетиком с влагопоглотителем помещают в полиэфирную контурную упаковку, покрытую алюминиевой ламинированной фольгой. Контурная упаковка снабжена дополнительной внутренней прозрачной полиэфирной вкладкой, которая обеспечивает надежную фиксацию шприца А и поршня для шприца Б в упаковке.
Шприц Б вместе с иглой инъекционной 0,9 × 12,3 мм «monoject» (№ 20 для дозировок 7,5 мг и 22,5 мг; № 18 для дозировки 45 мг) в пенале из прозрачного пластика и пакетик с влагопоглотителем помещают в полиэфирную контурную упаковку, покрытую алюминиевой ламинированной фольгой. Контурная упаковка снабжена дополнительной внутренней прозрачной полиэфирной вкладкой, которая обеспечивает надежную фиксацию шприца Б и иглы инъекционной в упаковке.
По одной контурной упаковке со шприцом А в комплекте с поршнем для шприца Б и пакетиком с влагопоглотителем и по одной контурной упаковке со шприцом Б в комплекте с иглой инъекционной и пакетиком с влагопоглотителем вкладывают вместе с инструкцией в картонную пачку.
Правила отпуска
По рецепту.
Информация о производителе
Владелец регистрационного удостоверения
«Астеллас Фарма Юроп Б.В.», Нидерланды.
Производитель
Шприц А:
«Толмар Инк.»,
701 Сентре Авеню
Фт. Коллинс СО 80526, США.
Шприц Б:
«Толмар Инк.»,
701 Сентре Авеню
Фт. Коллинс СО 80526, США
или
«Кангене биоФарма Инк.»,
1111 Саут Пака Стрит
Балтимор Мериленд 21230, США.
Упаковано
«Астеллас Фарма Юроп Б.В.»,
Хогемаат 2, 7942 JG Меппель, Нидерланды.
Выпускающий контроль качества
«Астеллас Фарма Юроп Б.В.»,
Хогемаат 2, 7942 JG Меппель, Нидерланды.
Претензии по качеству принимаются ПредставительствомвМоскве
Московское Представительство «Астеллас Фарма Юроп Б.В.», Нидерланды
109147 Москва, Марксистская ул. 16, «Мосаларко Плаза-1» бизнес-центр, 3 этаж.
Тел.: +7(495) 737 07 55; +7(495) 737 07 56.
Факс: +7 (495) 737 07 67.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Элигард только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание! Эта инструкция по применению лекарственного средства является официальной инструкцией производителя Tolmar Inc..
Авторское право:
- Tolmar Inc.
- https://www.rceth.by - Государственный реестр ЛС Республики Беларусь
| Тип данных | Сведения из реестра |
| Торговое наименование: | Элигард |
| Форма выпуска: | лиофилизат для приготовления раствора для подкожного введения 7,5 мг, 22,5 мг, 45 мг в шприце в комплекте с растворителем в шприце в упаковке №1 |
| Международное наименование: | Leuprorelin |
| Производитель: | Tolmar Inc., США |
| Заявитель: | Astellas Pharma Europe B.V., Нидерланды |
| Номер регистрации: | 10109/13/15/15/19/19/20 |
| Дата регистрации: | 29.04.2019 |
| Срок действия: | бессрочно |
| Дата переоформления: | 09.09.2020 |
| Тип: | Лекарственное средство |
| Оригинальное: | оригинальное |
| Состав лекарственного средства: | Leuprorelin |
| Код АТХ: | L02AE02 |
| Производитель готовой лекарственной формы: | Tolmar Inc., США |
| Производитель, осуществляющий фасовку/упаковку: | Tolmar Inc., США |
| Контроль качества: | |
| Выдача разрешения на выпуск лекарственного средства: | Astellas Pharma Europe B.V., Нидерланды |
| Другие участники производства: | производитель растворителя - Tolmar Inc., США |
| Заявленная цена: | 118,00EUR |
| Порядок отпуска: | по рецепту |
| Список хранения: | |
| Срок годности лекарства: | 2 года |
| Нормативная документация: | НД РБ 8719-2019 |
| Дата утверждения нормативной документации: | 29 апреля 2019 г. 0:00 |
| Срок действия нормативной документации: | |
| Изменение в нормативной документации: | изменение по разделу "Производитель" (исключение Cangene bioPharma LLC, США) (пр. №1259 от 23.10.2019) |
| Номер разрешения НД: | 10187 |
| Код АТХ | Название группы |
| L | Противоопухолевые препараты и иммуномодуляторы |
| L02 | Противоопухолевые гормональные препараты |
| L02A | Гормоны и их производные |
| L02AE | Аналоги гонадотропин-рилизинг гормона |
| L02AE02 | Leuprorelin |