- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Мидазолам Калцекс инструкция по применению
Официальная инструкция лекарственного препарата Мидазолам Калцекс раствор 5 мг/мл. Описание и применение Midazolam Kaltseks, аналоги и отзывы. Инструкция Мидазолам Калцекс раствор утвержденная компанией производителем.
Состав
действующее вещество: midazolam;
1 мл содержит мидазолама 5 мг.
вспомогательные вещества : соляная кислота, натрия хлорид, натрия гидроксид, вода для инъекций.
Лекарственная форма
Раствор для инъекций.
Основные физико-химические свойства: прозрачная бесцветная жидкость.
Фармакологическая группа
Снотворные и седативные препараты, производные бензодиазепина.
Код АТХ N05С D08.
Фармакологические свойства
Фармакологические.
Мидазолам является производным группы имидазобензодиазепинив. Свободная основа представляет собой липофильную вещество и имеет низкую растворимость в воде.
Основной азот в положении 2 имидазобензодиазепинового кольца позволяет мидазолама образовывать водорастворимые соли с кислотами, образуя стабильный и хорошо переносимый раствор для инъекций или инфузий.
Фармакологическое действие мидазолама характеризуется короткой продолжительностью через быстрое метаболическое преобразование в течение короткого периода времени. Мидазолам обладает мощным успокаивающим и снотворным эффектом. Кроме того, он обладает анксиолитическим, противосудорожным и миорелаксирующим эффектом. После внутримышечного или внутривенного введения возникает кратковременная антероградная амнезия (пациент не помнит о событиях, происходивших в период максимального действия активного вещества).
Фармакокинетика.
Всасывания после инъекции
Мидазолам быстро и полностью всасывается из мышечной ткани. Максимальная концентрация в плазме (max) достигается в течение 30 минут. Биодоступность после введения составляет более 90%.
Всасывания после ректального введения
Мидазолам быстро всасывается после ректального введения. С max достигается в течение примерно 30 минут. Биодоступность составляет примерно 50%.
распределение
После введения мидазолама на кривой «концентрация-время» в плазме крови (AUC) образуются одна или две отдельные фазы распределения. Объем стационарного распределения составляет 0,7-1,2 л / кг. 96-98% мидазолама связывается с белками плазмы крови, в основном с альбумином. Мидазолам медленно и в небольших количествах попадает в спинномозговую жидкость.
Установлено, что мидазолам медленно проникает через плацентарный барьер и попадает в кровоток плода человека. Мидазолам был обнаружен в грудном молоке человека в небольших количествах.
Метаболизм
Мидазолам почти полностью устраняется путем биотрансформации. Было подсчитано, что доля дозы метаболизируется через печень, составляет 30-60%. Мидазолам гидроксилируется изоферментом 3A4 цитохрома P450. Основным метаболитом в плазме и в моче альфа-гидроксимидазолам. Концентрация альфа-гидроксимидазоламу в плазме составляет 12% от исходного соединения. Альфа-гидроксимидазолам фармакологически активным, но вносит минимальный (около 10%) вклад в эффекты введенного мидазолама.
Выведение
У здоровых добровольцев период полувыведения мидазолама составляет от 1,5 до 2,5 часов.
Клиренс из плазмы составляет от 300 до 500 мл / мин. Мидазолам в основном выводится почками (60-80% введенной дозы) в виде альфа-гидроксимидазоламу, конъюгированного с глюкуронидом. Менее 1% выводится в виде неизмененного активного вещества в мочу. Период полувыведения альфа-гидроксимидазоламу составляет менее 1:00. Кинетика элиминации мидазолама, введенного в виде инфузии, не отличается от таковой при болюсной инъекции.
Особые группы пациентов
Пациенты пожилого возраста
У взрослых в возрасте от 60 лет период полувыведения может быть увеличен до четырех раз.
педиатрическая популяция
В то время как скорость всасывания мидазолама, введенного ректально, одинакова у детей и у взрослых, биодоступность у детей снижена (5-18%). По сравнению со взрослыми, период полувыведения после внутривенного и ректального введения короче (1-1,5 часа) в возрасте от 3 до 10 лет. Эта разница соответствует повышенному метаболическом клиренса у детей.
новорожденные
У новорожденных период полувыведения составляет в среднем 6-12 часов, вероятно, из-за незрелости печени и уменьшение клиренса (см. Раздел «Особенности применения»).
Пациенты с избыточной массой тела
Период полувыведения у пациентов с избыточной массой тела выше, чем у пациентов с нормальной массой тела (5,9 против 2,3 часа). Это связано с увеличением объема распределения примерно на 50% с поправкой на общую массу тела. Клиренс существенно не отличается у пациентов с нормальной и избыточной массой тела.
Пациенты с печеночной недостаточностью
Период полувыведения у пациентов с циррозом может удлиняться, а клиренс уменьшаться по сравнению с таким у здоровых добровольцев (см. Раздел «Особенности применения»).
Пациенты с почечной недостаточностью
Период полувыведения у пациентов с хронической почечной недостаточностью аналогичен таковому у здоровых добровольцев.
Критически больные пациенты.
Период полувыведения мидазолама увеличивается до шести раз у пациентов, находящихся в критическом состоянии.
Пациенты с сердечной недостаточностью.
Период полувыведения у пациентов с застойной сердечной недостаточностью дольше, чем у здоровых добровольцев (см. Раздел «Особенности применения»).
Клинические характеристики
Мидазолам Калцекс Показания
Мидазолам - снотворное короткого действия со следующими показаниями к применению:
взрослые
- седация с сохранением сознания перед или во время диагностических или терапевтических процедур с применением местной анестезии или без нее;
- анестезия (премедикация перед введением наркоза, индукция наркоза, в качестве седативного компонента в поддержке анестезии)
- седация в отделении интенсивной терапии.
- дети:
- седация с сохранением сознания перед или во время диагностических или терапевтических процедур с применением местной анестезии или без нее;
- анестезия (премедикация перед введением наркоза)
- седация в отделении интенсивной терапии.
Противопоказания
Повышенная чувствительность к мидазолама, бензодиазепинов или к вспомогательному веществу препарата.
Седация с сохранением сознания у пациентов с тяжелой или острой дыхательной недостаточностью.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
фармакокинетические взаимодействия
Мидазолам метаболизируется с помощью CYP3A4. Ингибиторы и индукторы CYP3A могут увеличивать и уменьшать концентрацию препарата в плазме и, следовательно, действие мидазолама, которая требует соответствующей коррекции дозы.
Фармакокинетические взаимодействия с ингибиторами или индукторами CYP3A4 более выражены при пероральном применении по сравнению с внутривенным введением мидазолама в частности, поскольку CYP3A4 также существует в верхних отделах желудочно-кишечного тракта. Это связано с тем, что после перорального применения будут изменены и системный клиренс, и доступность, в то время как после парентерального введения будет изменен только системный клиренс. После однократного введения мидазолама изменение максимального клинического эффекта из-за подавления CYP3A4 будет незначительной, в то время как продолжительность эффекта может быть увеличена. Однако после длительного применения мидазолама как величина, так и продолжительность эффекта будут увеличены при подавлении CYP3A4.
Нет доступных исследований о влиянии модуляции CYP3A4 на фармакокинетику мидазолама после ректального и внутримышечного введения. Ожидается, что эти взаимодействия будут менее выражены после ректального, чем после перорального применения, поскольку желудочно-кишечный тракт не будет привлечен, тогда как после введения эффекты модуляции CYP3A4 не должны существенно отличаться от тех, которые наблюдаются при внутривенном введении.
Поэтому рекомендуется тщательно следить за клиническим эффектом и показателями жизненно важных функций при применении мидазолама, учитывая, что клинический эффект мидазолама может быть более сильным и длиться дольше после одновременного введения ингибитора CYP3A4, даже если его вводят только один раз. В частности, введение высоких доз или длительных инфузий мидазолама пациентам, которые получают сильные ингибиторы CYP3A4 (например, во время интенсивной терапии), может вызвать длительный снотворный эффект, отсроченный выход из анестезии и угнетение дыхания, требует коррекции дозы.
При индукции CYP3A4 следует учитывать, что индукционной процесса нужно несколько дней для достижения максимального эффекта, а также несколько дней для его исчезновения. В отличие от лечения индуктором течение нескольких дней, кратковременное лечение приводит к менее выраженных взаимодействий с мидазоламом. Однако для сильных индукторов нельзя исключать значительную индукцию даже после кратковременного лечения. Мидазолам, как известно, не изменяет фармакокинетику других лекарственных средств.
Препараты, ингибирующие CYP3A
Противогрибковые средства группы азолов
• Кетоконазол увеличивает концентрацию внутривенно введенного мидазолама в плазме в 5 раз, в то время как конечный период полувыведения увеличивался примерно в 3 раза. Если парентеральный мидазолам вводится совместно с сильным ингибитором CYP3A, кетоконазолом, это следует делать в отделении интенсивной терапии или в аналогичных условиях, чтобы обеспечить тщательный клинический мониторинг и соответствующее лечение в случае угнетения дыхания и / или длительного седативного эффекта. Следует рассмотреть возможность поэтапного введения дозы или коррекции дозы, особенно если вводится более одного внутривенной дозы мидазолама. Такая рекомендация может применяться и к другим противогрибковым препаратам группы азолов (см. Далее), поскольку сообщалось о повышенной седативное действие внутривенно введенного мидазолама, хотя и в меньшей степени.
• Вориконазол повышает концентрацию внутривенно введенного мидазолама в плазме в 3 раза, в то время как период полувыведения также увеличивался примерно в 3 раза.
• флуконазол и итраконазол увеличивают концентрацию внутривенно введенного мидазолама в плазме в 2-3 раза, что связано с увеличением конечного периода полувыведения в 2,4 раза для итраконазола и в 1,5 раза для флуконазола.
• позаконазол увеличивает концентрацию внутривенно введенного мидазолама плазме крови в 2 раза.
Следует учитывать, что после перорального применения мидазолама его влияние будет значительно выше, чем влияние этих препаратов, особенно с кетоконазолом, итраконазолом и вориконазолом.
Мидазолам в ампулах не показан для перорального применения.
макролидные антибиотики
• Эритромицин увеличивает концентрацию внутривенно введенного мидазолама в плазме крови в 1,6-2 раза, что связано с увеличением конечного периода полувыведения мидазолама в 1,5-1,8 раза.
• Кларитромицин увеличивает концентрацию мидазолама в плазме до 2,5 раза, а конечный период полувыведения был увеличен в 1,5-2 раза.
Дополнительная информация по пероральной формы мидазолама
• Рокситромицин: хотя нет данных о влиянии рокситромицину на внутривенно введен мидазолам, слабое влияние на конечный период полувыведения пероральной таблетки мидазолама (увеличение примерно на 30%) указывает на то, что возможен незначительный влияние рокситромицину на внутривенно введен мидазолам.
Ингибиторы протеазы ВИЧ
• Саквинавир и другие ингибиторы протеазы ВИЧ: совместное применение с ингибиторами протеазы может вызвать значительное увеличение концентрации мидазолама. Совместное применение усиленного ритонавиром лопинавира увеличивает концентрацию внутривенно введенного мидазолама в плазме в 5,4 раза, что связано с аналогичным увеличением конечного периода полувыведения. Если парентеральный мидазолам вводят вместе с ингибиторами протеазы ВИЧ, параметры лечения должны соответствовать описанию в вышеприведенном разделе для противогрибковых средств группы азолов, кетоконазола.
Дополнительная информация по пероральной формы мидазолама
На основании данных о других ингибиторы CYP3A4 ожидается, что концентрация мидазолама в плазме будет значительно выше при пероральном приеме мидазолама. Поэтому ингибиторы протеазы не следует вводить одновременно с пероральным мидазоламом.
Блокаторы кальциевых каналов
• Дилтиазем: введение однократной дозы дилтиазема увеличивает концентрацию внутривенно введенного мидазолама в плазме примерно на 25%, а конечный период полувыведения на 43%.
Дополнительная информация по пероральной формы мидазолама
• Верапамил / дилтиазем увеличивает концентрацию перорального мидазолама в плазме в 3 и 4 раза соответственно. Конечный период полувыведения мидазолама увеличивается на 41% и 49% соответственно.
Другие лекарственные средства / фитопрепараты.
• Аторвастатин увеличивает концентрацию внутривенно введенного мидазолама в плазме в 1,4 раза по сравнению с контрольной группой.
Дополнительная информация по пероральной формы мидазолама
• Нефазодон увеличивает концентрацию перорального мидазолама в плазме в 4,6 раза, а конечный период полувыведения в 1,6 раза.
• Апрепитант увеличивает концентрацию мидазолама в плазме в зависимости от дозы (в 3,3 раза при дозе 80 мг в сутки), а конечный период полувыведения в 2 раза.
Препараты индуцируют CYP3A
• Рифампицин снижал концентрацию внутривенно введенного мидазолама в плазме крови на 60% после приема рифампицина в дозе 600 мг / сут в течение 7 дней. Конечный период полувыведения был укорочен примерно на 50-60%.
Дополнительная информация по пероральной формы мидазолама
• Рифампицин снижал концентрацию перорально введенного мидазолама на 96% у здоровых добровольцев и его психомоторные эффекты почти полностью терялись.
• Карбамазепин / фенитоин: при применении повторных доз карбамазепина или фенитоина снижалась концентрация перорально введенного мидазолама в плазме до 90%, а конечный период полувыведения был сокращен на 60%.
• Эфавиренц: 5-кратное увеличение соотношения альфа-гидроксимидазоламу, произведенного с помощью CYP3A4, и мидазолама подтверждает его индуцирующее действие на CYP3A4.
Фитопрепараты и продукты питания
Зверобой уменьшает концентрацию мидазолама в плазме примерно на 20-40%, что связано с сокращением конечного периода полувыведения примерно на 15-17%. В зависимости от конкретного экстракта зверобоя эффект индукции CYP3A4 может варьировать.
фармакодинамические взаимодействия
Совместное применение мидазолама с другими седативными / снотворными средствами и средствами, угнетающими ЦНС (включая алкоголь), может привести к усилению седативного и угнетение дыхания. К ним относятся производные опиатов (при их приеме в качестве анальгетиков, противокашлевых средств или средств заместительной терапии), антипсихотические средства, другие бензодиазепины, которые применяются как анксиолитики или снотворные средства, фенобарбитал, пропофол, кетамин, этомидат, антидепрессанты с седативным действием, H1-антигистаминные средства и антигипертензивные средства центрального действия.
Алкоголь может значительно усиливать седативное действие мидазолама. При применении мидазолама запрещено употребление алкоголя (см. Раздел «Особенности применения»).
Мидазолам снижает минимальную альвеолярную концентрацию ингаляционных анестетиков.
Особенности применения
Мидазолам должны назначать только опытные врачи в условиях, полностью оборудованных для мониторинга и поддержки дыхательной и сердечно-сосудистой функции, или лица, специально обученные распознаванию и лечению побочных реакций, включая реанимацию. В редких случаях сообщалось о серьезных Кардиореспираторной побочные реакции, включая угнетение дыхания, апноэ, остановку дыхания и / или остановку сердца. Такие опасные для жизни осложнения чаще возникают при введении инъекции очень быстро или при введении высокой дозы (см. Раздел «Побочные реакции»).
Особая осторожность необходима при седации с сохранением сознания у пациентов с нарушениями дыхательной функции.
Дети до 6 месяцев особенно склонны к развитию обструкции дыхательных путей и гиповентиляции, поэтому важно титровать дозу с небольшими приращениями клиническому эффекту и тщательно контролировать частоту дыхания и насыщения кислородом. После применения мидазолама как премедикации пациент должен находиться под тщательным наблюдением, поскольку чувствительность может быть различной и могут возникнуть симптомы передозировки.
Особая осторожность требуется при назначении мидазолама пациентам с высокой степенью риска:
• взрослые пациенты в возрасте от 60 лет
• хронически больные или ослабленные пациенты, например
- пациенты с хронической дыхательной недостаточностью
- пациенты с хронической почечной недостаточностью, нарушениями функции печени или сердца,
- педиатрические пациенты, особенно с сердечно-сосудистой нестабильностью.
Более низкие дозы следует назначать пациентам с высокой степенью риска (см. Раздел «Способ применения и дозы»), пациентов следует постоянно наблюдать на предмет ранних признаков изменения жизненно важных функций.
Как и при применении любого лекарственного средства, обладающего свойствами, которые подавляют ЦНС и / или миорелаксирующее свойствами, при применении мидазолама пациентам с myasthenia gravis нужно быть особенно осторожными.
толерантность
Сообщалось о некоторой потере эффективности при длительном применении мидазолама для седации в отделении интенсивной терапии.
зависимость
Когда мидазолам применяют при длительной седации в интенсивной терапии, следует учитывать возможное развитие физической зависимости. Риск развития зависимости увеличивается с увеличением дозы и продолжительности лечения; он также выше у пациентов с злоупотребление алкоголем и / или лекарственными средствами в анамнезе (см. раздел «Побочные реакции»).
Абстинентный синдром
Физическая зависимость может развиться при длительном лечении мидазоламом в отделениях интенсивной терапии. Итак, внезапное прекращение лечения приводит к абстинентного синдрома. Могут возникнуть такие симптомы: головная боль, мышечная боль, тревожность, напряжение, беспокойство, растерянность, раздражительность, рикошетной бессонница, изменение настроения, галлюцинации и судороги. Поскольку риск развития симптомов отмены после внезапного прекращения лечения выше, рекомендуется постепенное снижение дозы.
амнезия
Мидазолам вызывает антероградной амнезию (в некоторых ситуациях этот эффект очень желателен, прежде всего до и во время хирургических и диагностических процедур), продолжительность которой непосредственно связана с введенной дозой. Длительная амнезия может вызвать проблемы у амбулаторных больных, которых собираются выписывать после процедуры. После парентерального введения мидазолама пациенты могут быть выписаны из больницы или отправлены в консультационную комнату только при наличии сопровождающего лица.
парадоксальные реакции
При применении мидазолама зафиксировано парадоксальные реакции, такие как возбуждение, непроизвольные движения (включая тонические / клонические судороги и тремор), гиперактивность, враждебность, приступы ярости, агрессивность, пароксизмальная возбуждения и угроза насилия. Такие реакции могут возникать при застосовання высоких доз и / или при быстром введении препарата. Такие реакции более распространены у детей и пожилых пациентов.
Изменение элиминации мидазолама
Изменено вывода мидазолама может быть вызвано соединениями, которые ингибируют или индуцируют изофермент CYP3A4, поэтому дозу мидазолама, возможно, необходимо соответствующим образом скорректировать (см. Раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
Время элиминации мидазолама также может быть увеличено у пациентов с дисфункцией печени и низким сердечным выбросом, а также у новорожденных (см. Раздел «Фармакокинетика»).
Недоношенные дети и новорожденные
-За повышенного риска развития апноэ следует соблюдать осторожность при проведении седации у недоношенных и бывших недоношенных детей. Следует тщательно следить за частотой дыхания и за насыщением кислородом. У новорожденных следует избегать быстрой инъекции. Новорожденные имеют незрелые органы и / или пониженную функцию органов, поэтому более чувствительны к выраженным и / или длительных эффектов мидазолама на дыхательную функцию. Неблагоприятные гемодинамические реакции были зарегистрированы у детей с сердечно-сосудистой нестабильностью; у таких пациентов следует избегать быстрого введения.
Педиатрические пациенты в возрасте до 6 месяцев
Для этих пациентов мидазолам показан для седации только в отделении интенсивной терапии. Дети до 6 месяцев особенно склонны к развитию обструкции дыхательных путей и гиповентиляции. Поэтому нужно титрования дозы с небольшими приращениями до достижения клинического эффекта и тщательный контроль частоты дыхания и насыщения кислородом (см. Также подраздел «Недоношенные дети и новорожденные» выше).
Сопутствующее употребление алкоголя / средств, угнетающих ЦНС
Следует избегать одновременного применения мидазолама с алкоголем и / или средствами, угнетающими ЦНС. Одновременное применение может усилить клинический эффект мидазолама, вызывая выраженный седативный эффект или клинически значимое угнетение дыхания (см. Раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
Злоупотребление алкоголем или лекарственными средствами в анамнезе
Следует избегать применения мидазолама, а также других бензодиазепинов у пациентов со злоупотреблением алкоголя или лекарственных средств в анамнезе.
критерии выписки
После введения мидазолама пациенты могут быть выписаны из больницы или отправлены в консультационную комнату только по рекомендации врача и при наличии сопровождающего лица. Пациент не должен оставаться без присмотра после выписки.
Применение в период беременности или кормления грудью
Беременность.
Недостаточно данных для оценки безопасности мидазолама в период беременности.
Исследования на животных не указывают на тератогенный эффект, но при применении других бензодиазепинов наблюдается фетотоксичность. Нет данных о применении препарата в течение первых двух триместров беременности.
Сообщалось, что применение высоких доз мидазолама в последнем триместре беременности, во время родов или при применении в качестве индукционного агента анестезии при кесаревом сечении вызывает неблагоприятные побочные эффекты для матери или плода (ингаляционный риск для матери, нарушение сердечного ритма у плода, гипотонию, нарушение сосания, гипотермию и угнетения дыхания у новорожденных).
Кроме того, у детей, рожденных от матерей, получавших бензодиазепины регулярно во время последней стадии беременности, может развиться физическая зависимость с возможным риском развития симптомов абстиненции в постнатальном периоде.
Итак, мидазолам не следует назначать во время беременности, если это не является насущной необходимостью. Желательно избегать применения его при кесаревом сечении.
Риск для новорожденных следует принимать во внимание при применении мидазолама для любой операции, ближайшей к сроку родов.
Кормления грудью.
Мидазолам в небольших количествах выделяется в грудное молоко. Кормящим матерям не рекомендуется кормить ребенка грудью в течение 24 часов после введения мидазолама.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Седация, амнезия, нарушение внимания и нарушения мышечной функции могут негативно повлиять на способность управлять транспортным средством и обслуживать механизмы. Перед введением мидазолама следует предупредить пациента, чтобы он воздержался от управления транспортным средством и обслуживание механизмов до полного прекращения эффекта препарата. Врач должен решить, когда эти действия могут быть восстановлены. Рекомендуется обеспечить сопровождение пациента при возвращении домой после выписки.
Способ применения Мидазолам Калцекс и дозы
Применяют внутримышечно, внутривенно или ректально.
Инструкции по разведению лекарственного средства перед применением см. ниже «Указания по применению».
стандартная дозировка
Мидазолам - сильный седативный средство, которое требует медленного введения и индивидуального подбора дозы. Титрования дозы настоятельно рекомендуется для достижения безопасного уровня седации в соответствии с клиническими потребностей, физического состояния, возраста и сопутствующей терапии. Для пациентов в возрасте от 60 лет, ослабленных пациентов или хронически больных и детей препарат следует назначать с осторожностью, а факторы риска для каждого пациента должны оцениваться индивидуально. Стандартные дозировки приведены в таблице ниже. Дополнительная информация приведена в тексте после таблицы.
индикация | Взрослые <60 лет | Взрослые ≥60 лет / ослаблены или хронически больные пациенты | дети |
седация с сохранением сознания | в/в Начальная доза 2—2,5 мг Шаг титрования: 1 мг Суммарная доза 3,5—7,5 мг | в/в Начальная доза 0,5—1 мг Шаг титрования: 0,5—1 мг Суммарная доза <3,5 мг | в / в детям в возрасте от 6 месяцев до 5 лет Начальная доза 0,05—0,1 мг/кг Суммарная доза <6 мг в / в детям в возрасте от 6 до 12 лет Начальная доза 0,025—0,05 мг/кг Суммарная доза <10 мг ректально детям> 6 месяцев 0,3—0,5 мг/кг в / м детям в возрасте от 1 до 15 лет 0,05—0,15 мг/кг |
Премедикация перед введением наркоза | в/в 1—2 мг повторно в/м 0,07 —0,1 мг/кг | в/в Начальная доза 0,5 мг Медленное повышение дозы титрованием, если необходимо в/м 0,025—0,05 мг/кг | ректально детям> 6 месяцев 0,3—0,5 мг/кг в / м детям в возрасте от 1 до 15 лет 0,08—0,2 мг/кг |
индукция наркоза | в/в 0,15—0,2 мг/кг (0,3-0,35 мг / кг без премедикации) | в/в 0,05—0,15 мг/кг (0,15-0,3 мг / кг без премедикации) | |
Седативный компонент в поддержке анестезии | в/в прерывистые дозы 0,03-0,1 мг / кг или непрерывным инфузия 0,03 - 0,1 мг / кг / час | в/в низкие дозы, чем рекомендуется для взрослых <60 лет | |
Седация в отделении интенсивной терапии (ОИТ) | в/в Нагрузочная доза: 0,03-0,3 мг / кг с шагом 1-2,5 мг Поддерживающая доза 0,03-0,2 мг / кг / час | в / в новорожденным <32 недель гестационного возраста 0,03 мг / кг / час в / в новорожденным> 32 недель гестационного возраста и младенцам в возрасте до 6 месяцев 0,06 мг / кг / час в / в детям> 6 месяцев Нагрузочная доза: 0,05—0,2 мг/кг Поддерживающая доза 0,06-0,12 мг / кг / час | |
Дозирование при седации с сохранением сознания
Для седации, необходимой для диагностических и хирургических процедур, мидазолам вводят внутривенно. Соответствующую дозу подбирают индивидуально. Препарат нельзя вводить быстро или в виде болюсной инъекции, а только путем титрования дозы. Возникновение седативного эффекта может варьировать индивидуально, в зависимости от физического состояния пациента и режима дозирования, используемый (например, скорость введения, величина дозы). При необходимости могут быть введены дополнительные дозы в соответствии с индивидуальными потребностями. Действие наступает через 2 минуты после инъекции. Максимальный эффект достигается через 5-10 минут.
взрослые
Мидазолам следует вводить медленно со скоростью примерно 1 мг / 30 секунд. Взрослым в возрасте до 60 лет вводят от 2 до 2,5 мг за 5-10 минут до начала процедуры как начальную дозу. Начальная доза может сопровождаться следующими дополнительными дозами по 1 мг по необходимости. Средняя суммарная доза составляет от 3,5 до 7,5 мг. Введение суммарной дозы, превышающей 5 мг, обычно не требуется.
Начальная доза для пациентов в возрасте от 60 лет, ослабленных пациентов или пациентов с хроническими заболеваниями составляет 0,5-1 мг, вводится за 5-10 минут до начала процедуры. При необходимости можно вводить следующие дополнительные дозы по 0,5-1 мг мидазолама. Для этих пациентов может потребоваться больше времени для достижения максимального эффекта, поэтому дополнительные дозы мидазолама следует титровать очень медленно и осторожно. Введение суммарной дозы, превышающей 3,5 мг, обычно не требуется.
педиатрическая популяция
Введение: дозы мидазолама медленно титруют до достижения желаемого клинического эффекта. Начальную дозу вводят за 2-3 минуты. Чтобы полностью оценить седативный эффект, следует подождать еще 2-5 минут, прежде чем начинать процедуру или повторять дозу. Если необходимо усилить седативный эффект, следует продолжать вводить дополнительные низкие дозы, пока не будет достигнут необходимый степень седации. Для младенцев и детей до 5 лет могут понадобиться значительно более высокие дозы (мг / кг) по сравнению с детьми старшего возраста и подростками.
• Дети в возрасте до 6 месяцев: эти дети особенно склонны к развитию обструкции дыхательных путей и гиповентиляции, так седация с сохранением сознания для них не рекомендуется.
• Дети в возрасте от 6 месяцев до 5 лет: начальная доза составляет от 0,05 до 0,1 мг / кг. Для достижения желаемого эффекта может потребоваться введение дозы до 0,6 мг / кг, однако суммарная доза не должна превышать 6 мг. Более высокие дозы могут вызвать длительный седативный эффект и риск гиповентиляции.
• Дети в возрасте от 6 до 12 лет начальная доза составляет 0,025 до 0,05 мг / кг. Может понадобиться суммарная доза 0,4 мг / кг (максимальная доза - 10 мг). Более высокие дозы могут вызвать длительный седативный эффект и риск гиповентиляции.
• Дети в возрасте от 12 до 16 лет: применять рекомендуемые дозы для взрослых.
Ректальное введение: общая доза мидазолама обычно составляет от 0,3 до 0,5 мг / кг. Раствор, содержащийся в ампулах, вводят ректально с помощью пластикового аппликатора, прикрепленного к шприцу. Если объем вводимого слишком мал, можно добавить воду до общего объема 10 мл. Вся доза должна быть введена сразу. Избегать повторного ректального введения. Ректальное введение не рекомендуется детям до 6 месяцев из-за ограниченных данные по этой возрастной группы.
М введение: дозы варьируют от 0,05 до 0,15 мг / кг. Обычно не требуется суммарная доза превышает 10,0 мг. М введение возможно только в исключительных случаях. Ректального введения следует отдать предпочтение, поскольку инъекция болезненна.
Детям с массой тела менее 15 кг растворы мидазолама с концентрацией выше 1 мг / мл применять не рекомендуется. Высокие концентрации следует разводить до 1 мг / мл.
Дозирование при астении
Введение мидазолама непосредственно перед процедурой вызывает седативный эффект (гипнотическое или анестезирующий эффект и сниженный уровень сознания) и предоперационное ухудшение памяти. Мидазолам можно вводить в сочетании с антихолинергическими средствами. В таком случае мидазолам вводят внутривенно или внутримышечно (глубоко в мышечную массу, по 20-60 минут до индукции анестезии), а детям лучше применять препарат ректально (см. Ниже). После введения премедикации пациент должен находиться под постоянным тщательным контролем, поскольку чувствительность к препарату варьирует и могут возникнуть симптомы передозировки.
взрослые
Рекомендуемая доза, используемая для предоперационной седации и ухудшение памяти о предоперационные события для пациентов, относящихся к классу физического состояния ASA I и II, а также для пациентов в возрасте до 60 лет, составляет от 1 до 2 мг (при необходимости дозу можно повторить) или от 0,07 до 0,1 мг / кг внутримышечно. Для пациентов в возрасте от 60 лет, ослабленных пациентов или хронически больных доза должна быть уменьшена и скорректирована в зависимости от конкретного случая. Рекомендуемая внутривенная начальная доза составляет 0,5 мг, при необходимости ее увеличивают медленным титрованием. Рекомендованная начальная доза при введении составляет от 0,025 до 0,05 мг / кг. В случае одновременного введения наркотических средств дозу мидазолама следует уменьшить. Обычная доза составляет от 2 до 3 мг.
педиатрическая популяция
Новорожденные и дети до 6 месяцев
Это лекарственное средство не рекомендуется детям до 6 месяцев из-за ограниченных данные по этой возрастной группы.
Дети в возрасте от 6 месяцев
Ректальное введение: общую дозу мидазолама (обычно в диапазоне от 0,3 до 0,5 мг / кг) необходимо вводить за 15-30 минут до индукции анестезии. Раствор, содержащийся в ампулах, вводят ректально с помощью пластикового аппликатора, прикрепленного к шприцу. Если объем вводимого слишком мал, можно добавить воду до общего объема 10 мл.
М введение: внутримышечное введение болезненно, поэтому этот метод введения следует использовать только в исключительных случаях. Следует отдать предпочтение ректального введения. Диапазон эффективных и безопасных доз для введения составляет от 0,08 до 0,2 мг / кг. Детям в возрасте от 1 до 15 лет нужны пропорционально высокие дозы в пересчете на массу тела, чем взрослым.
Детям с массой тела менее 15 кг растворы мидазолама с концентрацией выше 1 мг / мл применять не рекомендуется. Раствор более высокой концентрации следует разводить до 1 мг / мл.
индукция наркоза
взрослые
Если мидазолам применяется перед другими анестезирующими средствами для индукции анестезии, индивидуальная реакция пациентов варьирует. Доза должна быть увеличена путем титрования до достижения желаемого эффекта. Дозу титровать в соответствии с возрастом пациента и его клинического статуса. Если мидазолам применяется до или в сочетании с другими внутривенными или ингаляционными лекарственными средствами, применяемыми для индукции анестезии, начальные дозы всех этих лекарственных средств сдил значительно уменьшить, иногда до 25% от обычной начальной дозы.
Желаемый уровень обезболивания достигается путем постепенного увеличения дозы. Для внутривенной индукции анестезии мидазолам вводят медленно, по частям. Каждую часть дозы (не более 5 мг) следует вводить в течение 20-30 секунд с 2-минутными интервалами между приемами.
• Для взрослых в возрасте до 60 лет , которым была назначена премедикация , обычно назначают дозу от 0,15 до 0,2 мг / кг.
• Для взрослых без премедикации в возрасте до 60 лет могут применяться более высокие дозы (0,3-0,35 мг / кг). При необходимости для завершения индукции могут быть введены дополнительные дозы примерно 25% от начальной дозы пациента. Индукция также может проводиться с помощью ингаляционных анестетиков. В рефрактерных случаях для индукции может применяться общая доза до 0,6 мг / кг, но такие высокие дозы могут вызвать длительное восстановление после анестезии.
• Для взрослых в возрасте от 60 лет, которым была назначена премедикация, ослабленных пациентов или пациентов с хроническими заболеваниями дозирования должно быть значительно снижена, например до 0,05-0,15 мг / кг, вводимых в течение 20-30 секунд, со временем наступления действия препарата 2 минуты.
• Для взрослых без премедикации в возрасте от 60 лет для индукции обычно требуются более высокие дозы мидазолама. Рекомендованная начальная доза составляет от 0,15 до 0,3 мг / кг. Для истощенных пациентов или пациентов с серьезным системным заболеванием без премедикации обычно следует вводят меньшее количество мидазолама для индукции. Начальная доза от 0,15 до 0,25 мг / кг обычно достаточно.
Как седативное компонент при комбинированной анестезии
взрослые
Мидазолам можно вводить как седативное компонент в комбинированной анестезии или путем дальнейшего мелкого введение малых доз внутривенно (в диапазоне от 0,03 до 0,1 мг / кг), или путем непрерывной инфузии мидазолама внутривенно (в диапазоне от 0,03 до 0,1 мг / кг / час), обычно в сочетании с анальгетиками. Доза и интервалы между дозами варьируют в зависимости от индивидуальной реакции пациента.
Для взрослых в возрасте от 60 лет, ослабленных пациентов или хронически больных для поддержки нужны более низкие дозы.
Седация в отделении интенсивной терапии
Желаемую степень седации достигается путем поэтапного титрования дозы мидазолама с последующей или непрерывной инфузии, или прерывистым болюсным введением. Мидазолам вводят в соответствии с клиническими потребностей, состояния пациента, возраста и сопутствующих препаратов (см. Раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
взрослые
Нагрузочная доза от 0,03 до 0,3 мг / кг, вводится медленно с нарастанием. Каждую дозу от 1 до 2,5 мг следует вводить в течение 20-30 секунд с 2-минутными интервалами между приемами. Для пациентов с гиповолемией, вазоконстрикцией или гипотермией нагрузочная доза должна быть уменьшена или пропущена. Если мидазолам вводят одновременно с сильными анальгетиками, последние следует вводить в первую очередь. Это обеспечивает безопасное титрование седативного эффекта мидазолама, таким образом, он не подвержен влиянию анальгетической седации.
Внутривенная поддерживающая доза от 0,03 до 0,2 мг / кг / час. Для пациентов с гиповолемией, вазоконстрикцией или гипотермией поддерживающую дозу необходимо уменьшить. Степень седации следует оценивать на регулярной основе. Длительная седация может привести к развитию толерантности, что может потребовать увеличения дозы.
педиатрическая популяция
Новорожденные и дети до 6 месяцев
Мидазолам вводят в виде внутривенной непрерывной инфузии. Начальная доза для новорожденных с гестационным возрастом менее 32 недель, составляет 0,03 мг / кг / час (0,5 мкг / кг / мин), а для новорожденных с гестационным возрастом более 32 недель, а также для детей до 6 месяцев - 0,06 мг / кг / ч (1 мкг / кг / мин).
Внутривенные погрузочные дозы не рекомендуются недоношенным, новорожденным и детям до 6 месяцев для достижения терапевтических концентраций лучше, чтобы скорость инфузии была выше в течение первых часов введения. Скорость инфузии следует часто и тщательно просматривать, чтобы выбрать минимальную эффективную дозу и предотвратить накопление препарата (особенно в течение первых 24 часов). Необходим тщательный контроль частоты дыхания и насыщения кислородом.
Дети в возрасте от 6 месяцев
Детям, находящимся на искусственной вентиляции легких, а также интубированных, следует вводить нагрузочную дозу от 0,05 до 0,2 мг / кг медленно в течение не менее 2-3 минут для достижения желаемого клинического эффекта.
Мидазолам не следует вводить в виде быстрой внутривенной инъекции. После введения нагрузочной дозы мидазолам вводят в виде непрерывной инфузии со скоростью от 0,06 до 0,12 мг / кг / час (от 1 до 2 мкг / кг / мин). При необходимости скорость инфузии может быть увеличена или уменьшена (обычно на 25% от начальной или следующей скорости инфузии), или дополнительные дозы мидазолама вводят для поддержания или увеличения желаемого эффекта.
Если инфузию мидазолама начинают гемодинамиично нестабильным пациентам, обычную нагрузочную дозу следует титровать низкими дозами, а пациента следует контролировать на наличие гемодинамических изменений (например, гипотонии). Эти пациенты более чувствительны к депрессивному влияния мидазолама на дыхательную функцию, поэтому нужно тщательно контролировать частоту дыхания и насыщения кислородом.
Недоношенным детям, новорожденным и детям с массой тела ниже 15 кг не рекомендуется применять растворы мидазолама с концентрацией выше 1 мг / мл. Раствор более высокой концентрации следует разводить до 1 мг / мл.
Пациенты с нарушениями функции почек
У пациентов с нарушениями функции почек (клиренс креатинина <10 мл / мин) фармакокинетика несвязанного мидазолама после однократного введения аналогична фармакокинетике у здоровых добровольцев. Однако после длительной инфузии у пациентов отделения интенсивной терапии (ОИТ) средняя продолжительность седативного эффекта в популяции с почечной недостаточностью была значительно увеличена, прежде всего из-за накопления альфа-гидроксимидазоламу глюкуронида. Нет конкретных данных для пациентов с тяжелой почечной недостаточностью (клиренс креатинина ниже 30 мл / мин), которые получают мидазолам для индукции анестезии.
Пациенты с нарушениями функции печени
При нарушениях функции печени уменьшается клиренс внутривенно введенного мидазолама с последующим увеличением терминального периода полувыведения. Это может привести к более сильному и длительного клинического эффекта. Могут понадобиться более низкие дозы мидазолама, и следует обеспечить тщательный мониторинг показателей жизненно важных функций (см. Раздел «Особенности применения»).
Указания по применению
Совместим с такими растворами для инфузий 0,9% раствор натрия хлорида, 5% раствор глюкозы, 10% раствор глюкозы, раствор Рингера, раствор Хартмана.
Для внутривенной инфузии содержимое ампул мидазолама Калцекс может быть разведено одним из вышеупомянутых растворов в соотношении 15 мг мидазолама на 100-1000 мл раствора.
Предназначен только для одноразового применения, неиспользованный остаток раствора следует уничтожить.
Перед применением раствор следует осмотреть. Следует использовать только прозрачный раствор без видимых частиц.
Как открыть ампулу:
- Вернуть ампулу цветной точкой к себе. Слегка постучать пальцем по верхней части ампулы, чтобы раствор оказался в нижней части ампулы (рис. 1).
- Ампулу открывать обеими руками удерживая нижнюю часть ампулы одной рукой, другой рукой нажать на верхнюю часть ампулы в направлении от цветной точки) (Рис. 2).
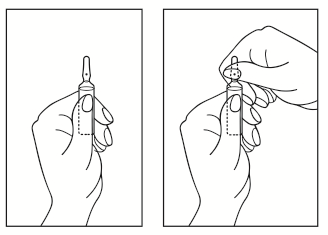
Рис. 1. Рис. 2.
Дети
Применение препарата детям подробно описано в разделе «Способ применения и дозы». Детям в возрасте до 6 месяцев для седации применять не рекомендуется, так как эта возрастная группа пациентов чрезвычайно чувствительна к гиповентиляции и нарушение проходимости дыхательных путей.
Передозировка
Симптомы.
Как и другие бензодиазепины, мидазолам обычно вызывает сонливость, атаксия, дизартрию и нистагм. Передозировка при изолированном введении мидазолама редко угрожает жизни, но может привести к арефлексии, апноэ, гипотонии, кардиореспираторной депрессии и в редких случаях - до комы. Кома обычно длится несколько часов, но она может быть более длительной и циклической, особенно у пожилых пациентов. Угнетающее влияние бензодиазепинов на дыхательную функцию более выражен у пациентов с заболеваниями дыхательных путей. Бензодиазепины усиливают действие других препаратов, угнетающих ЦНС, включая алкоголь.
Лечение.
Жизненно важные показатели пациента должны контролироваться, поддерживающую терапию нужно начинать в соответствии с клинического статуса пациента. В частности, пациентам может потребоваться симптоматическое лечение, направленное на поддержку кардиореспираторной деятельности, а также функций ЦНС.
При пероральном приеме следует избегать дальнейшем всасыванию, используя соответствующий метод, например применение активированного угля в течение 1-2 часов после передозировки. Если применяется активированный уголь, защита дыхательных путей обязательный для пациентов, страдающих сонливостью. В случае смешанного передозировки может быть рассмотрено промывание желудка, но не как обычное мероприятие.
При тяжелом угнетении ЦНС, следует рассмотреть применение флумазенил, антагониста бензодиазепинов. Это должно осуществляться только в условиях строгого контроля. Флумазенил имеет короткий период полувыведения (около часа), поэтому пациентов, которые получили флумазенил, следует наблюдать после прекращения его действия. Флумазенил следует применять с осторожностью при одновременном применении лекарственных средств, снижающих порог судом (например, трициклические антидепрессанты). Более подробную информацию о правильном применении флумазенил смотрите в краткой характеристике лекарственного средства.
Побочные эффекты
Очень часто (≥1 / 10), часто (≥1 / 100, <1/10), нечасто (≥1 / 1000, <1/100), редко (≥1 / 10000, <1/1000), очень редко (<1/10 000), частота неизвестна (невозможно определить по имеющимся данным).
Со стороны иммунной системы: частота неизвестна - повышенная чувствительность, ангионевротический отек, анафилактический шок.
Со стороны психики: частота неизвестна - спутанность сознания, эйфория, галлюцинации, возбуждение *, враждебность * ярость *, агрессивность * возбуждения *, физическая зависимость от лекарственных средств и синдром отмены, злоупотребления.
Со стороны нервной системы: частота неизвестна - непроизвольные движения (включая тонические / клонические движения и тремор мышц) * гиперактивность *, седация (длительная и послеоперационная), уменьшение бдительности, сонливость, головная боль, головокружение, атаксия, антероградная амнезия ** , продолжительность которой непосредственно связана с введенной дозой, судороги, вызванные синдромом отмены. У недоношенных детей и новорожденных сообщалось о судорогах.
Со стороны сердца: частота неизвестна - остановка сердца, брадикардия.
Со стороны сосудистой системы: частота неизвестна - артериальная гипотензия, вазодилатация, тромбофлебит, тромбоз.
Со стороны дыхательной системы: частота неизвестна - угнетение дыхания, апноэ, остановка дыхания, одышка, ларингоспазм, икота.
Со стороны желудочно-кишечного тракта: частота неизвестна - тошнота, рвота, запор, сухость во рту.
Со стороны кожи и подкожной ткани: частота неизвестна - кожная сыпь, крапивница, зуд.
Общие нарушения и реакции в месте введения: частота неизвестна - утомление, эритема в месте инъекции, боль в месте инъекции.
Травмы, интоксикация и процедурные осложнения: частота неизвестна - падение, переломы ***.
Обстоятельств: частота неизвестна - угроза насилия *.
* Сообщалось, что подобные парадоксальные реакции возникали среди детей и людей пожилого возраста, в частности (см. Раздел «Особенности применения»).
** Антероградная амнезия может храниться до конца процедуры, в нескольких единичных случаях была отмечена длительная амнезия (см. Раздел «Особенности применения»).
*** Риск падений и переломов выше у тех, кто принимает сопутствующие седативные препараты (включая алкогольные напитки), и у пациентов пожилого возраста.
Зависимость. Мидазолам может вызвать развитие физической зависимости, даже если применяется в терапевтических дозах. Прекращение лечения (особенно внезапное) после длительного введения может вызвать симптомы отмены, включая судороги синдрома отмены препарата (см. Раздел «Особенности применения»). Сообщалось о случаях злоупотребления препаратом. Возникали тяжелые Кардиореспираторной побочные реакции. Угрожающие жизни осложнения чаще наблюдались у взрослых в возрасте от 60 лет и у пациентов с ранее существовавшей дыхательной недостаточностью или нарушениями функции сердца, особенно при быстром введении или введении высоких доз (см. Раздел «Особенности применения»).
Срок годности Мидазолам Калцекс
2 года.
Не применять после истечения срока годности, указанного на упаковке.
Срок годности после разведения.
Химическая и физическая стабильность при применении была продемонстрирована в течение 24 часов при температуре 25 ° C и в течение 3 дней при температуре 2 - 8 ° C при разведении с такими инфузионными растворами: 0,9% раствор натрия хлорида, 5% и 10% раствор глюкозы, раствор Рингера и раствор Хартмана.
С микробиологической точки зрения раствор следует использовать немедленно. Если он не используется сразу, то за время и условия хранения к его использованию несет ответственность пользователь, и обычно они не должны превышать 24 ч при температуре 2 - 8 ° C, если только разведение не проводилось в хорошо контролируемых и валидизированных асептических условиях.
Условия хранения Мидазолам Калцекс
Не требует специальных условий хранения.
Хранить в оригинальной упаковке для защиты от действия света. Не замораживать.
Хранить в недоступном для детей месте.
Несовместимость.
Мидазолам Калцекс, раствор для инъекций / инфузий, можно разводить в 6% растворе глюкозы Macrodex. Мидазолам Калцекс нельзя смешивать с щелочными растворами для инъекций. Мидазолам оседает в растворах, содержащих натрия гидрокарбонат.
Это лекарственное средство нельзя смешивать с другими лекарственными средствами, кроме указанных выше (см. «Указания по применению»).
Упаковка
По 1 мл или 3 мл раствора в ампуле с бесцветного стекла и гидролитического класса с маркировочными кольцами и с точкой разлома.
По 5 ампул в контурной ячейковой упаковке (поддоне) с поливинилхлоридной пленки.
По 1 или 2 контурные упаковки (поддоны) в пачке с картона с контролем первого вскрытия в виде самоклеющейся стикер на каждой части пачке, что открывается.
Категория отпуска
По рецепту.
Производитель
Производитель, который отвечает за выпуск серии:
АО «Калцекс», Латвия.
Местонахождение производителя
Ул. Крустпилс, 71е, Рига, LV-1057, Латвия.
Заявитель.
АО «Калцекс», Латвия.
Местонахождение заявителя.
Ул. Крустпилс, 53, Рига, LV-1057, Латвия.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Мидазолам Калцекс только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- ХСМ Фарма с.р.о.
- http://www.drlz.com.ua - Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Мидазолам Калцекс |
| Производитель: | ХСМ Фарма с.р.о. |
| Форма выпуска: | раствор для инъекций, 5 мг / мл по 1 мл или 3 мл в ампуле, по 5 ампул в контурной ячейковой упаковке (поддоне), по 1 или 2 контурные упаковки (поддоны) в пачке из картона |
| Регистрационное удостоверение: | UA/18291/01/01 |
| Дата начала: | 04.09.2020 |
| Дата окончания: | 09.04.2025 |
| МНН: | Midazolam |
| Условия отпуска: | по рецепту |
| Состав: | 1 мл мидазолама 5 мг |
| Фармакологическая группа: | Снотворные и седативные препараты, производные бензодиазепина. |
| Код АТХ: | N05CD08 |
| Заявитель: | АО "Калцекс" |
| Страна заявителя: | Латвия |
| Адрес заявителя: | ул. Крустпилс, 53, Рига, LV-1057, Латвия |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Нет |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Моно |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| N | Средства, действующие на нервную систему |
| N05 | Психолептическое средства |
| N05C | Снотворные и седативные препараты |
| N05CD | Производные бензодиазепина |
| N05CD08 | Мидазолам |
