- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Ультибро Бризхайлер инструкция по применению
Официальная инструкция лекарственного препарата Ультибро Бризхайлер порошок 110 мкг/50 мкг. Описание и применение Ul'tibro Brizhajler, аналоги и отзывы. Инструкция Ультибро Бризхайлер порошок утвержденная компанией производителем.
Состав
действующее вещество: glycopyrronium bromide, indacaterol maleate;
1 капсула содержит 110 мкг индакатеролу, что соответствует 143 мкг индакатеролу малеата, что эквивалентно 85 мкг целевой дозы высвобождается, и 50 мкг гликопиронию, что соответствует 63 мкг гликопиронию бромид, что эквивалентно 43 мкг целевой дозы высвобождается;
Вспомогательные вещества: лактоза, магния стеарат.
Лекарственная форма
Порошок для ингаляций, твердые капсулы.
Основные физико-химические свойства:
капсулы с прозрачной желтой крышечкой с нанесенным черным знаком и прозрачным корпусом с нанесенным синим цветом надписью «ИPG110.50» под двумя синими полосами, размером 3, содержащие порошок от белого до почти белого цвета.
Фармакологическая группа
Средства, применяемые при обструктивных заболеваниях дыхательных путей. Комбинация адренергических и антихолинергических средств.
Код ATH R03AL04.
Фармакологические свойства
Фармакологические.
механизм действия
Когда индакатерол и гликопироний применяются вместе, они аддитивную эффективность, поскольку действуют на разные рецепторы и пути для достижения расслабления малых мышц. Из-за разницы в плотности β2-адренорецепторов и М3-рецепторов в центральных дыхательных путях по сравнению с меньшими дыхательными путями β2-агонисты могут быть более эффективными в расслаблении малых дыхательных путей, тогда как антихолинергическое соединение может быть более эффективной в больших дыхательных путях. Таким образом, для оптимальной бронходилатации во всех участках легких человека комбинация β2-адреноагониста и антагониста мускариновых рецепторов может быть эффективной.
Индакатерол
Индакатерол является агонистом β2-адренорецепторов длительного действия для применения один раз в сутки. Фармакологические эффекты β2-адренорецепторов, в том числе индакатеролу, по крайней мере частично объясняются стимуляцией внутриклеточной аденилатциклазы - фермента, который катализирует превращение аденозинтрифосфата (АТФ) на циклический 3 ', 5'-аденозинмонофосфат (циклический монофосфат). Повышение уровня цАМФ вызывает расслабление гладких мышц бронхов. Исследования in vitroпоказали, что индакатерол более чем в 24 раза активнее агонист β2-рецепторов по сравнению с β1-рецепторами и в 20 раз активнее по β3-рецепторов. При ингаляции индакатерол действует локально в легких как бронхолитик. Индакатерол представляет собой частичный агонист β2-адренорецепторов человека с наномолярный потенцией. Хотя β2-рецепторы являются преобладающими -адренорецепторами в бронхиальных гладких мышцах, а β1-рецепторы являются преобладающими рецепторами в сердце человека, β2-адренорецепторы также в сердце человека, содержит от 10% до 50% от общего количества адренорецепторов. Точные функции β2-адренорецепторов в сердце неизвестны, но их присутствие повышает вероятность того, что даже высокоселективные
β2-адренергические агонисты могут иметь сердечные эффекты.
Гликопироний
Гликопироний является ингаляционным антагонистом мускариновых рецепторов (антихолинергическим средство) длительного действия для применения один раз в сутки с целью поддерживающей бронхолитической терапии хронического обструктивного заболевания легких (ХОБЛ). Парасимпатические нервы являются основными бронхоконстриктивнимы нейронными путями в дыхательных путях, и холинергический тонус является ключевым компонентом обратной обструкции дыхательных путей при ХОБЛ. Гликопироний действует, блокируя бронхоконстриктивну действие ацетилхолина на клетки гладких мышц дыхательных путей, тем самым расширяя дыхательные пути.
Гликопиронию бромид - это високоспориднений антагонист мускариновых рецепторов. Более 4-кратная селективность в отношении человеческих М3-рецепторов по сравнению с человеческими М2-рецепторами была продемонстрирована в исследованиях связывания радиолиганду.
фармакодинамические эффекты
Первичные фармакодинамические эффекты
Комбинация индакатеролу и гликопиронию в лекарственном средстве Ультибро Бризхайлер продемонстрировала быстрое начало действия - в течение 5 минут после приема. Эффект остается устойчивым в течение 24-часового интервала дозирования.
Средний бронхолитический эффект, полученный из последовательных измерений объема форсированного выдоха за 1 с (ОФВ1) в течение 24 часов, составляет 0,32 литра после 26 недель лечения. Эффект был значительно выше в Ультибро Бризхайлеру по сравнению с индакатеролом, гликопиронием или Тиотропия отдельно (разница 0,11 л для каждого сравнения). Не было никаких доказательств эффекта тахифилаксии Ультибро Бризхайлеру с течением времени по сравнению с плацебо или его компонентов в монотерапии.
Влияние на частоту сердечных сокращений
Частоту эффектов на сердечные сокращения у здоровых добровольцев исследовали после применения одной дозы Ультибро Бризхайлеру 440 мкг / 200 мкг, которую вводили в четыре шага с промежутками времени в 1:00 и сравнивали с эффектами плацебо, индакатеролу 600 мкг, гликопиронию 200 мкг и сальметерола 200 мкг. Наибольшее повышение частоты сердечных сокращений при применении препарата Ультибро Бризхайлер по сравнению с плацебо составляло +5,69 уд / мин, наибольшее снижение было - 2,51 уд / мин. В общем, изучение влияния на частоту сердечных сокращений в течение долгого времени не выявило последовательного фармакодинамического эффекта Ультибро Бризхайлеру. Хотя не было существенных эффектов, когда Ультибро Бризхайлер сравнивали с индакатеролом и гликопиронием отдельно, частота сердечных сокращений была несколько выше (наибольшая разница - около 11 ударов в минуту) после ингаляции 200 мкг сальметерола. Частота сердечных сокращений у пациентов с ХОБЛ в надтерапевтичних дозах была исследована при применении Ультибро Бризхайлеру в дозах 150 мкг / 100 мкг, 300 мкг / 100 мкг и
600 мкг / 100 мкг. Не было никаких существенных эффектов Ультибро Бризхайлеру на среднюю частоту сердечных сокращений в течение 24 часов и частоту сердечных сокращений, оценивалась через 30 минут, 4 и 24 часов.
интервал QT
Компоненты лекарственного средства Ультибро Бризхайлер, как известно, не имеют влияния на удлинение QT при применении в клинических дозах. Исследование TQT с участием здоровых добровольцев, получавших дозы ингаляционного индакатеролу до 600 мкг, не показало клинически значимого влияния на интервал QT. Аналогично в исследовании TQT не наблюдалось удлинение QT после ингаляции доз 400 мкг гликопиронию. Эффекты Ультибро Бризхайлеру по интервала QTc были исследованы у здоровых добровольцев после ингаляции Ультибро Бризхайлеру 440 мкг / 200 мкг в четыре шага, разделенные одним часом. Самая соответствующая по времени разница по сравнению с плацебо составляла
4,62 мс (90% доверительный интервал (ДИ) 0,40; 8,85 мс), больше подходящее по время снижение составило -2,71 мс (90% ДИ -6,97; 1,54 мс), что свидетельствует о том, что Ультибро Бризхайлер не имел существенного влияния на интервал QT, как и ожидалось из свойств его компонентов. У пациентов с ХОБЛ дозы до 600 мкг / 100 мкг Ультибро Бризхайлеру также не имели никакого очевидного влияния на интервал QTc при повторных оценках ЭКГ, выполнялись через 15 минут - 24 часов после приема препарата. Несколько выше доля пациентов в группе Ультибро Бризхайлеру 600 мкг / 100 мкг имели удлинение QTc более 450 мс. Ряд заметных изменений QTcF по сравнению с исходным состоянием (> 30 мс) были одинаковы во всех группах активного лечения (Ультибро Бризхайлер
600 мкг / 100 мкг, 300 мкг / 100 мкг, 150 мкг / 100 мкг и 300 мкг индакатеролу), но их было меньше в группе плацебо.
Уровень калия в сыворотке и глюкозы в крови
У здоровых добровольцев после введения Ультибро Бризхайлеру 440 мкг / 200 мкг, уменьшение концентрации калия было очень малым (максимальная разница - 0,14 ммоль / л по сравнению с плацебо). Максимальный эффект на уровень глюкозы в крови составлял
0,67 ммоль / л.
Клиническая безопасность и эффективность
Клиническая программа разработки Ультибро Бризхайлеру III фазы [IGNITE] включала шесть исследований, в которых участвовали более 8000 пациентов:
1) SHINE, 26-недельное плацебо и активно контролируемое исследование (индакатерол
150 мкг один раз в сутки, гликопироний 50 мкг один раз в сутки, открыт прием тиотропия 18 мкг один раз в сутки)
2) ILLUMINATE, 26-недельное активно контролируемое исследование (флутиказона / сальметерол 50 мкг / 500 мкг два раза в день);
3) SPARK, 64-недельное активно контролируемое исследование (гликопироний 50 мкг один раз в сутки, открыт прием тиотропия 18 мкг один раз в сутки)
4) ENLIGHTEN, 52-недельное плацебо-контролируемое исследование, в которое были включены более 5000 пациентов.
В эти исследования были включены пациенты, которые имели ХОБЛ легкой и очень тяжелой степени, были в возрасте от 40 лет и имели анамнез курения не менее 10 лет. Из этих четырех исследований в двух (SHINE и ENLIGHTEN) было постбронходилатацийне ОФВ1 <80% и ≥ 30% от прогнозируемого нормального значения и постбронходилатацийне соотношение ОФВ1 / ФЖЕЛ (форсированная жизненная емкость легких) составило менее 70%. В 26-недельное активно контролируемое исследование ILLUMINATE были включены пациенты, которые имели постбронходилатацийне ОФВ1 <80% и ≥ 40% от прогнозируемого нормального значения. Для сравнения, в 64-недельном исследовании SPARK были включены пациенты, которые имели тяжелое и очень тяжелое ХОБЛ с постбронходилатацийним ОФВ1 <50% от прогнозируемого нормального значения.
5) 3-недельное плацебо и активно-контролируемое исследование (тиотропий один раз в сутки) переносимости физической нагрузки;
6) 52-недельное активно-контролируемое исследование (флутиказона / сальметерол раза в сутки).
В четыре из этих исследований были включены пациенты, которые имели ХОБЛ от умеренной до тяжелой степени. В 64-недельное исследование были включены пациенты, которые имели ХОБЛ очень тяжелой степени и обострения ХОБЛ от умеренной до тяжелой степени ≥ 1 в анамнезе в предыдущем году. В 52-недельное активно контролируемое исследование были включены пациенты, которые имели ХОБЛ от умеренного до очень тяжелой степени и обострения ХОБЛ от умеренной до тяжелой степени ≥ 1 в анамнезе в предыдущем году.
Влияние на функцию легких
Ультибро Бризхайлер, который вводили в дозе 110 мкг / 50 мкг один раз в сутки, показал клинически значимое улучшение функции легких (при измерении объема форсированного выдоха за одну секунду, ОФВ1) в ряде клинических исследований. В исследованиях ИИИ фазы бронхолитические эффекты наблюдались в течение 5 минут после первой дозы и сохранялись в течение 24-часового интервала дозирования. В течение 26-недельного (SHINE) и 52-недельного (ENLIGHTEN) исследований не было ослабление бронхолитического эффекта с течением времени.
минимальный ОФВ1
В исследовании [SHINE] Ультибро Бризхайлер увеличивал минимальный ОФВ1 на 200 мл по сравнению с плацебо на момент 26-недельной первичной конечной точки (р <0,001) и продемонстрировал значительное увеличение по сравнению с группами монотерапии отдельными компонентами (индакатерол и гликопироний), а также с группой лечение тиотропия, как показано в таблице ниже.
Минимальное ОФВ1 (предел среднего) после введения дозы в 1-й день и на 26-й неделе (первичная конечная точка)
сравнение лечения | День 1-й | Неделя 26-й |
Ультибро Бризхайлер — плацебо Ультибро Бризхайлер - индакатерол Ультибро Бризхайлер - гликопироний Ультибро Бризхайлер - тиотропий | 190 мл (р < 0,001) 80 мл (р < 0,001) 80 мл (р < 0,001) 80 мл (р < 0,001) | 200 мл (р < 0,001) 70 мл (р < 0,001) 90 мл (р < 0,001) 80 мл (р < 0,001) |
Средний переддозовий ОФВ1 (среднее значение, установленное по 45 и 15 минут до утренней дозы исследуемого препарата) был клинически значимым и статистически значимым в пользу Ультибро Бризхайлеру на 26-й неделе по сравнению с флутиказоном / сальметерол (разница в средних значениях по методу наименьших квадратов 100 мл, р <0,001) (ILLUMINATE), на 52-й неделе по сравнению с плацебо (разница в средних значениях по методу наименьших квадратов 189 мл, р <0,001; ENLIGHTEN), а также во время всех визитов к 64-й недели в сравнению с гликопиронием (разница в средних значениях по методу наименьших квадратов 70-80 мл, р-значение
<0,001) и тиотропия (разница в средних значениях по методу наименьших квадратов 60-80 мл, р-значение <0,001; SPARK).
Во время 52-недельного активно-контролируемого исследования средний ОФВ1 до введения дозы был статистически значимым в пользу препарата Ультибро Бризхайлер во время всех визитов к 52-й недели по сравнению с флутиказоном / сальметерол (разница в средних значениях по методу наименьших квадратов 62-86 мл, p <0,001). На 26-й неделе препарат Ультибро Бризхайлер вызывал статистически значимое улучшение пикового ОФВ1 по сравнению с плацебо в течение первых 4:00 после введения дозы (разница в средних значениях по методу наименьших квадратов 330 мл) (p <0,001).
пиковый ОФВ1
Ультибро Бризхайлер вызвал статистически значимое улучшение пикового ОФВ1 по сравнению с плацебо в течение первых 4 ч после введения дозы в 1-й день (210 мл, р <0,001) и на 26-й неделе (330 мл, р <0,001) и по сравнению с индакатеролом (120 мл), гликопиронием (130 мл), тиотропия (130 мл) на 26-й неделе (р <0,001 для всех сравнений; SHINE) и по сравнению с флутиказоном / сальметерол в 1-й день (70 мл,
р <0,001 ) и на 26-й неделе (150 мл, р <0,001; ILLUMINATE).
Площадь под кривой ОФВ1
Ультибро Бризхайлер увеличивал AUC0-12 ОФВ1 после введения дозы (первичная конечная точка) на 140 мл через 26 недель (р <0,001) в активно контролируемом исследовании ILLUMINATE по сравнению с флутиказоном / сальметерол.
начало действия
В исследованиях SHINE и ILLUMINATE Ультибро Бризхайлер продемонстрировал статистически значимое быстрое наступление эффекта бронходилататоров в 1-й день и на 26-й неделе.
Начало действия по сравнению с плацебо, тиотропия и флутиказоном / сальметерол на 5-й и 30-й минутах в 1-й день и на 26-й неделе
По сравнению с плацебо 5 минут 30 минут По сравнению с Тиотропия 5 минут 30 минут По сравнению с флутиказоном / сальметерол 5 минут 30 минут | День 1-й 130 мл * 200 мл * 70 мл * 90 мл * 80 мл * 80 мл * | Неделя 26-й 290 мл * 320 мл * 120 мл * 140 мл * 150 мл * 160 мл * |
* Р <0,001 для всех сравнений лечения.
Субпопуляция серийной спирометрии
В 26-недельном плацебо-контролируемом исследовании SHINE, в 1-й день проводилась 12-часовая серийная спирометрия (рис. 1) и 24-часовая серийная спирометрия на 26-й неделе (рис. 2) в подгруппе из 294 пациентов. Серийные значение ОФВ1 в течение 12:00 в день 1-й и значение ОФВ1 в день 2-й показаны на рисунке 1, а на 26-й неделе - на рисунке 2. Улучшение функции легких сохранялось в течение 24 часов после первой дозы и устойчиво сохранялось в течение 26 недельного периода лечения без признаков толерантности.
Рис. 1. 24-часовой профиль пределы среднего ОФВ1 (л) в 1-й день (субпопуляция серийной спирометрии)

Вот в - предел среднего ОФВ1 (л)
Вот х - время (изначально, 30 минут, 1:00, 2:00, 4:00, 8:00, 12:00,
23 часа 15 минут, 23 часов 45 минут)
лечение
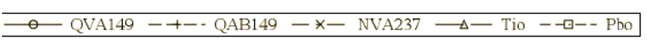
Рис. 2. 23 часов 45 минут профиля пределы среднего ОФВ1 (л) после 26 недель лечения (субпопуляция серийной спирометрии)
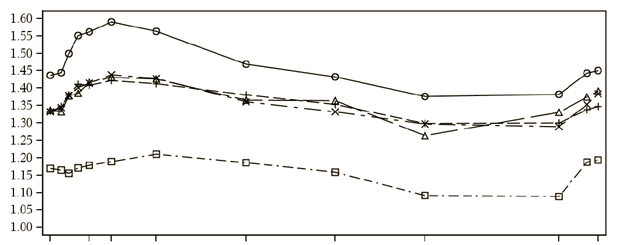
Вот в - предел среднего ОФВ1 (л)
Вот х - время (45 минут, 1:00, 2:00, 4:00, 8:00, 12:00, 16 часов,
22 часов, 23 часов 45 минут)
лечение

В субпопуляции серийной спирометрии исследования SHINE Ультибро Бризхайлер продемонстрировал статистически значимое улучшение ОФВ1 по сравнению с плацебо
(400 мл, р <0,001) и тиотропия (160 мл, р <0,001) через 2:00 после введения дозы на 26-й неделе.
Ультибро Бризхайлер также вызвал клинически значимое и статистически значимое улучшение ОФВ1 по сравнению с флутиказоном / сальметерол во всех временных точках, начиная с 5 минут после введения дозы до 12:00 после введения дозы как на 12-й неделе (р <0,001), так и 26- й неделе (р <0,001; ILLUMINATE) (см. рис. 3).
Рис. 3. Профиль пределы среднего ОФВ1 (литров) с 5 мин до 12 ч после введения дозы на 12-й неделе и 26-й неделе (полный комплект для анализа)
Неделя 12-й
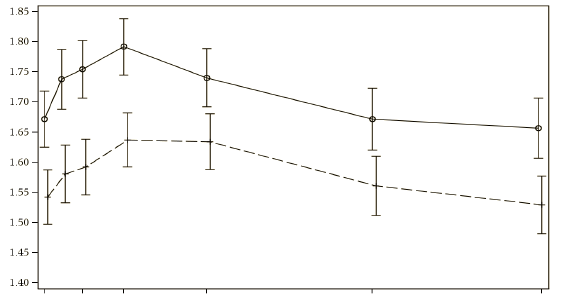
Вот в - предел среднего ОФВ1 (л)
Вот х - время (5 минут, 1:00, 2:00, 4:00, 8:00, 12:00)
лечение
Неделя 26-й
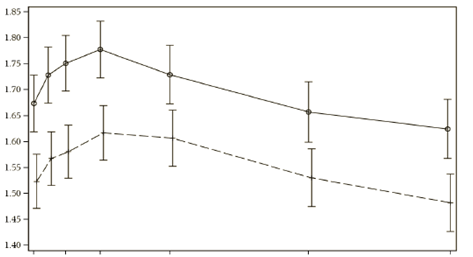
Вот в - предел среднего ОФВ1 (л)
Вот х - время (5 минут, 1:00, 2:00, 4:00, 8:00, 12:00)
лечение
В исследовании ILLUMINATE Ультибро Бризхайлер продемонстрировал значительное общее улучшение функции легких по сравнению с флутиказоном / сальметерол во всех ключевых подгруппах, включая возраст, пол, анамнез курения, тяжесть заболевания и возвратность.
Влияние на симптоматику
одышка
Ультибро Бризхайлер значительно снижал одышку согласно динамическим индексом одышки (Transitional Dyspnoea Index, TDI), он продемонстрировал клинически значимое и статистически значимое улучшение итогового балла TDI на 26-й неделе по сравнению с плацебо (разница в средних значениях по методу наименьших квадратов 1,09 р <0,001), тиотропия (разница в средних значениях по методу наименьших квадратов 0,51,
р = 0,007; SHINE) и флутиказоном / сальметерол (разница в средних значениях по методу наименьших квадратов 0,76, р = 0,003; ILLUMINATE).
Значительно более высокий процент пациентов, получавших Ультибро Бризхайлер ответили
1-бальным или более выраженным улучшением итогового балла TDI на 26-й неделе по сравнению с плацебо (68,1% и 57,5% соответственно, р = 0,004). Высокий процент пациентов продемонстрировал клинически значимый ответ на 26-й неделе применения Ультибро Бризхайлеру по сравнению с Тиотропия (68,1% против 59,2%, р = 0,016; SHINE) и флутиказоном / сальметерол (65,1% против 55,5% флутиказона / сальметерола, р = 0,88; ILLUMINATE).
Качество жизни, связанное со здоровьем
Ультибро Бризхайлер один раз в день также показал статистически значимое влияние на связанную со здоровьем качество жизни, определяется с помощью анкеты госпиталя Святого Георгия для оценки дыхательной функции (St. George's Respiratory Questionnaire, SGRQ), через 26 недель, определявшие за снижением общей оценки SGRQ по сравнению с плацебо (разница в средних значениях по методу наименьших квадратов -3,01,
р = 0,02) и тиотропия (разница в средних значениях по методу наименьших квадратов -2,13, р = 0,009; SHINE), а снижение по сравнению с индакатеролом и гликопиронием составляли -1,09 и -1,18 соответственно. Через 64 недели по сравнению с Тиотропия (разница пределы среднего -2,69, р <0,001; SPARK). На 52-й неделе снижение по сравнению с флутиказоном / сальметерол было статистически значимым (разница в средних значениях по методу наименьших квадратов -1,3, p = 0,003).
Более высокий процент пациентов, получавших Ультибро Бризхайлер, ответивших клинически значимым улучшением оценки SGRQ (определено как снижение минимум на 4 единицы по сравнению с исходным уровнем) на 26-й неделе по сравнению с плацебо (63,7% и 56,6% соответственно, р = 0,088) и тиотропия (63,7% против 56,4% тиотропий,
р = 0,047; SHINE), а на 64-й неделе по сравнению с гликопиронием и тиотропия (57,3% - Ультибро Бризхайлер по сравнению с 51,8% - гликопироний, р = 0,055, 50,8% - тиотропий,
р = 0,051; SPARK) и на 52-й неделе по сравнению с флутиказоном / сальметерол (49,2% в группе препарата Ультибро Бризхайлер против 43,7% в группе флутиказона / сальметерола, относительный риск: 1,30; p <0,001).
повседневная деятельность
Ультибро Бризхайлер продемонстрировал статистически преобладающее улучшения по сравнению с Тиотропия по проценту дней, когда пациенты в состоянии выполнять обычную повседневную работу в течение 26 недель (8,45%, р <0,001; SHINE) и показал численное улучшения по сравнению с гликопиронием (1,87, р = 0,195) и статистическое улучшение по сравнению с тиотропия (4,95, р = 0,001; SPARK).
обострения ХОБЛ
На 64-й неделе в исследовании SPARK Ультибро Бризхайлер один раз в день снижал частоту средней тяжести или тяжелого обострения ХОБЛ на 12% по сравнению с гликопиронием (р = 0,038) и на 10% по сравнению с открытым приемом тиотропия
(р = 0,096).
Кроме того, было показано, что Ультибро Бризхайлер клинически и статистически превосходил гликопироний и тиотропий в снижении частоты всех обострений ХОБЛ (легких, средней тяжести и тяжелых), со снижением частоты на 15% при применении Ультибро Бризхайлеру по сравнению с гликопиронием (р = 0,001) и на 14% по сравнению с тиотропия (р = 0,002). Количество всех обострений ХОБЛ / пациенто-лет составила 3,34 в группе препарата Ультибро Бризхайлер (2893 явления), 3,92 в группе гликопиронию (3294 явления) и 3,89 в группе тиотропия (3301 явление).
Во время 52-недельного исследования сравнения препарата Ультибро Бризхайлер
(n = 1675) и флутиказона / сальметерола (n = 1679) препарат Ультибро Бризхайлер отвечал первичной целью исследования не большей эффективности частоты всех обострений ХОБЛ (слабого, умеренной или тяжелой степени) по сравнению с флутиказоном / сальметерол. Количество всех обострений ХОБЛ / пациенто-лет составила 3,59 в группе лекарственного средства Ультибро Бризхайлер (4531 явление) и 4,03 в группе флутиказона / сальметерола
(4969 явлений). Препарат Ультибро Бризхайлер дополнительно показал большую эффективность в снижении ежегодной частоты всех обострений на 11% по сравнению с флутиказоном / сальметеролом (p = 0,003).
По сравнению с флутиказоном / сальметерол препарат Ультибро Бризхайлер снижал ежегодную частоту обострений умеренной или тяжелой степени на 17% (p <0,001) и обострений тяжелой степени (требующих госпитализации) на 13% (статистически незначимых, p = 0,231). Количество обострений ХОБЛ средней или тяжелой степени / пациенто-лет составила 0,98 в группе препарата Ультибро Бризхайлер
(1265 явлений) и 1,19 в группе флутиказона / сальметерола (1452 явления). Препарат Ультибро Бризхайлер увеличивал время до начала первых обострений умеренной или тяжелой степени при снижении риска развития обострений на 22% (p <0,001) и увеличивал время до начала первых обострений тяжелой степени при снижении риска развития обострений на 19% (p = 0,046).
Частота развития пневмонии составила 3,2% в группе препарата Ультибро Бризхайлер по сравнению с 4,8% в группе флутиказона / сальметерола (p = 0,017). Время до начала первой волны пневмонии увеличивался на фоне приема препарата Ультибро Бризхайлер сравнению с флутиказоном / сальметерол (p = 0,013).
В другом исследовании сравнения препарата Ультибро Бризхайлер (n = 258) и флутиказона / сальметерола (n = 264) продолжительностью 26 недель количество обострений ХОБЛ средней или тяжелой степени / пациенто-лет составила 0,15 против 0,18 (18 явлений на 22 явлений) , соответственно (p = 0,512), а количество всех обострений ХОБЛ / пациенто-лет (слабого, умеренной или тяжелой степени) составляла 0,72 против 0,94 (86 явлений против 113 явлений), соответственно (p = 0,098).
Гликопироний и тиотропий не показали никакой разницы в снижении риска.
Использование препаратов для неотложной терапии
Прием в течение 26 недель Ультибро Бризхайлеру один раз в сутки значительно уменьшил применения неотложной помощи (сальбутамол) на 0,96 впрыска / сутки
(р <0,001) по сравнению с плацебо и 0,54 впрыска / сутки (р <0,001) по сравнению с Тиотропия в исследовании [SHINE], а также на 0,39 впрыска / сутки (р = 0,019) по сравнению с флутиказоном / сальметерол в исследовании ILLUMINATE.
В течение 64 недель Ультибро Бризхайлер уменьшил применения неотложной помощи (сальбутамол) на 0,76 впрыска / сутки (р <0,001) по сравнению с Тиотропия в исследовании SPARK. В течение 52 недель препарат Ультибро Бризхайлер уменьшил применения препарата неотложной помощи на 0,25 впрыска / сутки по сравнению с флутиказоном / сальметерол (p <0,001).
Толерантность к физической нагрузке
В 3-недельном исследовании BRIGHT, где толерантность к физической нагрузке была протестирована с помощью велоэргометрии при субмаксимальной (75%) нагрузке (тест на толерантность к субмаксимальной нагрузки), Ультибро Бризхайлер, который применяли утром, снижал динамическую гиперинфляцию и увеличивал продолжительность нагрузки, сохранялось начиная с первой дозы. В первый день лечения объем вдоха при нагрузке значительно улучшалось (250 мл,
р <0,001) по сравнению с плацебо. После трех недель лечения улучшения объема вдоха с Ультибро Бризхайлер было больше (320 мл, р <0,001), а при физической нагрузке увеличился (59,5 с, р = 0,006) по сравнению с плацебо. Аналогичные результаты наблюдались в группе тиотропия.
Измерения с помощью общей плетизмографии остаточного объема (С) и функционального остаточного объема (ФЗО) позволяет получить представление о закрытии дыхательных путей и отражает наличие «ловушек воздух», что считается отличительной чертой ХОБЛ. В первый день лечения через 60 минут после введения дозы Ультибро Бризхайлер уменьшил ЗО на 380 мл (р <0,001) по сравнению с плацебо и ФЗО на 350 мл
(р <0,001) по сравнению с плацебо. На 21-й день через 60 минут после введения дозы отмечали дальнейшее сокращение ЗО на 520 мл (р <0,001) и ФЗО на 520 мл (р <0,001).
Детская популяция
Европейское агентство по лекарственным средствам отказалось от требования предоставить результаты исследований Ультибро Бризхайлеру во всех подгруппах педиатрических пациентов с ХОБЛ.
Фармакокинетика .
всасывания
Ультибро Бризхайлер
После ингаляции лекарственного средства Ультибро Бризхайлер медиана времени до достижения максимальной концентрации в плазме крови индакатеролу и гликопиронию составляла примерно 15 минут и 5 минут соответственно.
На основании данных исследований in vitro ожидается, что доза индакатеролу, доставлена в легкие, будет одинаковой при применении Ультибро Бризхайлеру и индакатеролу 150 мкг в монотерапии. Стационарная экспозиция индакатеролу после ингаляции Ультибро Бризхайлеру была или такой же, или чуть ниже, чем системная экспозиция после ингаляции индакатеролу 150 мкг в монотерапии.
Биодоступность индакатеролу после ингаляции Ультибро Бризхайлеру была в пределах от 61 до 85%, тогда как в гликопиронию - около 47% от доставленной дозы.
Стационарная экспозиция гликопиронию после ингаляции Ультибро Бризхайлеру была подобна системной экспозиции гликопиронию после ингаляции 50 мкг препарата в монотерапии.
Индакатерол
Концентрации индакатеролу в сыворотке увеличивались с повторным применением один раз в сутки. Стационарное состояние достигается в течение 12-15 дней. Среднее соотношение накопления индакатеролу, то есть AUC в течение 24-часового интервала дозирования на 14 день или 15 день по сравнению с 1-й днем находилось в диапазоне от 2,9 до 3,8 при ингаляции 1 раз в сутки в дозах от 60 мкг до 480 мкг (доставленной дозы).
Гликопироний
У пациентов с ХОБЛ фармакокинетический стационарное состояние гликопиронию достигался в течение одной недели после начала лечения. Стационарная средняя максимальная и минимальная плазменная концентрация гликопиронию при применении в рекомендуемой дозе 1 раз в сутки составляла 166 пг / мл и 8 пг / мл соответственно. Стационарная экспозиция гликопиронию (AUC в течение 24-часового интервала дозирования) была примерно в
1,4 -1,7 раза выше, чем после первой дозы.
распределение
Индакатерол
После введения объем распределения индакатеролу на этапе конечной элиминации составлял 2557 литров, что указывает на экстенсивное распределение. Связывание с белками плазмы и сыворотки человека in vitro составляло около 95%.
Гликопироний
После введения стационарный объем распределения гликопиронию составил 83 литра, а объем распределения в терминальной фазе - 376 литров. Объем распределения в терминальной фазе после ингаляции был почти в 20 раз больше, отражающий значительно медленную элиминацию после ингаляции. Связывание с белками плазмы и сыворотки человека in vitro составляло от 38% до 41% при концентрации от 1 до
10 нг / мл.
Метаболизм
Индакатерол
После приема радиоактивно меченого индакатеролу в исследовании ADME (всасывание, распределение, метаболизм, экскреция) у людей неизмененный индакатерол был основным компонентом в сыворотке крови и составил примерно одну треть от общей связанной с препаратом AUC в течение 24 часов. Гидроксилированных производная была самым значительным метаболитом в плазме крови. Фенольные в глюкуронидов индакатеролу и гидроксилированного индакатеролу были следующими значимыми метаболитами. Диастереомер гидроксилированного производного - N-глюкуронид индакатеролу, а также С и N-деалкильовани продукты были идентифицированы среди других метаболитов.
In vitro изоформа UGT1A1 является основным источником метаболического клиренса индакатеролу. Однако, как показано в клиническом исследовании у популяций с разными генотипами UGT1A1, генотип UGT1A1 незначительно влияет на системную экспозицию индакатеролу. Окислительные метаболиты были обнаружены при инкубации с рекомбинантными CYP1A1, CYP2D6 и CYP3A4. Установлено, что CYP3A4 является предпочтительным изоферментом, ответственным за гидроксилирование индакатеролу. Исследования in vitro в дальнейшем показали, что индакатерол имеет низкое сродство к субстрату для ефлюкснои помпы P-gp.
Гликопироний
Исследования метаболизма in vitro показали подобные метаболические пути для гликопиронию бромида у животных и людей. Гидроксилирования обуславливает образование различных моно и
бес-гидроксилированных метаболитов, а прямой гидролиз приводит к образованию производного карбоновой кислоты (М9). I n vivo М9 образуется из проглоченной фракции ингальованого гликопиронию бромида. Глюкуронид и / или сульфатные конъюгаты гликопиронию были найдены в моче людей после повторных ингаляций, что составляет около 3% от дозы.
Ряд изоферментов CYP способствовали окислительной биотрансформации гликопиронию. Ингибирования или индуцирования метаболизма гликопиронию вряд ли приводить к существенным изменениям системной экспозиции активного вещества.
Исследование ингибирования in vitro показали, что гликопиронию бромид не имеет значимой способности подавлять CYP1A2, CYP2A6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 или CYP3A4 / 5, ефлюкс-транспортеры MDR1, MRP2 или MXR и транспортеры захвата OCT1 или OCT2. Исследование индукции ферментов in vitro не выявили клинически значимого индукции гликопиронию бромидом любого из тестируемых изоферментов цитохрома Р450 или UGT1A1 и транспортеров MDR1 и MRP2.
Выведение
Индакатерол
В клинических исследованиях, которые включали сбор мочи, количество индакатеролу, что выводится в неизмененном виде с мочой, была в целом ниже, чем 2,5% от доставленной дозы. Почечный клиренс индакатеролу составлял, в среднем, от 0,46 до 1,2 л / час. По сравнению с сывороточным клиренсом индакатеролу 23,3 л / ч очевидно, что почечный клиренс играет незначительную роль (от 2 до 5% от системного клиренса) в элиминации системно доступного индакатеролу.
В исследовании ADME индакатеролу, что применялся перорально, фекальный путь экскреции доминировал над мочевым путем. Индакатерол выводился с калом в основном в виде неизмененной исходного вещества (54% от дозы) и в меньшей степени в виде гидроксилированных метаболитов индакатеролу (23% от дозы). Баланс массы был полным,
≥ 90% дозы находили в экскрементах.
Концентрации индакатеролу в сыворотке снижались многофазным образом со средним периодом полувыведения в пределах от 45,5 до 126 часов. Эффективный период полувыведения, рассчитанный по накоплением индакатеролу после многократного применения, колебался от 40 до 52 часов, что согласуется с наблюдаемым время к стационарному состоянию - примерно 12-15 дней.
Гликопироний
После внутривенного введения [3H] -миченого гликопиронию бромида человеку средняя экскреция радиоактивности в течение 48 часов составила 85% от дозы. Еще 5% дозы было выявлено в желчи.
Почечная экскреция исходного препарата составляла примерно 60-70% от общего клиренса системно доступного гликопиронию, в то время как нениркови процессы клиренса составляли около 30-40%. Желчный клиренс является составной непочечный клиренса, но в основном непочечный клиренс, как полагают, связан с метаболизмом.
Средний почечный клиренс гликопиронию после ингаляции находился в диапазоне от 17,4 до 24,4 л / час. Активная канальцевая секреция способствует почечной экскреции гликопиронию. До 23% от доставленной дозы обнаружено в моче как исходный препарат.
Концентрации гликопиронию в плазме снизились многофазным образом. Средний терминальный период полувыведения был гораздо дольше после ингаляции (от 33 до
57 часов), чем после (6,2 часа) и перорального (2,8 часа) введения. Модель элиминации предусматривает длительную легочную абсорбцию и / или переход гликопиронию в системный кровоток в течение 24 часов после ингаляции и больше.
Линейность / нелинейность
Индакатерол
Системная экспозиция индакатеролу увеличивалась при повышении дозы (доставленной) (120 мкг - 480 мкг) пропорционально дозе.
У больных ХОБЛ как системная экспозиция, так общая экскреция с мочой гликопиронию в фармакокинетически стационарном состоянии увеличились примерно дозопропорцийно в диапазоне доз от 44 до 176 мкг.
особые популяции
Ультибро Бризхайлер
Популяционный фармакокинетический анализ данных у больных ХОБЛ после ингаляции Ультибро Бризхайлеру не указал ни одного существенного влияния возраста, пола и (безжировой) массы тела в системное воздействие индакатеролу и гликопиронию. Безжировая масса тела (которая является функцией массы и роста) была определена как ковариата. Наблюдалась отрицательная корреляция между системным воздействием и безжировой массой тела (или массой тела), однако коррекция дозы не рекомендуется в связи с величиной изменения или прогнозной погрешностью безжировой массы тела.
Курение и базовый ОФВ1 не имели очевидного влияния на системную экспозицию индакатеролу и гликопиронию после ингаляции Ультибро Бризхайлеру.
Индакатерол
Популяционный фармакокинетический анализ показал, что нет ни одного клинически значимого влияния возраста (взрослые до 88 лет), пола, массы тела (32-168 кг) или расы на фармакокинетику индакатеролу. Не предполагала никакой разницы между этническими подгруппами в этой популяции.
В связи с очень низким вкладом мочевого пути к полной экскреции, исследования у пациентов с нарушением функции почек не проводили.
Гликопироний
В популяционном фармакокинетического анализа данных в отношении больных ХОБЛ массу тела и возраст определен как факторы индивидуальной изменчивости системной экспозиции. Гликопироний в рекомендованной дозе можно безопасно применять во всех возрастных группах и группах по массе тела.
Пол, курение и базовый ОФВ1 не имели явного влияния на системную экспозицию.
Пациенты с нарушением функции печени
Ультибро Бризхайлер
Исходя из клинических фармакокинетических характеристик компонентов Ультибро Бризхайлеру в монотерапии, его могут применять в рекомендуемой дозе пациенты с легкой и средней тяжести нарушением функции печени. Нет данных по пациентов с тяжелым нарушением функции печени.
Индакатерол
У пациентов с легкой и средней тяжести нарушением функции печени не обнаружено ни значимых изменений Cmax или AUC индакатеролу, ни разницы в связывании белка по сравнению со здоровыми людьми из группы контроля. Исследование с участием пациентов с тяжелым нарушением функции печени не проводились.
Гликопироний
Клинические исследования не были проведены у пациентов с печеночной недостаточностью. Гликопироний выводится преимущественно из большого круга кровообращения путем почечной экскреции. Считается, что нарушение печеночного метаболизма гликопиронию не влечет клинически значимого увеличением системной экспозиции.
Пациенты с нарушением функции почек
Ультибро Бризхайлер
Исходя из клинических фармакокинетических характеристик компонентов Ультибро Бризхайлеру в монотерапии, его могут применять в рекомендуемой дозе пациенты с легкой и средней тяжести нарушением функции почек.
Больным с тяжелым нарушением функции почек или терминальной стадией болезни почек, которые требуют диализа, Ультибро Бризхайлер следует применять, только если ожидаемая польза превышает потенциальный риск.
Индакатерол
В связи с очень низким вкладом мочевого пути к полной элиминации индакатеролу малеата из организма исследования с участием пациентов с нарушением функции почек не проводили.
Гликопироний
Нарушение функции почек влияет на системную экспозицию гликопиронию бромида. Умеренное среднее увеличение общей системной экспозиции (AUCостаннього) до 1,4 раз было отмечено у пациентов с легкой и средней тяжести нарушением функции почек и до 2,2 раза у пациентов с тяжелым нарушением функции почек или терминальной стадией болезни почек. Больным ХОБЛ с легкой и средней тяжести нарушением функции почек (скорость клубочковой фильтрации (СКФ) ≥ 30 мл / мин /
1,73 м2) гликопиронию бромид можно применять в рекомендуемой дозе.
Этническая принадлежность
Ультибро Бризхайлер
После коррекции на безжировую массу тела не было установлено статистически значимого влияния этнической принадлежности (японцы по сравнению с неяпонцы) на экспозицию обоих соединений.
Индакатерол
Никакой разницы между этническими подгруппами обнаружено не было. Опыт лечения пациентов негроидной популяции ограничен.
Гликопироний
Не было никаких существенных различий в общей системной экспозиции (AUC) между японскими пациентами и пациентами европеоидной расы. Фармакокинетические данные по других национальностей или рас недостаточны.
Доклинические данные по безопасности
Ультибро Бризхайлер
Влияние лекарственного средства Ультибро Бризхайлер на частоту сердечных сокращений увеличивался по величине и продолжительности по сравнению с влиянием, наблюдается при применении каждого компонента в отдельности. Сокращение электрокардиографических интервалов, которые отражают увеличение частоты сердечных сокращений и снижение систолического и диастолического артериального давления, также проявляли после лечения Ультибро Бризхайлером. Индакатерол, который вводили собакам отдельно или в комбинации как Ультибро Бризхайлер, вызывал аналогичную частоту и тяжесть поражения миокарда. Системная экспозиция (AUC) в концентрации, в которой не наблюдается неблагоприятного воздействия (NOAEL), была в 64 и 59 раз выше, чем у человека при приеме дозы 110 мкг / 50 мкг, для каждого компонента соответственно.
В исследованиях на крысах не замечено никакого влияния на эмбрион или плод на любом дозовой уровне Ультибро Бризхайлеру.
Индакатерол
Влияние на сердечно-сосудистую систему был связан с β2-агонистического свойствами индакатеролу, в частности с тахикардией, аритмией и поражением миокарда у собак. Легкое раздражение полости носа и гортани наблюдалось у грызунов. Все эти нарушения были при экспозиции, выше чем та, которую ожидают в людей.
Хотя индакатерол не влиял на общие репродуктивные характеристики в исследовании фертильности крыс наблюдали снижение количества беременных в поколении F1 при экспозиции в 14 раз выше, чем у людей, которых лечили индакатеролом. Индакатерол не имел эмбриотоксического или тератогенного действия на крыс или кроликов.
Исследование генотоксичности не выявили мутагенного или кластогенного потенциала. Гликопироний
Доклинические данные не обнаружили особой опасности для людей на основе традиционных исследований фармакологии безопасности, токсичности повторных доз, генотоксичности, канцерогенного потенциала, токсичности для репродукции и развития.
Гликопироний ни проявлял тератогенных свойств у крыс и кроликов после ингаляции. Фертильность и пре- и постнатальное развитие не нарушались у крыс. Гликопиронию бромид и его метаболиты существенно не проникают через плацентарный барьер беременных мышей, кроликов и собак. Гликопиронию бромид (в том числе его метаболиты) проникает в молоко крыс и достигает концентрации, в 10 раз более высокой, чем в крови самок.
Исследование генотоксичности не выявили мутагенного или кластогенного потенциала гликопиронию бромида. Исследование канцерогенности у трансгенных мышей с использованием перорального введения и использования ингаляции у крыс не обнаружили никаких доказательств канцерогенности при системной экспозиции препарата (AUC) у мышей примерно в 53 раз выше и у крыс в 75 раз выше, чем при максимальной рекомендуемой дозе один раз в день у человека.
Клинические характеристики
Ультибро Бризхайлер Показания
Поддерживающая бронхолитическое терапия для облегчения симптомов и снижению частоты обострений у взрослых пациентов с хроническими обструктивными заболеваниями легких (ХОБЛ).
Противопоказания
Повышенная чувствительность к действующему веществу, лактозы или к любой из вспомогательных веществ.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Одновременное применение индакатеролу и гликопиронию в препарате Ультибро Бризхайлер, когда обе действующие вещества находятся в стационарном состоянии, не влияет на фармакокинетику других лекарственных средств.
Специальные исследования взаимодействия с Ультибро Бризхайлером не проводились. Информация о возможных взаимодействия основывается на свойствах каждого из компонентов.
Взаимодействия, связанные с индакатеролом
Не было выявлено, что индакатерол является причиной взаимодействия с другими лекарственными средствами. Исследования in vitro показали, что потенциал индакатеролу вызвать метаболические взаимодействия с лекарственными средствами в системных экспозициях, достигаемые в клинической практике, является незначительным.
Взаимодействия, связанные с гликопиронием
Исследования in vitro показали, что гликопироний не угнетает и не стимулирует метаболизм других активных веществ или процессов с участием транспортеров лекарств. Метаболизм, в котором участвуют несколько ферментов, играет второстепенную роль в элиминации гликопиронию. Ингибирования или индукция метаболизма гликопиронию вряд ли приведет к релевантных изменений системной экспозиции активного вещества.
Не рекомендуется одновременное применение с:
Бета-адреноблокаторами: бета-адреноблокаторы могут ослаблять или противодействовать эффекта β2-агонистов. Поэтому Ультибро Бризхайлер не следует назначать вместе с бета-адреноблокаторами (включая глазные капли), если нет веских причин для их применения. При необходимости следует отдать предпочтение кардиоселективным бета-адреноблокаторы, хотя их следует применять с осторожностью.
Антихолинергическими средствами:
Одновременное применение Ultibro Breezhaler с другими антихолинергическими лекарственными средствами не изучалось и поэтому не рекомендуется (см. Раздел «Особенности применения»).
Симпатомиметиками: одновременное применение других симпатомиметиков (отдельно или в составе комбинированной терапии) может усиливать побочные эффекты индакатеролу.
Необходимо с осторожностью применять одновременно с:
Гипокалиемический средствами: одновременное применение с гипокалиемический средствами из группы производных метилксантина, стероидами или некалийзберигаючимы диуретиками может усиливать гипокалиемический эффекты β2-агонистов, поэтому их следует применять с осторожностью.
Учитывать при одновременном применении
Метаболические и транспортные взаимодействия: ингибирование ключевых участников клиренса индакатеролу - CYP3A4 и Р-гликопротеина - повышает системную экспозицию индакатеролу до двух раз. Увеличение экспозиции за счет взаимодействия не вызывает проблем с безопасностью, учитывая опыт безопасности лечения индакатеролом в клинических исследованиях до одного года в дозе, в два раза выше максимальной рекомендованной дозы индакатеролу.
Циметидин и другие ингибиторы транспорта органических катионов: в клинических исследованиях у здоровых добровольцев циметидин - ингибитор транспорта органических катионов, который, как считается, способствует почечной экскреции гликопиронию - увеличивал общую экспозицию (AUC) гликопиронию на 22% и снижает почечный клиренс на
23%. Таким образом, клинически значимых лекарственных взаимодействий не ожидается, если гликопироний применяют одновременно с циметидином или другими ингибиторами транспорта органических катионов.
Особенности применения
Астма
Препарат Ультибро Бризхайлер не следует применять для лечения бронхиальной астмы из-за отсутствия данных по этому показания.
Агонисты β2-адренорецепторов длительного действия могут повышать риск серьезных нежелательных явлений, связанных с астмой, включая летальный исход, при использовании для лечения бронхиальной астмы.
Не предназначен для применения при острых состояниях
Ультибро Бризхайлер назначают один раз в сутки для долгосрочной поддерживающей терапии. Препарат не предназначен для первоначального лечения острых эпизодов бронхоспазма, то есть как неотложная терапия.
гиперчувствительность
Сообщалось о реакции гиперчувствительности немедленного типа после применения индакатеролу или гликопиронию, которые входят в состав препарата Ультибро Бризхайлер. Если есть признаки развития аллергической реакции, в частности, ангионевротический отек (затруднение дыхания или глотания, отек языка, губ и лица) крапивница или сыпь на коже, лечение следует немедленно прекратить и назначить альтернативную терапию.
Парадоксальний бронхоспазм
Как и при применении другой ингаляционной терапии, применение препарата Ультибро Бризхайлер может привести к развитию парадоксального бронхоспазма, может быть опасным для жизни. Если возникает парадоксальный бронхоспазм, применение препарата Ультибро Бризхайлер необходимо немедленно прекратить и начать альтернативную терапию.
антихолинергический эффект
Как и другие антихолинергические лекарственные средства, Ультибро Бризхайлер следует применять с осторожностью пациентам с закрытоугольной глаукомой или с задержкой мочи.
Пациенты должны быть проинформированы о симптомах острой закрытоугольной глаукомы и необходимости отмены препарата Ультибро Бризхайлер, а также о необходимости немедленно связаться со своим врачом в случае появления каких-либо из этих симптомов.
задержка мочи
Нет данных по пациентов с задержкой мочи, таким образом, препарат Ультибро Бризхайлер следует с осторожностью применять этим пациентам.
Пациенты с нарушением функции почек тяжелой степени
Умеренное повышение общего системного воздействия (AUClast) гликопиронию в 1,4 раза наблюдалось у пациентов с легкой и умеренным нарушением функции почек в 2,2 раза у пациентов с тяжелым нарушением функции почек или заболеванием почек в терминальной стадии.
Пациентам с нарушением функции почек тяжелой степени (оценена скорость клубочковой фильтрации ниже 30 мл / мин / 1,73 м2), включая пациентов с заболеванием почек в терминальной стадии, требующие проведения диализа, Ультибро Бризхайлер следует применять, только если ожидаемая польза превышает потенциальный риск . По этим пациентами необходимо внимательно наблюдать относительно появления возможных нежелательных реакций на препарат.
Влияние на сердечно-сосудистую систему
Препарат Ультибро Бризхайлер следует с осторожностью применять пациентам с нарушением сердечно-сосудистой системы (ишемическая болезнь сердца, острый инфаркт миокарда, нарушения сердечного ритма, артериальная гипертензия).
Агонисты β2-адренорецепторов могут вызвать клинически значимое влияние на сердечно-сосудистую систему в некоторых пациентов, определяется повышением частоты пульса, повышением АД и / или другими симптомами. Если это влияние возникает на фоне применения препарата, может возникнуть необходимость в отмене препарата. Кроме этого, сообщалось, что агонисты β2-адренорецепторов приводят к изменениям на ЭКГ (ЭКГ), таким как сглаживание зубца Т, удлинение интервала QT и депрессия сегмента ST, хотя клиническая значимость этих наблюдений неизвестна. Таким образом, агонисты β2-адренорецепторов длительного действия следует с осторожностью применять пациентам с установленным или подозреваемым удлинением интервала QT или которые получают лекарственные средства, влияющие на интервал QT.
Пациенты с нестабильной стенокардией при ишемической болезни сердца, левожелудочковой недостаточностью, перенесенным инфарктом миокарда, аритмии (за исключением хронической стабильной фибрилляции предсердий), синдромом удлиненного интервала QT в анамнезе или с пролонгацией QTc интервала (по методу Фридерика) (> 450 мс), были исключены по клиническим исследованиям, таким образом, опыт применения препарата этим группам пациентов отсутствует. Лекарственное средство Ультибро Бризхайлер следует с осторожностью применять этим группам пациентов.
гипокалиемия
Агонисты β2-адренорецепторов могут вызвать выраженную гипокалиемию у некоторых пациентов, что может привести к развитию побочных эффектов со стороны сердечно-сосудистой системы. Снижение уровня калия в плазме крови обычно временное и не требует его пополнения. У пациентов с ХОБЛ тяжелой степени гипокалиемии может быть усилено гипоксией и сопутствующим лечением, что может повысить склонность к нарушению сердечного ритма.
Клинически значимые эффекты гипокалиемии не отмечены в клинических исследованиях препарата Ультибро Бризхайлер при применении в рекомендованных терапевтических дозах.
гипергликемия
Ингаляция высоких доз агонистов β2-адренорецепторов может вызвать повышение уровня глюкозы в плазме крови. После начала лечения Ультибро Бризхайлер следует более тщательно контролировать уровень глюкозы в плазме крови у пациентов с сахарным диабетом.
Во время длительных клинических исследований клинически значимые изменения уровня глюкозы в плазме крови были более частыми у большинства пациентов, принимавших препарат Ультибро Бризхайлер, (4,9%) в рекомендованных дозах, чем у тех, кто принимал плацебо (2,7%). Влияние Ультибро Бризхайлер не изучались у пациентов с недостаточно контролируемым сахарным диабетом.
общие нарушения
Препарат Ультибро Бризхайлер следует с осторожностью применять пациентам с судорожными расстройствами или тиреотоксикозом и пациентам, которые неадекватно реагируют на воздействие агонистов β2-адренорецепторов.
вспомогательные вещества
Пациентам с редкими наследственными проблемами непереносимости галактозы, дефицита лактазы Лаппа или глюкозо-галактозной мальабсорбции не следует принимать этот препарат.
Применение в период беременности или кормления грудью
беременность
Данные по применению препарата Ультибро Бризхайлер беременным женщинам отсутствуют. Индакатерол может замедлять роды за счет расслабляющего действия, которое он оказывает на гладкую мускулатуру матки. Поэтому препарат Ультибро Бризхайлер следует применять во время беременности только в случаях, если ожидаемая польза для матери превышает потенциальный риск для плода.
кормление грудью
Неизвестно, индакатерол, гликопироний и их метаболиты экскретируются в грудное молоко. Вопрос о применении препарата Ультибро Бризхайлер кормления грудью, следует рассматривать только в том случае, если ожидаемая польза для больше, чем риск для ребенка.
фертильность
Данные исследований репродуктивной функции и другие данные, полученные в результате опытов на животных, не вызывают беспокойства относительно фертильности как мужчин, так и женщин.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Ультибро Бризхайлер не влияет, или оказывает незначительное влияние на способность управлять автотранспортом или работать с механизмами. Однако, возникновение головокружения может влиять на способность управлять автотранспортом или работать с механизмами (см. Раздел «Побочные реакции).
Способ применения Ультибро Бризхайлер и дозы
дозировка
Рекомендуемая доза - ингаляция содержимого одной капсулы с помощью ингалятора Ультибро Бризхайлер один раз в сутки.
Ультибро Бризхайлер рекомендуется применять один раз в сутки в одно и то же время каждый день. Если прием дозы пропущен, следующую дозу следует принять как можно скорее. Пациенты должны знать, что нельзя принимать больше одной дозы в сутки.
Пациенты пожилого возраста
Пациенты пожилого возраста (старше 75 лет) могут применять Ультибро Бризхайлер в рекомендованной дозе.
Нарушение функции почек
Пациенты с нарушением функции почек легкой и средней степени тяжести могут применять Ультибро Бризхайлер в рекомендованной дозе. Пациентам с тяжелым нарушением функции почек или с заболеванием почек в терминальной стадии, требующие проведения диализа, Ультибро Бризхайлер следует применять, только если ожидаемая польза превышает потенциальный риск.
Нарушение функции печени
Пациенты с нарушением функции печени легкой и средней степеней тяжести могут применять Ультибро Бризхайлер в рекомендованной дозе. Данные по применению Ультибро Бризхайлер пациентам с тяжелым нарушением функции печени отсутствуют.
способ применения
Только для ингаляционного применения.
Капсулы Ультибро Бризхайлер следует применять только с помощью ингалятора Ультибро Бризхайлер.
Пациенты должны быть проинструктированы относительно правильного применения препарата.
Как применять ингалятор
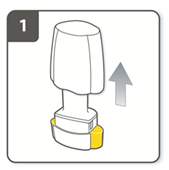
| Снять колпачок. |
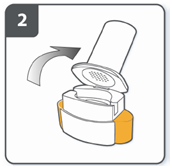
| Открыть ингалятор: прочно удерживать основу ингалятора и наклонить мундштук. Ингалятор открыт. |
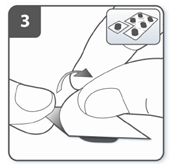
| Подготовить капсулу: отделить один блистер от блистерной упаковки, оторвав его по линии перфорации. Взять один блистер и снять защитную подложку для того, чтобы открыть капсулу. НЕ выжимать капсулу через фольгу. |
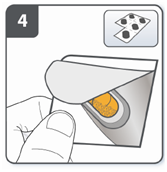
| Вынуть капсулу: капсулы следует всегда хранить в блистере и вынимать только перед применением. Сухими руками вынуть капсулу из блистера. Капсулу глотать. |
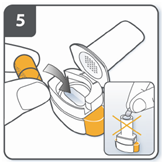
| Вставить капсулу: поместить капсулу в камеру для капсулы. Никогда не размещайте капсулу непосредственно в мундштуке. |
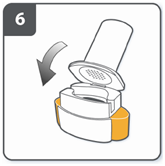
| Закрыть ингалятор: закрыть ингалятор к «щелчок». |
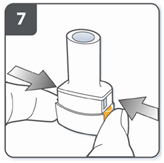
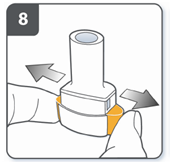
| Проколоти капсулу: держать ингалятор в вертикальном положении так, чтобы мундштук был направлен вверх. Проколоть капсулу путем одновременного сильного нажатия на обе боковые кнопки. Сделать это только один раз. В тот момент, когда капсула проколется, Вы должны услышать щелчок. |
| Полностью отпустить боковые кнопки. |
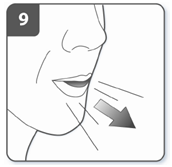
| Видихнути: прежде чем поместить мундштук в рот, сделать полный выдох. Не дуйте в мундштук. |
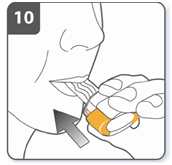
| Вдохнуть лекарственное средство: для того, чтобы лекарственное средство попал глубоко в Ваших дыхательных путей, необходимо держать ингалятор, как это показано на рисунке. Боковые кнопки должны быть расположены перед Вами слева и справа. Не стеснять боковые кнопки. Поместить мундштук в рот и плотно сжать губы вокруг него. Сделать быстрый, но равномерный вдох так глубоко, как только Вы можете. Не будет нажата на боковые кнопки. |
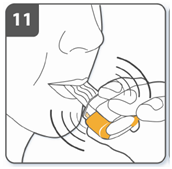
| Примечание: при вдыхании через ингалятор капсула вращается в камере, и Вы должны услышать жужжание. Вы почувствуете сладкий аромат, как только лекарства начнут попадать в Ваших легких. Если Вы не слышите жужжание: капсулу может заклинить в камере. Если это случится: открыть ингалятор и осторожно освободить капсулу, постукивая по основанию ингалятора. Не будет нажата на боковые кнопки. Опять вдохнуть лекарство, повторив пункты 9 и 10. |
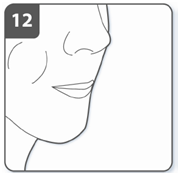
| Задержать дыхание: после того, как Вы вдохнули лекарства: задержать дыхание крайней мере на 5-10 секунд или на сколько сможете не испытывая неудобства, одновременно вынимая ингалятор изо рта. Затем сделать выдох. Открыть ингалятор и проверить капсулу на остатки порошка. Если в капсуле остался порошок: закрыть ингалятор. Повторить пункты от 9 до 12. Большинство людей может опорожнить капсулу одним или двумя вдохами. Дополнительная информация Некоторые люди могут иногда непродолжительное время кашлять сразу после вдыхания лекарственного средства. Если такое случилось с вами, не волнуйтесь. Если капсула пуста, Вы получили достаточное количество лекарственного средства. |
| После завершения приема Вашей суточной дозы Ультибро Бризхайлер: снова открыть мундштук и удалить пустую капсулу, наклоняя камеру, чтобы капсула выпала. Пустую капсулу выбросить в бытовые отходы. Закрыть ингалятор и вставить на место колпачок. Не хранить капсулы в ингаляторе Ультибро Бризхайлер. |
Дети
Препарат не предназначен для применения у детей.
Передозировка
Передозировка может привести к появлению усиленных эффектов, типичных для
β2-адренергических стимуляторов, таких как тахикардия, тремор, сердцебиение, головная боль, тошнота, рвота, сонливость, желудочковая аритмия, метаболический ацидоз, гипокалиемия и гипергликемия. Также могут возникать антихолинергические эффекты, такие как повышение внутриглазного давления (боль, нарушение зрения или покраснение глаз), запор или трудности с опорожнением. Показано поддерживающее и симптоматическое лечение. В серьезных случаях пациентов следует госпитализировать. Использование кардиоселективных бета-адреноблокаторов может рассматриваться для лечения бета-адренергических эффектов, но только под наблюдением врача и с особой осторожностью, поскольку применение бета-адреноблокаторов может спровоцировать бронхоспазм.
В исследованиях разовой дозы с участием здоровых добровольцев 4-кратная терапевтическая доза Ультибро Бризхайлеру (четыре дозы по 50 мкг / 110 мкг в час) хорошо переносилась, существенно не влияя на сердечный ритм, интервал QTc, уровень калия в сыворотке крови и уровень глюкозы в крови . У пациентов с ХОБЛ, получавших дозы до 600 мкг / 100 мкг препарата в течение двух недель, не было отмечено никаких значимых эффектов на сердечный ритм, интервал QTc, уровень глюкозы и калия в крови. Наблюдалось увеличение частоты желудочковых ектопий после 14 дней применения 300 мкг / 100 мкг и 600 мкг / 100 мкг лекарственного средства Ультибро Бризхайлер, но низкая частота и небольшое количество пациентов (N = 49 и N = 51 при применении 600 мкг / 100 мкг и 300 мкг / 100 мкг лекарственного средства Ультибро Бризхайлер соответственно) исключает точный анализ.
Дополнительная информация, связанная с индакатеролом
У пациентов с ХОБЛ, получавших разовую дозу в 10 раз превышала максимальную рекомендованную терапевтическую дозу индакатеролу, наблюдалось умеренное повышение частоты пульса, систолического артериального давления и увеличение интервала QTc.
Дополнительная информация, связанная с гликопиронием
Высокие дозы гликопиронию могут вызвать антихолинергические симптомы, которые могут потребовать лечения. Острая интоксикация вследствие непреднамеренного проглатывания капсул гликопиронию маловероятна из-за его низкую биодоступность (около 5%). Пиковые плазменные уровни и общая системная экспозиция после введения 150 мкг гликопиронию бромид (эквивалент 120 мкг гликопиронию) у здоровых добровольцев были соответственно примерно в 50 раз и в 6 раз выше, чем пиковая и общая системная экспозиция в стационарном состоянии, достигается при применении рекомендованных доз гликопиронию, и хорошо переносились.
Побочные эффекты
Резюме профиля безопасности
Профиль безопасности базируется на опыте применения препарата Ультибро Бризхайлер и его отдельных компонентов.
Опыт изучения безопасности Ультибро Бризхайлеру состоял из экспозиции до 15 месяцев в рекомендуемой терапевтической дозе.
Препарат Ультибро Бризхайлер показал аналогичные нежелательные реакции на каждый компонент. Поскольку он содержит индакатерол и гликопироний, тип и тяжесть побочных эффектов, связанных с каждым из этих компонентов, ожидаются подобными таких в комбинации.
Профиль безопасности характеризуется типичными антихолинергическими и бета-адренорецепторами симптомами, связанными с отдельными компонентами комбинации. Другие наиболее распространенные побочные реакции, связанные с продуктом (сообщили менее 3% пациентов, применявших Ультибро Бризхайлер), были кашель, назофарингит и головную боль.
Нежелательные реакции, выявленные при клинических испытаний и постмаркетинговых исследований, приведенные по классам систем органов MedDRA. В пределах каждого класса системы органов нежелательные реакции распределены по частоте, наиболее частые первые. В каждой группе по частоте неблагоприятные реакции на лекарственное средство представлены в порядке убывания серьезности. Кроме этого, соответствующая частота возникновения каждой нежелательной реакции приведена следующим образом: очень часто (≥ 1/10); часто (от ≥ 1/100 до
<1/10); нечасто (от ≥ 1/1 000 до <1/100); редко (от ≥ 1/10 000 до <1/1 000) очень редко (<1/10 000) неизвестна частота (не может быть оценена на основе имеющихся данных).
нежелательные реакции | частота возникновения |
Инфекции и инвазии | |
Инфекции верхних дыхательных путей 2 | очень часто |
Ринофарингит 2 | Часто |
Инфекции мочевыводящих путей 2 | Часто |
Гайморит 2 | Часто |
ринит 2 | Часто |
Со стороны иммунной системы | |
гиперчувствительность 2 | Часто |
Ангионевротический отек 2 | Нечасто |
Со стороны обмена веществ и питания | |
Гипергликемия и сахарный диабет | Часто |
психические нарушения | |
бессонница 2 | Нечасто |
Со стороны нервной системы | |
головокружение 2 | Часто |
Головная боль 2 | Часто |
Парестезия 2 | редко |
Со стороны органов зрения | |
Глаукома 1 | Нечасто |
кардиологические нарушения | |
Ишемическая болезнь сердца 2 | Нечасто |
Фибрилляция предсердий 2 | Нечасто |
тахикардия 2 | Нечасто |
Сердцебиение 2 | Нечасто |
Со стороны дыхательной системы, органов грудной клетки и средостения | |
Кашель 2 | Часто |
Орофарингеальный боль, включая раздражение в горле 2 | Часто |
Парадоксальний бронхоспазм 2 | Нечасто |
дисфония 2 | Нечасто |
Носова кровотеча 2 | Нечасто |
Со стороны желудочно-кишечного тракта | |
Расстройство желудка 2 | Часто |
Зубной кариес 2 | Часто |
Гастроэнтерит 2 | Нечасто |
Сухость во рту 2 | Нечасто |
Со стороны кожи и подкожно-жировой клетчатки | |
Зуд / сыпь 2 | Нечасто |
Со стороны костно-мышечной и соединительной ткани | |
Скелетно-мышечная боль 2 | Нечасто |
Мышечный спазм 2 | Нечасто |
миалгия 2 | Нечасто |
Боль в конечностях 2 | Нечасто |
Со стороны почек и мочевыделительной системы | |
Обструкция шейки мочевого пузыря и задержка мочи 2 | Часто |
Общие нарушения и реакции в месте введения | |
пирексия 1 | Часто |
Боль в груди 2 | Часто |
Периферические отеки 2 | Нечасто |
усталость | Нечасто |
1Небажани реакции, наблюдалась при применении лекарственного средства Ультибро Бризхайлер, но не отдельных компонентов.
2 Сообщение были получены в послерегистрационный период; частота была рассчитана, исходя из опыта применения препарата при проведении клинических исследований.
Описание отдельных нежелательных реакций на препарат
Кашель был частым, но обычно легкой интенсивности.
Сообщение о подозреваемых нежелательные реакции
Сообщение о подозреваемых нежелательные реакции после регистрации лекарственного средства имеет большое значение. Это позволяет в дальнейшем контролировать соотношение польза / риск применения лекарственного средства. Работники здравоохранения должны сообщать обо всех подозреваемых нежелательные реакции через национальную систему фармаконадзора.
Срок годности Ультибро Бризхайлер
2 года.
Условия хранения Ультибро Бризхайлер
Хранить при температуре не выше 25 ° С в оригинальной упаковке для защиты от влаги. Хранить в недоступном для детей месте.
Упаковка
По 6 капсул в блистере, по 1, по 2 или по 5 блистеров в пачке вместе с одним ингалятором. Или по 6 капсул в блистере, по 5 блистеров в пачке вместе с одним ингалятором, по 3 пачки в коробке.
Категория отпуска
По рецепту.
Производитель
Новартис Фарма Штайн АГ.
Местонахождение производителя
Шаффхаусерштрассе, 4332 Штейн, Швейцария (Schaffhauserstrasse, 4332 Stein, Switzerland).
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Ультибро Бризхайлер только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- https://www.novartis.com/ - Новартис Фарма Штейн АГ
- http://www.drlz.com.ua - Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Ультибро Бризхайлер |
| Производитель: | Новартис Фарма Штейн АГ |
| Форма выпуска: | порошок для ингаляций, твердые капсулы по 110 мкг / 50 мкг по 6 капсул в блистере, по 1, по 2 или по 5 блистеров в пачке вместе с одним ингалятором в коробке по 6 капсул в блистере, по 5 блистеров в пачке вместе с одним ингалятором, по 3 пачки в коробке |
| Регистрационное удостоверение: | UA/14569/01/01 |
| Дата начала: | 02.07.2020 |
| Дата окончания: | неограниченный |
| МНН: | Indacaterol and glycopyrronium bromide |
| Условия отпуска: | по рецепту |
| Состав: | 1 капсула содержит 110 мкг индакатеролу, что соответствует 143 мкг индакатеролу малеата, что эквивалентно 85 мкг целевой дозы высвобождается, и 50 мкг гликопиронию, что соответствует 63 мкг гликопиронию бромид, что эквивалентно 43 мкг целевой дозы высвобождается |
| Фармакологическая группа: | Средства, применяемые при обструктивных заболеваниях дыхательных путей. Комбинация адренергических и антихолинергических средств. |
| Код АТХ: | R03AL04 |
| Заявитель: | Новартис Фарма АГ |
| Страна заявителя: | Швейцария |
| Адрес заявителя: | Лихтштрассе 35, 4056 Базель, Швейцария |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Нет |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Комбинированный |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| R | Средства, действующие на респираторную систему |
| R03 | Средства, применяемые при обструктивных заболеваниях дыхательных путей |
| R03A | Адренергические препараты для ингаляционного применения |
| R03AL | Адренергические в сочетании с антихолинергическими средствами |
| R03AL04 | Индакатерол и гликопиронию бромид |