- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Примовист инструкция по применению
Официальная инструкция лекарственного препарата Примовист раствор 10 мл. Описание и применение Primovist, аналоги и отзывы. Инструкция Примовист раствор утвержденная компанией производителем.
Состав
действующее вещество: динатриевая соль гадоксетовои кислоты (Gd-EOB-DTPA).
1 мл раствора для инъекций содержит 181,43 мг динатриевой соли гадоксетовои кислоты (Gd-EOB-DTPA) (эквивалентно 0,25 ммоль).
Вспомогательные вещества: тринатриева соль калоксетовои кислоты (Ca-EOB-DTPA), трометамол, кислота соляная разведенная, натрия гидроксид, вода для инъекций.
Лекарственная форма
Раствор для инъекций.
Основные физико-химические свойства: прозрачный раствор, не содержащий включений.
Фармакологическая группа
Парамагнитные контрастные средства.
Код АТХ V08С А10.
Фармакологические свойства
Фармакологические.
механизм действия
Лекарственное средство Примовист - это парамагнитный контрастное средство для магнитно-резонансной визуализации.
Эффект усиления контрастности обусловлен гадоксетатом (Gd-EOB-DTPA), ионным комплексом, состоящим из гадолиния (iii) и лиганда етоксибензил-диетилентриамин-пентаоцтовои кислоты (EOB-DTPA). При сканировании с использованием Т1-взвешенных импульсных последовательностей сокращение времени продольной релаксации возбужденных атомных ядер, вызванное ионами гадолиния, увеличивает интенсивность сигнала и, таким образом, повышает контрастность изображения некоторых тканей.
фармакодинамические влияния
Гадоксетат натрия уменьшает время релаксации даже при низких концентрациях. При рН 7, напряженности магнитного поля 0,47 Т и температуре 40 ° С релаксивнисть r1, определяемая по влиянию на время продольной релаксации Т1 протонов в плазме составляет около 8,7 л / ммоль / с, релаксивнисть (r2), что определяется по влиянию на время продольной релаксации (Т2) составляет около 8,56 л / ммоль / с. При напряженности магнитного поля 1,5 Т и температуре 37 ° С релаксивнисть в плазме составляет: r1 = 6,9 л / ммоль / с, r2 = 8,7 л / ммоль / с. Релаксивнисть незначительно зависит от напряженности магнитного поля.
EOB-DTPA образует стабильный комплекс с парамагнитным ионом гадолиния с чрезвычайно высокой термодинамической стабильностью (log KGdl = 23,46). Gd-EOB-DTPA является гидрофильной соединением с высокой водорастворимостью и коэффициентом распределения между н-бутанола и буфером при рН 7,6 около 0,011. Через липофильностью етоксибензильного фрагмента гадоксетат натрия проявляет двухфазный принцип действия распределение в внеклеточном пространстве после болюсной инъекции с последующим селективным захватом гепатоцитами. Релаксивнисть r1 в тканях печени составляет 16,6 л / ммоль / с (при 0,47 Т), повышает интенсивность сигнала тканей печени. Далее гадоксетат натрия выводится с желчью.
Поражение с отсутствующим или пониженной функцией гепатоцитов (цисты, метастазы, большинство гепатоцеллюлярных карцином) не будут накапливать лекарственное средство Примовист. Хорошо дифференцированная гепатоцеллюлярная карцинома может содержать функционирующие гепатоциты и показывать некоторое контрастности визуализации в гепатоцитарний фазе. Поэтому необходима дополнительная клиническая информация для установления правильного диагноза.
Субстанция не проявляет каких-то выраженных угнетающее свойств относительно ферментов в клинически значимых концентрациях.
визуализация
После болюсной инъекции лекарственного средства Примовист динамическая визуализация в артериальной, портовенозний и равновесной фазах позволяет получить неодинаковую временную картину контрастирования разных типов поражений печени в качестве основы для радиологической характеристики поражений.
Контрастности паренхимы печени в ходе гепатоцитарнои фазы позволяет определить количество пораженных участков печени, их сегментарный распределение, визуализацию и границы, улучшает выявления поражений. Различения поражений печени по характеру динамики контрастности / вымывание контрастного средства позволяет получить дополнительную информацию.
Отсрочена (гепатоцитарна) фаза может исследоваться через 20 минут после инъекции, при этом период визуализации длится не менее 120 минут.
Результаты диагностики и технической эффективности в ходе клинических исследований указывают на минимальное улучшение при визуализации через 20 минут после инъекции по сравнению с периодом 10 минут после инъекции.
Период визуализации уменьшается до 60 минут в пациентов, нуждающихся в диализе, и у пациентов с повышенным уровнем билирубина (> 3 мг / дл).
Печеночная экскреция лекарственного средства Примовист вызывает контрастности желчевыводящей системы.
Физико-химические свойства готового к применению раствора лекарственного средства Примовист:
Осмоляльность при 37 ° C (мОсм / кг H2O) | 688 |
Вязкость при 37 ° C (мПа · с) | 1,19 |
Плотность при 37 ° C (г / мл) | 1,0881 |
pH | 7,4 |
педиатрические пациенты
Исследования методом наблюдения были проведены с привлечением 52 педиатрических пациентов (в возрасте от 2 месяцев до 18 лет). Пациенты были направлены на магнитно-резонансную визуализацию (МРВ) печени с применением лекарственного средства Примовист для оценки подозреваемых или известных фокальных поражений печени. Дополнительная диагностическая информация была получена при сравнении магнитно-резонансных изображений печени с контрастированием и без контрастирования. Сообщалось о тяжелых побочных реакциях, однако ни одна не была оценена исследователем как связана с применением лекарственного средства Примовист через ретроспективный характер и малое количество образцов этого исследования нельзя сделать вывод об эффективности и безопасности применения лекарственного средства для детей.
Фармакокинетика.
распределение
После введения профиль «концентрация-время» динатриевой соли гадоксетовои кислоты характеризовался биекспоненцийним снижением. Динатриевая соль гадоксетовои кислоты распределяется во внеклеточном пространстве (объем распределения в равновесном состоянии около
0,21 л / кг). Субстанция проявляет незначительное связывания с белками (менее 10%). Лекарственное средство проникает через плацентарный барьер в незначительном количестве.
Натрия гадоксетат является линейным гадолиниевмисним контрастным средством (GdCA). Исследования показали, что после применения GdCA гадолиний задерживается в теле. Это включает задержку в мозге и других тканях и органах.
Применение GdCA может вызывать дозозависимое повышение интенсивности Т1-взвешенного сигнала в мозге, особенно в зубчатом ядре, бледном слое и таламусе. Повышение интенсивности сигнала и доклинические данные указывают на то, что гадолиний высвобождается из линейных гадолиниевмисних контрастных средств.
Метаболизм
Гадоксетат натрия не метаболизируется.
вывод
Динатриевая соль гадоксетовои кислоты (Gd-EOB-DTPA) в эквивалентных количествах выводится почками и через печень. Период полувыведения Gd-EOB-DTPA составлял примерно 1:00. Фармакокинетика была линейной дозе 0,4 мл / кг (100 мкмоль / кг). Общий клиренс (Cltot) составил около 250 мл / мин, в то время как почечный клиренс (Clr) составил около 120 мл / мин.
Характеристики отдельных групп пациентов
Пациенты пожилого возраста (от 65 лет). Через физиологические изменения функции почек с возрастом клиренс в плазме крови гадоксетату натрия уменьшался с 210 мл / мин у пациентов младшего возраста к
163 мл / мин у пациентов в возрасте от 65 лет. Конечный период полувыведения и системный распределение были выше у пожилых пациентов (2,3 часа и 197 мкмоль × ч / л по сравнению с 1,6 часа и
153 мкмоль × ч / л). Выведение почками введенной дозы происходит у всех пациентов в полном объеме через 24 часа, разницы между здоровыми пациентами пожилого и молодого возраста не выявлено.
Почечная и / или печеночная недостаточность. У пациентов с легкой и умеренной степенью нарушения функции печени по сравнению со здоровыми добровольцами наблюдалось повышение плазменных концентраций, периода полувыведения и выведение с мочой, а также снижение выведения через печень легкой и средней степени. Однако не наблюдалось клинически значимых различий в контрастировании печеночного сигнала. У пациентов с тяжелыми нарушениями функции печени, особенно у пациентов с аномально высокими (> 3 мг / дл) уровнем билирубина, AUC повышалась до 259 мкмоль × ч / л по сравнению с 160 мкмоль × ч / л в контрольной группе. Период полувыведения был повышен до 2,6 часа по сравнению с 1,8 часа в контрольной группе. Вывод гепатобилиарной системой значительно снижалось до 5,7% введенной дозы, а также снижалось контрастности печеночного сигнала.
У пациентов с терминальной стадией почечной недостаточности AUC повышалась в 6 раз до
903 мкмоль × ч / л, а конечный период полувыведения удлинялся до 20 часов. Гемодиализ повышает клиренс гадоксетату натрия (см. Раздел «Особенности применения»). В общем при проведении процедуры диализа в течение 3:00 около 30% дозы гадоксетату натрия был выведен из 1:00 после введения. Дополнительно к воздействию гемодиализа на клиренс значительная фракция введенной дозы гадоксетату натрия выводится в таких пациентов с желчью, на что указывает средний степень извлечения около 50% в кале в течение 4 дней (диапазон от 24,6 до 74,0%; n = 6 пациентов) .
Доклинические данные по безопасности.
В стандартных исследованиях острой и субхроническое токсичности, генотоксичности и сенсибилизирующее потенциала не было обнаружено специфического риска для человеческого организма.
Сердечно-сосудистая безопасность. Незначительное и преходящее удлинение интервала QT наблюдалось у собак при исследовании высшей дозы 0,5 ммоль / кг, что соответствует 20-кратной дозе для человека. В высоких концентрациях Gd-EOB-DTPA блокирует ген специфических калиевых каналов сердца (ген hERG) и удлиняет продолжительность потенциала действия папиллярных мышц в изолированных морских свинок. Это указывает на возможность индукции удлинение интервала QT при передозировке лекарственного средства Примовист. В исследованиях фармакологической безопасности не наблюдалось влияния на другие системы органов.
Репродуктивная токсикология и лактация. В исследованиях эмбриотоксичности у кроликов после повторного применения 0,2 ммоль / кг Gd-EOB-DTPA, что составляет 25,9-кратное (в расчете на площадь поверхности тела) или 80-кратное (в расчете на массу тела) рекомендуемую дозу для человека наблюдалась повышенная количество постимплантацийних потерь и повышенный уровень абортов. У крыс менее 0,5% внутривенно введенной дозы (0,1 ммоль / кг) радиоактивно меченого гадоксетату выделялось с грудным молоком. Абсорбция после перорального применения была очень низкой у крыс (0,4%).
Местная переносимость. Реакции местной непереносимости наблюдались лишь после введения Gd-EOB-DTPA.
Канцерогенность. Исследований канцерогенности не проводилось.
Клинические характеристики
Примовист Показания
Примовист показан для выявления очаговых поражений печени и получения дополнительных данных о характере поражений при Т1 взвешенной магнитно-резонансной визуализации (МРВ).
Примовист следует применять, только если диагностическая информация является важной и не может быть получена с помощью магнитно-резонансной визуализации (МРВ) без применения контрастного вещества и когда необходима отсрочено фаза изображения.
Лекарственное средство применяют для диагностики только путем внутривенного введения.
Противопоказания
Повышенная чувствительность к действующему веществу или к любому другому компоненту препарата.
Особые меры безопасности .
Проверка. Лекарственное средство следует тщательно осмотреть перед использованием. Лекарственное средство Примовист нельзя применять в случае значительного изменения окраски, появления твердых частиц или нарушения целостности упаковки.
Обращения. Шприцы следует вынимать из пластиковой коробки непосредственно перед применением. Колпачок следует снимать со шприца только непосредственно перед применением.
Утилизация. Неиспользованный препарат или отходы следует утилизировать в соответствии с требованиями местного законодательства.
Съемную этикетку с предварительно заполненного шприца следует наклеить на медицинскую карту пациента с целью обеспечения четкого документирования по использованию контрастных веществ, содержащих гадолиний. Следует также указать введенную дозу. Если используется электронная карта пациента, следует ввести название лекарственного средства, номер серии и дозу.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Транспортировка гадоксетату в печень может быть опосредованное транспортными полипептидами органических анионов (ТПОА). Нельзя исключать, что мощные ингибиторы ТПОА могут вызвать взаимодействие и снизить эффект контрастности печени. Однако отсутствуют клинические данные в пользу этой теории.
Исследование взаимодействия у здоровых добровольцев показали, что одновременное применение эритромицина не влияло на эффективность и фармакокинетику лекарственного средства Примовист. Клинических исследований взаимодействия с другими лекарственными средствами не проводилось.
Влияние повышенного уровня билирубина или ферритина у пациентов
Повышенные уровни билирубина или ферритина могут уменьшить эффект контрастности печени вызванный лекарственным средством Примовист (см. Раздел «Фармакологические свойства»).
Взаимодействие с диагностическими тестами
При определении содержания железа в сыворотке крови комплексометричнимы методами (например методом комплексации с фероцина) в период до 24 часов после исследования с применением лекарственного средства Примовист могут быть получены ложные значения из-за наличия свободной комплексообразующие вещества в растворе контрастного средства.
Особенности применения
Применяются общие правила безопасности, действующие при проведении магнитно-резонансной визуализации, например исключения кардиостимуляторов и ферромагнитных имплантатов.
Диагностические процедуры, которые включают применение контрастных средств, должны проводиться под наблюдением врача, имеющего опыт применения и имеет достаточные знания по проведению процедуры.
После инъекции пациент должен находиться под наблюдением минимум 30 минут, поскольку опыт применения контрастных веществ свидетельствует о том, что большинство побочных реакций проявляется именно в этот период.
Нарушение функции почек
Перед введением лекарственного средства Примовист следует проводить скрининг всех пациентов на наличие почечной дисфункции по результатам лабораторных данных.
У пациентов с острой или хронической тяжелой почечной недостаточностью (скорость клубочковой фильтрации <30 мл / мин / 1,73 м2) наблюдались случаи нефрогенного системного фиброза (НСФ), что ассоциировались с применением контрастных веществ, содержащих гадолиний. Особый риск имеют пациенты, которым проводится трансплантация печени, поскольку частота острой почечной недостаточности в этой группе высока. Из-за риска развития НСФ при применении лекарственного средства Примовист следует избегать применения лекарственного средства пациентам с тяжелой почечной недостаточностью и пациентам в периоперационном периоде трансплантации печени, кроме случаев, когда диагностическая информация крайне необходима и не может быть получена при проведении ГРО без контрастного усиления.
Гемодиализ, проведенный через короткий промежуток времени после применения лекарственного средства Примовист, может быть полезным для выведения препарата из организма. Данные по применению гемодиализа для профилактики или лечения НСФ у пациентов, которые до этого не находились на диализе, отсутствуют.
Пациенты пожилого возраста
Поскольку почечный клиренс гадобутрола у пациентов пожилого возраста может быть нарушен, особенно важным является проведение исследования о наличии почечной дисфункции у пациентов в возрасте от 65 лет.
Пациенты с сердечно-сосудистыми заболеваниями
Следует с осторожностью применять препарат Примовист пациентам с тяжелыми сердечно-сосудистыми заболеваниями из-за ограниченности данных.
Примовист не следует применять пациентам с неконтролируемой гипокалиемией.
Следует с большой осторожностью применять препарат Примовист пациентам:
- с врожденным синдромом удлиненного интервала QT в анамнезе;
- с аритмией в анамнезе при применении лекарственных средств, удлиняют сердечную реполяризацию;
- которые применяют лекарственные средства, удлиняющие сердечную реполяризацию, например антиаритмические средства класса III (амиодарон, соталол).
Применение лекарственного средства Примовист может вызвать преходящее удлинение интервала QT у отдельных пациентов (см. Раздел «Фармакологические свойства»).
гиперчувствительность
Аллергические реакции, включая шок, могут наблюдаться после введения гадолиниевмисних контрастных средств для ГРО. Большинство побочных реакций проявляется в течение 30 минут после применения контрастного средства. Однако, как и при применении других контрастных средств этого класса, могут наблюдаться отсроченные реакции в период от нескольких часов после введения до нескольких дней. Всегда должны быть наготове соответствующие препараты для лечения аллергических реакций, а также средства неотложной помощи.
Риск развития реакций гиперчувствительности выше при наличии указанных ниже состояний и заболеваний:
- реакция на предыдущие введения контрастных средств;
- бронхиальная астма в анамнезе
- аллергические реакции в анамнезе.
Решение о применении лекарственного средства Примовист пациентам со склонностью к аллергии следует принимать после особенно тщательной оценки соотношения риск / польза.
Реакции гиперчувствительности могут быть более выраженными у пациентов, применяющих бета-блокаторы, особенно при наличии бронхиальной астмы. Следует принимать во внимание, что пациенты, которые применяют бета-блокаторы, могут иметь рефрактерность к стандартной терапии реакций гиперчувствительности бета-агонистмы.
Если развилась реакция гиперчувствительности, то следует немедленно прекратить введение контрастного средства.
местная непереносимость
М введение может вызвать реакции местной непереносимости, включая фокальный некроз, поэтому рекомендуется избегать использования этого пути введения (см. Раздел «Фармакологические свойства»).
Накопление в теле
После введения натрия гадоксетату гадолиний может задерживаться в мозге и других тканях тела (кости, печень, почки, кожа) и может вызывать дозозависимое повышение интенсивности Т1-взвешенного сигнала в мозге, особенно в зубчатом ядре, бледном слое и таламусе. Клиническая значимость не известна. Для пациентов, которые будут нуждаться повторного сканирования, следует взвешивать преимущества диагностики с использованием натрия гадоксетату и потенциальное депонирование гадолиния в мозге и других тканях.
вспомогательные вещества
Это лекарственное средство содержит 11,7 мг натрия на 1 мл, а доза составляет 0,1 мл / кг массы тела. Следует принимать во внимание указанную информацию, особенно пациентам, которые придерживаются диеты с контролируемым потреблением натрия.
Применение в период беременности или кормления грудью
Беременность. Нет никаких данных клинических исследований по применению гадоксетату беременным женщинам. В исследованиях на животных при введении повторных высоких доз препарат проявлял репродуктивной токсичности (см. Раздел «Фармакологические свойства»). Лекарственное средство Примовист не рекомендуется применять в период беременности, если нет абсолютных показаний.
Лактация. Контрастные вещества, содержащие гадолиний, попадают в грудное молоко в очень незначительном количестве (см. Раздел «Фармакологические свойства»). При применении терапевтических доз не следует ожидать влияния на младенцев через незначительное количество действующего вещества, что выделяется с грудным молоком, и слабое всасывание из желудочно-кишечного тракта. Решение о продлении грудного вскармливания или его прекращения на 24 часа после применения лекарственного средства Примовист должны принимать врач и женщина, которая кормит грудью.
Фертильность. Результаты исследований на животных не показали нарушения фертильности.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Не применяется.
Способ применения Примовист и дозы
способ применения
Готовый к применению водный раствор лекарственного средства Примовист вводится в неразбавленном виде путем болюсной инъекции со скоростью около 2 мл / с. После инъекции контрастного средства внутривенную канюлю следует промыть 0,9% раствором натрия хлорида.
Информацию о визуализации см. в разделе «Фармакологические свойства».
дозировка
В диагностических целях следует применять самую низкую дозу, обеспечивающую достаточную контрастность. Доза должна быть рассчитана с учетом массы тела пациента и не должна превышать рекомендуемую дозу на килограмм массы тела, как указано в этом разделе.
Рекомендуемая доза лекарственного средства Примовист составляет:
взрослые: 0,1 мл лекарственного средства Примовист на 1 кг массы тела.
повторное дозирование
Отсутствует клиническая информация по применению повторных доз лекарственного средства Примовист.
Отдельные группы пациентов
почечная недостаточность
Следует избегать применения лекарственного средства Примовист пациентам с тяжелой почечной недостаточностью (скорость клубочковой фильтрации <30 мл / мин / 1,73м2) и пациентам в периоперационном периоде трансплантации печени, кроме случаев, когда диагностическая информация крайне необходима и не может быть получена при проведении ГРО без контрастного усиления (см. раздел «Особенности применения»). Если нельзя избежать применения лекарственного средства Примовист, доза не должна превышать 0,025 ммоль / кг массы тела. Во время одного сканирования не следует применять более чем одну дозу. Поскольку информации о повторного применения недостаточно, инъекцию лекарственного средства Примовист не следует повторять, за исключением случаев, когда период между инъекциями составляет не менее 7 дней.
Пациенты с печеночной недостаточностью
Нет необходимости в коррекции дозы.
Пациенты пожилого возраста (старше 65 лет)
Необходимости в коррекции доз для геронтологических пациентов не выявлено. При применении у пациентов пожилого возраста необходима особая осторожность (см. Раздел «Особенности применения»).
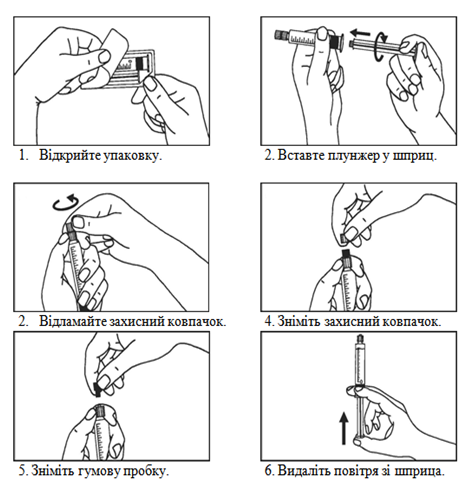
Инструкция по использованию шприца
Предварительно заполненные шприцы следует подготовить к инъекции непосредственно перед применением. Колпачок следует снимать со шприца только непосредственно перед применением. Неиспользованный препарат или отходы следует утилизировать в соответствии с требованиями местного законодательства.
Съемную этикетку с предварительно заполненного шприца следует наклеить на медицинскую карту пациента с целью обеспечения четкого документирования по использованию контрастных веществ, содержащих гадолиний. Следует также указать введенную дозу. Если используется электронная карта пациента, следует ввести название лекарственного средства, номер серии и дозу.
Дети
Безопасность и эффективность лекарственного средства Примовист не установлена для пациентов в возрасте до 18 лет, поэтому препарат не применяется в этой категории пациентов. Имеющиеся на сегодня данные приведены в разделе «Фармакологические свойства».
Передозировка
Отсутствуют сообщения о передозировке и не имеет характеристики симптомов передозировки.
Разовые дозы лекарственного средства Примовист 0,4 мл / кг (0,1 ммоль / кг) массы тела хорошо переносились. В ограниченного количества пациентов доза 0,2 мл / кг (0,5 ммоль / кг) массы тела изучалась в ходе клинических исследований; частота побочных реакций была выше, но новых побочных явлений не было обнаружено у этих пациентов.
В случае случайной передозировки рекомендуется наблюдение за пациентом, включая мониторинг сердечно-сосудистой системы. В таком случае возможна индукция удлинение интервала QT (см. Раздел «Фармакологические свойства»).
Лекарственное средство Примовист выводится путем диализа. Однако отсутствуют данные относительно того, можно ли применять гемодиализ для профилактики развития нефрогенного системного фиброза.
Побочные эффекты
Данные о профиле безопасности лекарственного средства Примовист базируются на результатах клинических исследований с участием более 1900 пациентов и постмаркетинговых наблюдениях.
Наиболее частыми побочными реакциями (≥ 0,5%) у пациентов, получавших препарат Примовист, были: тошнота, головная боль, чувство жара, повышение артериального давления, боли в спине и головокружение.
Наиболее серьезной побочной реакцией у пациентов, получавших препарат Примовист, был анафилактический шок. Отсроченные анафилактоидные реакции (в период от нескольких часов после введения до нескольких дней) наблюдались редко. Большинство побочных эффектов имели временный характер и были легкой или средней степени тяжести.
Побочные реакции, которые наблюдались при применении лекарственного средства Примовист, приведены в таблице ниже. Они классифицированы по классам систем органов (медицинский словарь регуляторной активности (MedDRA) версия 12.1). Соответствующие сроки MedDRA были использованы для описания определенных реакций, их симптомов и схожих по симптоматике состояний.
Перечисленные ниже побочные реакции, зарегистрированные в ходе клинических исследований, распределены по частоте возникновения: часто (≥ 1/100 до <1/10), нечастые (от ≥ 1/1000 до <1/100), редкие (от ≥ 1 / 10000 до <1/1000). Побочные реакции, которые были обнаружены только в период постмаркетингового наблюдения, частота которых не установлена, обозначены как «частота неизвестна». В каждой группе побочные реакции указаны в порядке убывания степени их тяжести.
Таблица. Побочные реакции, зарегистрированные в ходе клинических исследований или в период постмаркетингового наблюдения у пациентов, которым применяли препарат Примовист
система органов | частые | редкие | одиночные | частота неизвестна |
Со стороны иммунной системы | гиперсенситивный / анафилактоидные реакции (например шок *, гипотензия, фаринголарингеальная отек, крапивница, отек лица, ринит, конъюнктивит, боль в животе, гипестезия, чихание, кашель, бледность) | |||
Со стороны нервной системы | головная боль | вертиго, головокружение, дисгевзия, парестезии, паросмия | тремор, акатизия | беспокойство |
Со стороны сердца | блокада пучка Гиса, пальпитация | тахикардия | ||
Со стороны сосудов | повышение артериального давления, приливы | |||
Со стороны дыхательных путей, органов грудной клетки и средостения | расстройства со стороны дыхательных путей (одышка *, респираторный дистресс) | |||
Желудочно-кишечные расстройства | тошнота | рвота, сухость во рту | дискомфорт в ротовой полости, гиперсекреция слюны | |
Со стороны кожи и подкожной клетчатки | сыпь, зуд ** | макулопапулезная сыпь, гипергидроз | ||
Со стороны костно-мышечной и соединительной тканей | боль в спине | |||
Общие нарушения и состояние в месте инъекции | боль в груди, реакции в месте инъекции (различные виды) ***, ощущение жара, лихорадка, утомляемость, атипичные ощущения | дискомфорт, недомогание |
* Сообщалось о угрожающие жизни состояния и / или летальный исход. Эти сообщения получены в послерегистрационный период.
** зуд (генерализованный зуд, зуд глаз).
*** Реакции в месте инъекции (различные виды) включают следующие сроки: кровоизлияние в месте инъекции, жжение в месте инъекции, ощущение холода в месте инъекции, раздражение в месте инъекции, боль в месте др инъекции.
Описание отдельных побочных реакций
В ходе клинических исследований сообщалось об изменениях лабораторных показателей, такие как: повышение уровня железа в сыворотке крови, повышение уровня билирубина, повышение уровня печеночных трансаминаз, снижение уровня гемоглобина, повышение уровня амилазы, лейкоцитурия, гипергликемия, увеличение соотношения альбумин / креатинин в моче, гипонатриемия , повышение уровня неорганических фосфатов, снижение уровней белка в сыворотке крови, лейкоцитоз, гипокалиемия, повышение уровня лактатдегидрогеназы. В ходе клинических исследований регулярно проводилась ЭКГ, и у некоторых пациентов наблюдалось транзиторное удлинение интервала QT без каких-либо связанных побочных явлений.
Сообщалось о случаях нефрогенного системного фиброза (НСФ) при применении других гадолиниевмисних контрастных средств (см. Раздел «Особенности применения»).
Сообщение о подозреваемых побочные реакции
Сообщать о подозреваемых побочные реакции в период постмаркетингового наблюдения очень важно. Это дает возможность постоянно контролировать соотношение польза / риск применения лекарственного средства. Медицинские работники должны сообщать о любых подозреваемые побочные реакции.
Срок годности Примовист
5 лет.
Условия хранения Примовист
Не требует специальных условий хранения.
Несовместимость.
Поскольку исследований совместимости не проводилось, это лекарственное средство не следует смешивать с другими лекарственными средствами.
Упаковка
По 10 мл в стеклянном шприце; по 1 шприцу в прозрачной пластиковой коробке, закрытой бумагой, вложенной в картонную коробку.
Категория отпуска
По рецепту.
Производитель
Байер АГ.
Местонахождение производителя
Мюллерштрассе 178, 13353, Берлин, Германия.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Примовист только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- https://www.bayer.com - Байер АГ
- http://www.drlz.com.ua - Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Примовист |
| Производитель: | Байер АГ |
| Форма выпуска: | раствор для инъекций 0,25 ммоль/мл; по 10 мл в стеклянном шприце, по 1 шприцу в прозрачной пластиковой коробке, закрытой бумагой, вложенной в картонную коробку |
| Регистрационное удостоверение: | UA/17931/01/01 |
| Дата начала: | 06.02.2020 |
| Дата окончания: | 02.06.2025 |
| МНН: | Gadoxetic acid |
| Условия отпуска: | по рецепту |
| Состав: | 1 мл раствора для инъекций содержит 181,43 мг динатриевой соли гадоксетовои кислоты (Gd-EOB-DTPA) (эквивалентно 0,25 ммоль) |
| Фармакологическая группа: | Парамагнитные контрастные средства. |
| Код АТХ: | V08CA10 |
| Заявитель: | Байер АГ |
| Страна заявителя: | Германия |
| Адрес заявителя: | Кайзер-Вильгельм-Алее 1, 51373 Леверкузен, Германия |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Нет |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Моно |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| V | Различные средства |
| V08 | Контрастные средства |
| V08C | Контрастные средства для ямр-томографии |
| V08CA | Парамагнитные контрастные средства |
| V08CA10 | Гадоксетова кислота |

