- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Внимание! Срок действия регистрационного удостоверения UA/18362/01/01 закончился 01.04.2023
Аккофил инструкция по применению
Официальная инструкция лекарственного препарата Аккофил раствор 480 мг/0,5 мл. Описание и применение Akkofil, аналоги и отзывы. Инструкция Аккофил раствор утвержденная компанией производителем.
Состав
действующее вещество: филграстим (Г-КСФ) (с использованием генетически модифицированных бактерий Е.соli) Г-КСФ - рекомбинантный человеческий гранулоцитарный колониестимулирующий фактор;
вспомогательные вещества: кислота уксусная ледяная, натрия гидроксид в пересчете на натрий 0.02 мг, сорбит (Е 420) 25 мг, полисорбат 80, вода для инъекций.
Лекарственная форма
Раствор для инъекций в предварительно заполненных шприцах. Аккофил 30: 1 предварительно заполненный шприц (0,5 мл) содержит ЗО млн ЕД (300 мкг) филграстиму; Аккофил 48: 1 предварительно заполненный шприц (5 мл) содержит 48 млн ЕД (480 мкг) филграстима.
Фармакологическая группа
Код АТС: L03AA02.
Фармакологические свойства
Аккофил является биоподобные.
Филграстим - это высокоочищенный негликозилированные белок, состоящий из 175 аминокислот. Филграстим получают из штаммов Е. coli, которая была генетически модифицирована путем добавления гена, кодирующего человеческий гранулоцитарный колониестимулирующий фактор. Аккофил - это лекарственное средство, изготовленное биологическими / биотехнологическими методами, в основном напоминает эталонный препарат филграстима, который уже разрешен (биоподобные). В четырех различных исследованиях фазы и на здоровых добровольцах Аккофил и эталонный препарат филграстима показали сравнимую фармакокинетику (биоэквивалентность) после однократного и подкожного введения, а также после многократного подкожного введения; их фармакодинамика была также сравнимой по абсолютного числа нейтрофилов как для Стах, так и для AUCt (ИС до 95% между 80-125 °%).
Во время исследования фазы III, включавшее 110 пациентов (ПП), страдающих раком молочной железы (стадия Ila, ИИЬ или Ilia) и получают химиотерапию ТАС, Аккофил показал клиническую эффективность, сравнимую с результатами, опубликованными для эталонного препарата филграстим, что касается первичного критерия «количество дней с выраженной нейтропенией (<0,5 * · 10 9 / л), а также другие вторичные критерии оценки. Механизм действия Человеческий гранулоцитарный колониестимулирующий фактор - гликопротеин - регулирует функционально активных нейтрофилов и их выход в кровь из костного мозга. Фармакологические. Филграстим значительно увеличивает количество нейтрофилов в периферической крови уже в течение первых 24 часов после введения и одновременно приводит к некоторому увеличению количества моноцитов.
У некоторых пациентов с тяжелой хронической нейтропенией филграстим также может незначительно повысить количество циркулирующих эозинофилов и базофилов нормализуются. У некоторых пациентов наблюдается эозинофилия или базофилия еще до начала лечения. Увеличение количества нейтрофилов при применении препарата в диапазоне рекомендуемых доз зависит от величины дозы их функциональные свойства нормальные или усиленные, о чем свидетельствуют результаты исследования хемотаксиса и фагоцитоза. Применение филграстима, как первичное, так и после химиотерапии, активирует клетки-предшественники гемоцитов периферической крови (КПГПК). Периферические стволовые клетки крови (ПОКА) можно забирать у больного и вводить ему после лечения цитостатиками в высоких дозах вместо пересадки костного мозга или как дополнение к ней.
Введение КПГПК ускоряет восстановление кроветворения, уменьшает опасность геморрагических осложнений и потребность в переливании тромбоцитарной массы. У здоровых доноров доза филграстима, что составляет 10 мкг на килограмм массы тела в сутки, что вводится подкожно в течение 4 - 5 дней подряд, дает в большинстве случаев выход> 4 * 10 Июнь CD34 + клеток на килограмм масса тела реципиента после двух лейкоферез. После лечения филграстимом количество нейтрофилов в крови уменьшается примерно на 50% через 1-2 дня, и возвращается к нормальным значениям через 1-7 дней. Лечение филграстимом приводит к значительному снижению заболеваемости, тяжести и продолжительности как нейтропении, так и фебрильных эпизодов, которые часто наблюдаются после лечения цитостатической химиотерапией или апластической химиотерапией с последующей трансплантацией костного мозга.
Пациентов во химиотерапией, которые также получали филграстим, нужно госпитализировать реже и на более короткий срок. Кроме того, им можно реже использовать антибиотики, чем пациентам, которые прошли химиотерапию без дополнительного лечения. Лечение филграстимом значительно сокращает продолжительность фебрильной нейтропении, применение антибиотиков и госпитализации после индукционной химиотерапии у пациентов с острым миелоидный лейкоз. Появление лихорадки и зафиксированных инфекций при таких условиях не уменьшалась. Эффективность Г-КСФ еще не установлена у пациентов, вследствие уменьшения спинального резерва уже имеют лейкопения до начала лечения (например, после большой лучевой терапии и / или повторных циклах химиотерапии). У этих пациентов лечение Г-КСФ не может временно заменить обычное корректировки доз химиотерапии.
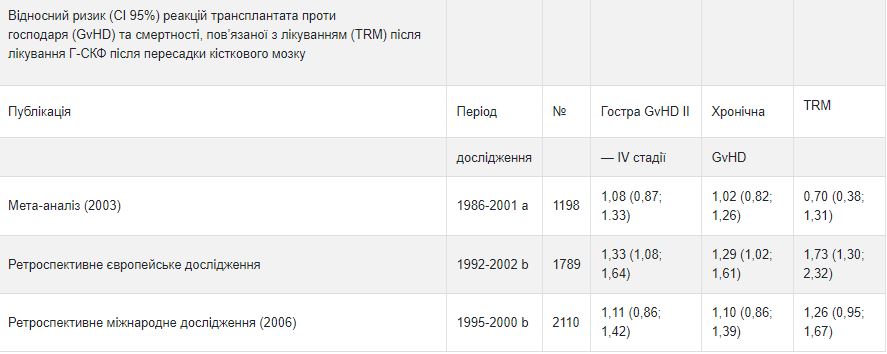
В ретроспективном европейском исследовании было изучено использование Г-КСФ после аллогенной трансплантации костного мозга у пациентов с острой лейкемией. В нем указано, что использование Г-КСФ связано с повышенным риском реакции «трансплантат против хозяина» (GvHD), смертности, связанной с лечением (TRM) и смертности. Другое международное ретроспективное исследование пациентов с острым или хронической миелоидной лейкемией не выявило влияния на GvHD, TRM и смертность. Мета-анализ исследований по аллогенной трансплантации, в том числе результаты девяти проспективных рандомизированных исследований, восьми ретроспективных исследований и одного контрольного случае, не выявил влияния на риск возникновения острой реакции GvHD или ранней смертности вследствие лечения.
а Анализ включал исследования, связанные с трансплантацией костного мозга в этот период; в некоторых исследованиях применяли GM-CSF (фактор, стимулирующий колонию гранулоцитив- макрофагов).
b Анализ включал пациентов, получавших трансплантации костного мозга в этот период.
Лечение филграстимом детей или взрослых с тяжелой хронической нейтропенией (тяжелая наследственная, периодическая или идиопатическая нейтропения) вызывает увеличение абсолютного количества нейтрофилов в периферической крови, а также снижение инфекций и их последствий. Применение филграстима у ВИЧ-инфицированных пациентов удерживает количество нейтрофилов в пределах нормы, позволяя вводить противовирусные препараты и / или другие миелосупрессивного препараты в обычной дозе. Нет никаких доказательств того, что пролиферация ВИЧ стимулируется у пациентов, инфицированных вирусом и которых лечат филграстимом. Как и другие гемопоэтические факторы роста, Г-КСФ обнаружил in vitro стимулирующее действие на рост эндотелиальных клеток человека.
Фармакокинетика. Абсорбция Существует положительная линейная корреляция между дозой и сывороточной концентрацией филграстима, независимо от того, вводят филграстим внутривенно или подкожно. Максимальные концентрации 'филграстима в сыворотке между 5 и 1840 нг / мл были продемонстрированы после введения разовых доз в пределах от 1,7 до 69,0 мкг на килограмм массы тела (короткая 30-минутная в / в инфузии). После подкожного введения рекомендованной дозы измеряли сывороточные концентрации до максимум 118 нг / мл и они оставались выше 10 нг / мл в течение 8-16 часов. Исчисленный объем распределения в крови составлял примерно 150 мл / кг. Вывод Клиренс филграстиму имеет кинетику первой степени после подкожного и внутривенного введения. Общий определенный клиренс составлял 0,6 мл / мин / кг.
Период полувыведения составляет приблизительно 3,5 ч. Во время непрерывных вливаний филграстима в течение 28 дней у пациентов, имевших аутотрансплантат костного мозга, не было данных о накоплении продукта, период полувыведения оставался сопоставимым. Фармакокинетический профиль, установленный при концентрации 0,96 мг / мл, представляет незначительную разницу, связанную с концентрацией, по сравнению с более низкими концентрациями 0,6 мг / мл и 0,3 мг / мл. Эта разница не влияет на общую фармакодинамическом ответ (измеряется в соответствии с реакцией нейтрофилов).
Кинетика для определенных групп пациентов. Пациенты с почечной и печеночной недостаточностью
В исследовании, в котором участвовали 12 пациентов с различной степенью почечной функции, наблюдалось повышение С и AUC, а также уменьшение объема распределения и клиренса у субъектов с конечной стадией почечной болезни по сравнению со здоровыми добровольцами и пациентами с умеренной почечной недостаточностью. Поскольку средние профили АНК были одинаковыми между различными степенями почечной функции, в том числе у пациентов с терминальной стадией почечной болезни, коррекции дозы филграстима не требуется для пациентов с нарушением функции почек.
Результаты исследования 12 пациентов с нарушениями работы печени показывают, что фармакокинетика и фармакодинамика филграстиму сопоставимы у субъектов с нарушениями работы печени и у здоровых лиц. Поэтому корректировки дозы не требуется пациентам с нарушениями работы печени. Доклинические данные Экспрессия рецепторов фактора роста гранулоцитов (Г-КСФ) была подмеченная в определенных злокачественных клетках. Нельзя исключить, что филграстим может выступать фактором роста при некоторых видах опухолей. Канцерогенный потенциал филграстима не изучен. Филграстим НЕ индуцировал генетические мутации бактерий, ни при наличии, ни при отсутствии ферментной системы, метаболизируется препарат. Филграстим не имел заметного влияния на фертильность самца или самки крысы или на время гестации самок в дозе до 500 мкг / кг.
Клинические характеристики
Аккофил Показания
Аккофил показан для: • уменьшение продолжительности и тяжести нейтропении у пациентов (взрослых и детей), получают интенсивную миелосупрессивную химиотерапию цитотоксическими препаратами по поводу злокачественных новообразований (за исключением хронического миелолейкоза и МДС). Для детей, страдающих острой миелоидной лейкемией, не проводилось рандомизированного исследования, однако есть последовательные неконтролируемые или НЕРАНДОМИЗИРОВАННОГО исследования; • для уменьшения продолжительности нейтропении у больных, получающих высокодозной химиотерапии цитотоксическими препаратами с последующей аутологичной или аллогенной трансплантацией костного мозга • для мобилизации периферических стволовых клеток крови (ПСКК) • для длительного использования для увеличения количества нейтрофилов и уменьшения инфекций у детей и взрослых, перенесших клинически значимые инфекции в течение последних 12 месяцев и трижды документированной нейтропении АНК <0,5 * 109 / л, в условиях врожденной, циклической или тяжелой идиопатической нейтропении; • лечение устойчивой нейтропении (абсолютное количество нейтрофилов 51,0 х 109 / л) у пациентов с развернутой стадией ВИЧ-инфекции для снижения риска бактериальных инфекций, когда другие методы лечения нейтропении неуместны.
Противопоказания
Повышенная чувствительность к действующему веществу или к любым вспомогательных веществ.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Особенности применения
Повышенная чувствительность Сообщалось о случаях реакций гиперчувствительности, включая анафилаксии у пациентов, получавших филграстим при начального или дальнейшего лечения. Пациентам с клинически значимой повышенной чувствительностью к Аккофил прием препарата следует прекратить. Не следует назначать Аккофил пациентам с историей повышенной чувствительности к филграстима и пегфилграстиму. Побочные реакции со стороны легких Сообщалось о побочных реакциях со стороны легких, в частности о интерстициальную пневмонию после введения Г-КСФ. Риск может быть увеличен у пациентов с недавней историей легочных инфильтратов или пневмонии. Появление легочных расстройств, таких как кашель, лихорадка и одышка, связанных с рентгенологическими признаками легочных инфильтратов,
Прием Аккофил следует прекратить и начать соответствующее лечение. Гломерулонефрит Сообщалось о гломерулонефрит у пациентов, получавших филграстим и пегфилграстим. Обычно эти случаи исчезают после снижения дозы или после прекращения лечения филграстимом и пегфилграстимом. Рекомендуется контроль показателей мочи. Синдром капиллярного утечки Сообщалось о синдроме капиллярного утечки, который может угрожать жизни, если лечение затягивается, после введения факторов роста Гранулоцитарный линии. Состояние характеризуется гипотонией, гипоальбуминемией, отеком и гемоконцентрация. Пациенты, имеющие симптомы синдрома капиллярного утечки, должны находиться под тщательным контролем и получать стандартное симптоматическое лечение, в том числе и интенсивную терапию (см. ПОБОЧНЫЕ РЕАКЦИИ).
Спленомегалия и разрыв селезенки После введения филграстима пациентам и здоровым донорам сообщалось о случаях спленомегалии, которые, как правило, развивались бессимптомно, и случаи разрыва селезенки. Некоторые случаи разрыва селезенки были летальными 3 этой причине следует тщательно контролировать размер селезенки (например, с помощью клинического обследования, УЗИ). Пациентов, которые жалуются на боль в верхней левой части живота и / или в левом плече, следует проверить на наличие увеличение размеров селезенки или разрыва селезенки. Установлено, что снижение дозы филграстима замедляет или останавливает ход спленомегалии у пациентов с тяжелой хронической нейтропенией. Для 3% пациентов была необходима спленэктомия. Рост злокачественных клеток гранулоцитарного факторы роста могут способствовать росту in vitro не только миелоидных, но и немиелоидных клеток.
Хронический миелоидный лейкоз или миелодиспластический синдром. Безопасность и эффективность филграстиму для пациентов с миелодиспластическим синдромом или хроническим миелоидного лейкоза не определены. Применение Аккофилу при этих заболеваниях не показано. Особую осторожность следует проявлять при установке диагностического разграничения острой трансформации хронического миелоидного лейкоза и острый миелобластный лейкемии. Тромбоцитопения У пациентов, получавших филграстим, наблюдали тромбоцитопения. Количество тромбоцитов следует тщательно контролировать, особенно в течение первых недель лечения Аккофилом. Временное прекращение или уменьшение дозы Аккофил следует рассмотреть для пациентов с тяжелой хронической нейтропенией, в которых развивается тромбоцитопения (количество тромбоцитов <100 * 109 / л). Лейкоцитоз лейкоцитоз 100 * 109 / л или более наблюдался периодически у пациентов, принимавших филграстим в дозах, превышающих 0300000 ЕД (3 мкг) на килограмм в сутки. Не зафиксировано никаких побочных реакций, непосредственно связанных с этим степени лейкоцитоза. Однако из-за рисков лейкоза следует регулярно проверять формулу лейкоцитов через регулярные промежутки времени.
Если количество лейкоцитов превышает 50 * 109 / л после ожидаемого Надир (самый низкий показатель), следует немедленно прекратить прием Аккофил. Кроме того, если количество лейкоцитов превышает 70 * 109 / л при приеме Аккофил для мобилизации ПСКК, необходимо прекратить прием Аккофил. Временный лейкоцитоз (количество лейкоцитов> 50 * 109 / л) наблюдался у 41% обследованных здоровых доноров. Количество лейкоцитов> 75 * 109 / л выявлено у 2% здоровых доноров. Иммуногенность Как и для всех терапевтических белков, существует потенциальный риск иммуногенности. Частота выработки антител к филграстима составляет менее 1% в более чем 1000 субъектов, получавших филграстим при клинических исследований, проведенных Amgen; однако эти антитела не были связаны с нейтрализующей действием или с нежелательными клиническими последствиями. Аортит Сообщалось о аортит после введения Г-КСФ у здоровых лиц и онкологических больных. Среди симптомов были: повышение температуры, боль в животе, недомогание, боли в спине и усиление маркеров воспаления (например, С-реактивный белок и количество лейкоцитов). В большинстве случаев аортит диагностировали с помощью КТ и снимали его после прекращения лечения Г-КСФ (см. Также ПОБОЧНЫЕ РЕАКЦИИ). Гематурия и протеинурия гематурия и протеинурия наблюдались у небольшого количества пациентов. Анализы мочи следует делать регулярно. также ПОБОЧНЫЕ РЕАКЦИИ). Гематурия и протеинурия гематурия и протеинурия наблюдались у небольшого количества пациентов. Анализы мочи следует делать регулярно. также ПОБОЧНЫЕ РЕАКЦИИ). Гематурия и протеинурия гематурия и протеинурия наблюдались у небольшого количества пациентов. Анализы мочи следует делать регулярно.
ВНИМАНИЕ И МЕРЫ ПО сопутствующих заболеваний Остеопороз Контроль плотности костей рекомендуется пациентам, у которых уже есть остеопороз и которые в течение шести месяцев непрерывно принимали Аккофил, поскольку случаи остеопороза наблюдались во время длительного лечения. Особые меры предосторожности для пациентов с серповидно-клеточной анемией По данным публикаций, большое количество лейкоцитов неблагоприятная для пациентов, страдающих серповидноклеточной анемией. По этой причине врач должен назначать Аккофил чрезвычайно осторожно для этих пациентов и тщательно контролировать соответствующие лабораторные показатели. Он должен принимать во внимание возможную связь со спленомегалией и вазооклюзийнимы кризисами. Сообщалось о кризисе серповидноклеточной анемии, которая в некоторых случаях оказалась смертельной при применении филграстима такими пациентами. Врач должен быть осторожным при назначении Аккофил пациентам с серповидно признаку или серповидноклеточная анемия. Аллергия на латекс Защитный колпачок содержит природный каучук, который может вызвать аллергическую реакцию. Непереносимость фруктозы Аккофил содержит сорбит. Поэтому пациентам с редкой наследственной непереносимостью фруктозы не следует применять данный препарат. Натрий Аккофил содержит менее 1 ммоль (23 мг) натрия в 1 предварительно наполненном шприце (0,5 мл раствора для инъекций), то есть он по сути является «безнатриевим». Поэтому пациентам с редкой наследственной непереносимостью фруктозы не следует применять данный препарат. Натрий Аккофил содержит менее 1 ммоль (23 мг) натрия в 1 предварительно наполненном шприце (0,5 мл раствора для инъекций), то есть он по сути является «безнатриевим». Поэтому пациентам с редкой наследственной непереносимостью фруктозы не следует применять данный препарат. Натрий Аккофил содержит менее 1 ммоль (23 мг) натрия в 1 предварительно наполненном шприце (0,5 мл раствора для инъекций), то есть он по сути является «безнатриевим».
ВНИМАНИЕ И МЕРЫ ПО ХИМИОТЕРАПИИ Риск, связанный с повышением дозы химиотерапии. Аккофил не следует применять для увеличения дозировки цитотоксической химиотерапии, превышает рекомендуемый режим дозирования. Необходимо принять специальные меры предосторожности по лечению пациентов, получающих химиотерапию в высоких дозах, поскольку, с одной стороны, до сих пор не было продемонстрировано улучшение реакции опухолей на такое лечение, а с другой - химиотерапия с высокой дозой может привести к усилению токсических эффектов, включая влияние на сердце, легкие, нервную систему и кожу (см. профессиональную информацию о применяемых химиотерапии). Химиотерапия при задержке мислосупресии Данных об эффективности филграстима в химиотерапии, вызывает задержку миелосупрессии - нитрозуреямы или митомицином С, в том числе введение миелосупрессивных доз антиметаболитов, таких как 5-FU или цитозин - арабинозид все еще недостаточно. Влияние химиотерапии на эритроциты и тромбоциты Аккофил значительно снижает частоту тяжелой и фебрильной нейтропении. Однако для пациентов, получавших лечение схеме миелотоксической химиотерапии, существует риск развития тромбоцитопении и анемии. Поэтому рекомендуется регулярно проверять количество тромбоцитов и гематокрит. Особая осторожность требуется при применении с химиотерапевтическими средствами (комбинированная или монотерапия), которые, как известно, вызывают тяжелую тромбоцитопению. Тромбоцитопения Пациенты, получающие Аккофил после высоких доз миелосупрессивной химиотерапии, могут иметь повышенный риск развития тромбоцитопении. Влияние химиотерапии на эритроциты и тромбоциты Аккофил значительно снижает частоту тяжелой и фебрильной нейтропении. Однако для пациентов, получавших лечение схеме миелотоксической химиотерапии, существует риск развития тромбоцитопении и анемии. Поэтому рекомендуется регулярно проверять количество тромбоцитов и гематокрит. Особая осторожность требуется при применении с химиотерапевтическими средствами (комбинированная или монотерапия), которые, как известно, вызывают тяжелую тромбоцитопению. Тромбоцитопения Пациенты, получающие Аккофил после высоких доз миелосупрессивной химиотерапии, могут иметь повышенный риск развития тромбоцитопении. Влияние химиотерапии на эритроциты и тромбоциты Аккофил значительно снижает частоту тяжелой и фебрильной нейтропении. Однако для пациентов, получавших лечение схеме миелотоксической химиотерапии, существует риск развития тромбоцитопении и анемии. Поэтому рекомендуется регулярно проверять количество тромбоцитов и гематокрит. Особая осторожность требуется при применении с химиотерапевтическими средствами (комбинированная или монотерапия), которые, как известно, вызывают тяжелую тромбоцитопению. Тромбоцитопения Пациенты, получающие Аккофил после высоких доз миелосупрессивной химиотерапии, могут иметь повышенный риск развития тромбоцитопении. Поэтому рекомендуется регулярно проверять количество тромбоцитов и гематокрит. Особая осторожность требуется при применении с химиотерапевтическими средствами (комбинированная или монотерапия), которые, как известно, вызывают тяжелую тромбоцитопению. Тромбоцитопения Пациенты, получающие Аккофил после высоких доз миелосупрессивной химиотерапии, могут иметь повышенный риск развития тромбоцитопении. Поэтому рекомендуется регулярно проверять количество тромбоцитов и гематокрит. Особая осторожность требуется при применении с химиотерапевтическими средствами (комбинированная или монотерапия), которые, как известно, вызывают тяжелую тромбоцитопению. Тромбоцитопения Пациенты, получающие Аккофил после высоких доз миелосупрессивной химиотерапии, могут иметь повышенный риск развития тромбоцитопении.
РЕКОМЕНДАЦИИ ПО КОНТРОЛЮ ФОРМУЛЫ КРОВИ Лечение препаратом Аккофил не предотвращает возникновение тромбоцитопении и анемии "при приеме миелосупрессивных препаратов. Поскольку во время лечения Аккофилом такие лекарственные средства в принципе могут вводить пациентам в больших дозах или в больших количествах, риск тромбоцитопении и анемии также может возрастать. Рекомендуется регулярно контролировать показатели крови. Анемия и преходящий рост миелоидных стволовых клеток - это другие гематологические проявления, которые также требуют тщательного мониторинга (см. Раздел ВНИМАНИЕ И МЕРЫ ПО ОБЩИХ РИСКОВ И побочные эффекты, тромбоцитопения и ВНИМАНИЕ И МЕРЫ ПО химиотерапия).
Инфекции, которые могут вызвать миелосупрессии Причиной нейтропении может быть условно-патогенная инфекция, например, комплекс Mycobacterium avium, который проникает в костный мозг, или злокачественное образование, например, лимфома. Пациентам, страдающим от инфекции, которая пронизывает костный мозг, или от рака, следует дополнительно рассматривать основную патологию в дополнение к лечению нейтропении препаратом Аккофил. Механизм действия филграстиму нейтропенией относительно указанных клинических случаев недостаточно известен.
ОСОБЫЕ КА категориями ПАЦИЕНТОВ / СПЕЦИФИЧЕСКИЕ ПОКАЗАНИЯ Особые меры безопасности у пациентов, которые проходят мобилизацию ПСКК Оценка количества мобилизованных периферических стволовых клеток крови При проведении оценки количества ПСКК, мобилизованных у больных, получивших терапию с применением Аккофил, особое внимание следует уделять метода количественного определения. Результаты проточного цитометрического анализа количества С034 + клеток значительно отличаются в зависимости от примененной методологии определения. Итак, следует с осторожностью относиться к результатам определения их количества, полученных в других лабораториях. Результаты статистического анализа взаимосвязи количества введенных СО34 + клеток и скорости нормализации количества тромбоцитов после проведения химиотерапии с применением высоких доз химиопрепаратов свидетельствуют о сложной, но постоянную зависимость.
Рекомендации о необходимости обеспечения минимального содержания на уровне> 2,0 * 6 октября CD34 + клеток / кг основываются на опубликованных данных об опыте адекватного восстановления гематологических показателей. При уровне, превышающем минимальный рекомендуемый, наблюдается быстрая нормализация, при уровне ниже рекомендуемого, - длительнее. Мобилизация Нет ни одного рандомизированного сравнения двух рекомендуемых методов мобилизации (филграстим отдельно, или в сочетании с мислосупресивною химиотерапией) в пределах одной популяции пациентов. Степень вариации между отдельными пациентами и между лабораторными анализами CD34 + клеток означает, что непосредственное сравнение различных исследований затруднено. Поэтому трудно рекомендовать оптимальный метод. Выбор метода мобилизации следует рассматривать в связи с общими целями лечения для отдельного пациента. Предшествующее лечение цитотоксическими средствами и мобилизация ПСКК У больных, которым ранее проводили интенсивную миелосупрессивную терапию, на фоне применения препарата Аккофил для мобилизации ПСКК может не происходить увеличение количества ПСКК до рекомендуемого минимального уровня (≥2,0 * 106CD34 + клеток / кг). Некоторые цитотоксические средства проявляют особую токсичность относительно клеток-предшественников гемопоэза и негативно влияют на их мобилизацию.
Длительное применение препаратов мелфалан, карбоплатин или кармустин (BCNU) перед мобилизацией клеток-предшественников может привести к ухудшению результатов. Однако одновременное применение этих препаратов с филграстимом эффективно при мобилизации ПСКК. Если планируется трансплантация ПСКК, рекомендуется провести мобилизацию стволовых клеток на ранней стадии лечения больного. Особое внимание следует обратить на количество клеток-предшественников, активированных у таких больных до применения препаратов химиотерапии в высоких дозах. Если результаты мобилизации в соответствии с вышеприведенным критериям, следует рассмотреть применение альтернативных методов лечения, не требующие использования клеток-предшественников. Особые меры безопасности для здоровых доноров, которые проходят мобилизацию ПСКК Мобилизация ПСКК здоровых доноров влияет на состояние их здоровья и применяется исключительно для получения аллогенных стволовых клеток для трансплантации. Доноры, которым проводят мобилизацию ПСКК для трансплантации, должны соответствовать стандартным требованиям по клиническим показаниям и результатам лабораторных анализов, предъявляемых к доноров стволовых клеток. Если необходимо провести более одного лейкафереза, перед аферезом следует обратить особое внимание донорам, количество тромбоцитов которых составляет <100 * 109 / л. Как правило, не следует проводить аферез, если количество тромбоцитов составляет <75 * 109 / л. должны соответствовать стандартным требованиям по клиническим показаниям и результатам лабораторных анализов, предъявляемых к доноров стволовых клеток. Если необходимо провести более одного лейкафереза, перед аферезом следует обратить особое внимание донорам, количество тромбоцитов которых составляет <100 * 109 / л. Как правило, не следует проводить аферез, если количество тромбоцитов составляет <75 * 109 / л. должны соответствовать стандартным требованиям по клиническим показаниям и результатам лабораторных анализов, предъявляемых к доноров стволовых клеток. Если необходимо провести более одного лейкафереза, перед аферезом следует обратить особое внимание донорам, количество тромбоцитов которых составляет <100 * 109 / л. Как правило, не следует проводить аферез, если количество тромбоцитов составляет <75 * 109 / л.
Транзиторная тромбоцитопения (количество тромбоцитов <100 х 109 / л) после введения филграстима и лейкафереза наблюдалась у 35% пациентов. О некоторых случаях снижение количества тромбоцитов <50x109 / л было сообщено. Лейкаферез не следует проводить донорам, которые нуждаются в антикоагулянтной терапии или с нарушениями гемостаза. Дальнейшее введение филграстима следует отменить или уменьшить дозу в случаях рост лейкоцитов до уровня, превышающего 70 х 109 / л. Мониторинг состояния доноров, которые получают Г-КСФ для мобилизации ПСКК, следует продолжать до нормализации гематологических показателей. У здоровых доноров данные о длительном приеме ограничены. В период постмаркетинговых исследований поступали сообщения о случаях побочных явлений со стороны легких (кровохарканье, инфильтрация легких) у здоровых доноров.
В течение периода мониторинга до 4 лет не сообщалось об аномальном кроветворения у здоровых доноров. Риск содействие образованию злокачественных клонов миелоидных клеток не исключен. Для обеспечения длительного мониторинга безопасности рекомендуется систематически сообщать и регистрировать данные о донацию каждой стволовой клетки и фиксировать их. Специальные меры предосторожности для реципиентов аллогенных ПСКК, мобилизованных введением Аккофил Данные свидетельствуют о том, что иммунологической взаимодействия аллогенных ПСКК и реципиента присущий большая степень риска развития острой и хронической реакции «трансплантат против хозяина» по сравнению с трансплантацией костного мозга (см. Характеристики / ВЛИЯНИЕ).
Особые меры предосторожности у пациентов с тяжелой наследственной, периодической или идиопатической нейтропенией Безопасность и эффективность филграстима не установлены для новорожденных и пациентов с аутоиммунной нейтропенией. Аккофил не следует применять пациентам с тяжелой врожденной нейтропенией, в которых развивается лейкемия или выявляются признаки прогрессирования лейкемии. Трансформация в лейкоз или предлейкоз Особая осторожность необходима при диагностике тяжелой хронической нейтропении, чтобы дифференцировать ее от других гематологических заболеваний, таких как апластическая анемия, миелодисплазия и миелолейкоз
До начала лечения следует провести развернутый анализ крови с определением лейкоцитарной формулы и количества тромбоцитов, а также определить морфологическую картину костного мозга и кариотип. Возникновение МДС (МДС) или лейкемии у пациентов с тяжелой хронической нейтропенией, участвовавших в клинических исследованиях результатов применения филграстима наблюдается редко (12,1% случаев в течение 5 лет). Указанные нарушения наблюдались лишь у пациентов с наследственной нейтропенией. МДС и лейкоз являются частыми осложнениями заболевания, их связь с терапией с применением филграстима является неопределенным. Примерно у 12% пациентов (без цитогенетических нарушений до начала терапии) по результатам следующих анализов наблюдались отклонения, в том числе моносемия. неизвестно, или повышает долговременная терапия с применением филграстима у пациентов с тяжелой хронической нейтропенией риск цитогенетических нарушений, МДС или трансформации заболевания лейкемией. Морфологическое и ультразвуковое обследование костного мозга пациентов следует проводить регулярно, с интервалом примерно каждые 12 месяцев. Особые меры предосторожности для пациентов с ВИЧ-инфекцией Количество клеток крови Необходимо тщательно контролировать абсолютное количество нейтрофилов (АКН), особенно в течение первых недель терапии препаратом Аккофил.
В зависимости от условий, у некоторых больных может наблюдаться очень быстрое и значительное увеличение АКН при первых введениях Аккофил. В течение первых дней применения препарата рекомендуется ежедневно определять АКН. В дальнейшем АКН следует проверять минимум 2 раза в неделю в течение первых 2 недель и затем каждую неделю или через неделю в течение всего курса поддерживающей терапии. В случае перерыва в приеме препарата Аккофил в дозе 300 мкг / сутки у больных во время лечения может наблюдаться значительное колебание АКН. С целью определения минимального уровня АКН (надира) рекомендуется проводить контроль общего анализа крови перед каждым введением препарата Аккофил. Особые популяции пациентов Опыт пациентов с тяжелыми нарушениями функции печени и / или почек ограничен (см. ФАРМАКОКИНЕТИКА и Дозировка / Способ применения).
Влияние филграстима у пациентов со значительным уменьшением количества миелоидных кпитин- предшественников еще не изучено. Поскольку Аккофил действует в основном на созревание предшественников нейтрофилов и, таким образом, увеличивает количество нейтрофилов в крови, его влияние может быть уменьшен у пациентов с низким количеством предшественников (например, у пациентов, прошедших лучевую терапию или интенсивную химиотерапию).
ВНИМАНИЕ И МЕРЫ ПО ДИАГНОСТИКИ
Сканирование костей Увеличение гемопоэтической активности костного мозга в ответ на лечение факторами роста связано с временными аномальными результатами поисками костей. Это явление необходимо учитывать при интерпретации результатов сканирования.
Применение в период беременности или кормления грудью
Беременность Безопасность филграстиму для беременных не установлена. В литературе имеются сообщения о том, что филграстим проходит плацентарный барьер у беременных. По результатам исследований на животных обнаружена репродуктивная токсичность. У кроликов, получавших высокие дозы (гораздо выше, чем обычное клиническое облучения), что приводит к токсичности для матери, наблюдается повышенная частота эмбриональной летальности. Препарат Аккофил не рекомендуется применять в период беременности, кроме случаев крайней необходимости. Кормление грудью Неизвестно, проникает филграстим и его метаболиты в грудное молоко, поэтому препарат не вводят беременным женщинам. Итак риск для младенцев нельзя исключить.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Аккофил имеет незначительное влияние на способность управлять автомобилем и другими машинами. После приема Аккофил может возникнуть головокружение (см. Раздел ПОБОЧНЫЕ РЕАКЦИИ). Исследований относительно влияния на скорость реакции при управлении автотранспортом или другими механизмами не проводилось.
Способ применения Аккофил и дозы
Пациенты, получающие цитотоксическую химиотерапию по поводу злокачественных заболеваний.
дозировка
Рекомендуемая доза Аккофил составляет 0500000 ЕД (5 мкг) на килограмм массы тела в сутки. Лечение с Аккофил следует начинать не ранее, чем через 24 часа после назначения цитотоксической 'химиотерапии. Содержимое предварительно наполненного шприца Аккофил 30 (60 млн ЕД / мл) соответствует суточной дозе, необходимой для пациента весом 60 кг. Содержимое предварительно наполненного шприца Аккофил 48 соответствует суточной дозе, необходимой для пациента весом 96 кг:
продолжительность лечения
Ежедневное введение Аккофил следует продолжать до тех пор, пока ожидаемое количество нейтрофилов нормализуется после превышения низкого числа нейтрофилов (надир). После стандартной химиотерапии, предназначенной при солидных опухолях, лимфомах и лимфоидных лейкемиях, длительность лечения может составлять до 14 дней. После индукционного и консолидационного лечения острого миелоидного лейкоза продолжительность лечения может быть значительно длиннее (до 38 дней), в зависимости от типа, дозы и режима дозирования цитотоксической химиотерапии.
У пациентов, получающих цитотоксическую химиотерапию, как правило, наблюдается кратковременное увеличение числа нейтрофилов через 1-2 дня после начала лечения. Однако, чтобы обеспечить длительный терапевтический успех, прием Аккофил не следует прерывать до того, как ожидаемый надир (самый низкий показатель) будет превышен и количество нейтрофилов нормализуется. Не рекомендуется преждевременное прекращение лечения с Аккофил, то есть до достижения ожидаемого Надир (самого низкого показателя). Лечение следует прекратить, когда количество нейтрофилов достигла 1,0 * 109 / л, после превышения Надир (низкой нормы). Способ применения Аккофил можно вводить как ежедневную подкожную инъекцию, так и 30-минутную ежедневную инфузию после разведения в 5% растворе глюкозы (см. Инструкции для растворения в разделе СПЕЦИАЛЬНЫЕ ПРИМЕЧАНИЯ).
В большинстве случаев предпочтительным является подкожное введение. Результаты одного из исследований позволяют предположить, что введение может сократить продолжительность действия. Клиническое значение этого наблюдения в случае повторного введения не установлено. Пациенты, получавшие цитотоксическую химиотерапию, после которой состоялась трансплантация костного мозга Дозировка Начальная рекомендуемая доза Аккофил составляет 1,0 млн ЕД (10 мкг) на килограмм массы тела в сутки. Первую дозу Аккофил следует ввести не ранее, чем через 24 часа после введения цитотоксической химиотерапии, но не позднее, чем через 24 часа после пересадки костного мозга. Продолжительность лечения Эффективность и безопасность применения Аккофил, который использовался в течение 28 дней по этому показаниям, не установлено.
корректировка дозы
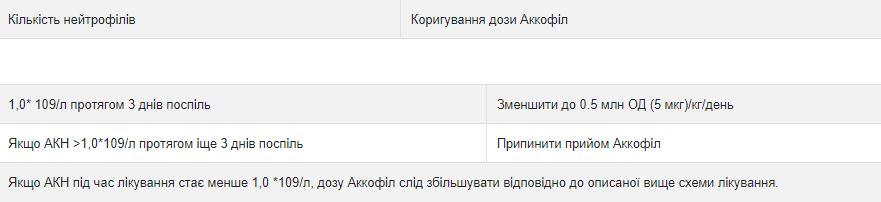
После того, как низкий показатель нейтрофилов (надир) прошел суточную дозу Аккофил следует скорректировать в соответствии со схемой, в зависимости под изменения формулы крови:
АКН = абсолютное количество нейтрофилов Способ применения Аккофил вводят в виде 30-минутной или 24-часовой инфузии, либо в виде 24-часовой непрерывной подкожной инфузии. Аккофил должен быть разведен в 20 мл 5% раствора глюкозы (см. Инструкции по растворения в разделе СПЕЦИАЛЬНЫЕ ПРИМЕЧАНИЯ).
Мобилизация периферических стволовых клеток крови (ПСКК). Мобилизация периферических стволовых клеток крови у пациентов, получающих миелосупрессивную терапию с последующим аутологичных переливанием ПСКК, с трансплантацией костного мозга или без нее, или у пациентов, которые проходят апластической терапию с последующей пересадкой ПСКК. Дозировка Рекомендуемая доза Аккофил составляет 1,0 млн ЕД (10 мкг) на килограмм массы тела в сутки в течение 5-7 дней подряд. Продолжительность лечения Одной-двух процедур лейкафереза на 5 и 6 день, как правило, достаточно.
При других обстоятельствах может потребоваться дополнительный Лейкаферез. Прием Аккофил следует продолжать до последнего лейкафереза. Способ применения Аккофил вводят в виде непрерывной 24-часовой п инфузии или в виде единовременной подкожной инъекции. Перед инфузией, Аккофил должен быть разведен в 20 мл 5% раствора глюкозы (см. Инструкции по растворения в разделе СПЕЦИАЛЬНЫЕ ПРИМЕЧАНИЯ). Мобилизация ПСКК после миелосупрессивной химиотерапии Дозировка Рекомендуемая доза Аккофилу составляет 0500000 ЕД (5 мкг) на килограмм массы тела в сутки с первого дня после окончания химиотерапии, пока количество нейтрофилов не вернется к норме после ожидаемого Надир (низкой количества).
Лейкаферез должен происходить в период, когда абсолютное количество нейтрофилов (АНК) меняется с <0,5 * 109 / л до> 5,0 * 109 / л. У пациентов, ранее не проходили интенсивной химиотерапии, одного лейкафереза часто бывает достаточно. В других случаях рекомендуется дополнительный Лейкаферез. У больных, которым ранее проводили интенсивную химиотерапию, на фоне применения препарата Аккофил для мобилизации ПСКК может не происходить увеличение количества ПСКК до рекомендуемого минимального уровня (общий минимальный прирост от лейкафереза:> 10 а 30 * 104 GM-CFC / кг или> 1 а 2 5 * 106 СО34 + клеток / кг). Способ применения Аккофил вводят подкожно.
Мобилизация ПСКК у здоровых доноров перед аллогенной трансплантацией ПСКК Мобилизация кпитин-предшественников следует проводить только под наблюдением центров, имеющих опыт сбора кпитин-предшественников от здоровых доноров. Дозировка Рекомендуемая доза Аккофил составляет 1 млн ЕД (10 мкг) на килограмм массы тела в сутки в течение 4-5 дней подряд. Лейкаферез необходимо начинать на 5 день и продолжать до 6 дня, если необходимо, чтобы собрать количество 4 * 106 CD34 + клеток на килограмм массы тела реципиента. Безопасность и эффективность введения Аккофил здоровым донорам до 16 и от 60 лет не оценивались. Способ применения Аккофил вводят подкожно.
Пациенты с тяжелой наследственной, периодической или идиопатической нейтропенией (ТХН) Дозировка Наследственная нейтропения: начальная рекомендуемая доза Аккофил составляет 1200000 ЕД (12 мкг) на килограмм массы тела в сутки, в виде единой дозы или нескольких. Идиопатическая и периодическая нейтропения: рекомендуемая начальная доза Аккофил составляет 0500000 ЕД (5 мкг) на килограмм массы тела в сутки, в виде единой дозы или нескольких. Корректировка дозы У каждого пациента дозу необходимо устанавливать индивидуально, чтобы достичь минимальной АНК в 1,5 * 109 / л. Для поддержания необходимого количества нейтрофилов требуется длительное ежедневное введение препарата. Дозу удвоить, если через 1-2 недели не достигнуто целевого значения АНК 1,5 * 10Э / л, и уменьшить вдвое, если АНК превышает 10 * 109 / л.
Скорее увеличение дозы показано для пациентов с тяжелыми инфекциями. Дозы, превышающие 14500000 ЕД (145 мкг) на килограмм массы тела в сутки, являются безопасными и хорошо переносятся. Способ применения Аккофил вводят подкожно. Пациенты с ВИЧ-инфекцией Дозировка Восстановление числа нейтрофилов Рекомендованная начальная доза Аккофил - 0100000 ЕД / кг (1 мкг / кг) массы тела в сутки с увеличением дозы до 0400000 ЕД (4 мкг / кг) массы тела в сутки до нормализации количества нейтрофилов (АКН> 2,0 х Ю9 / л. в клинических исследованиях более 90% пациентов отреагировали на эту дозу, и их нейтропения нормализовалась в течение 2 дней (в среднем). в редких случаях (<10% пациентов) для восстановления числа нейтрофилов доза препарата может быть увеличена до 1,0 млн ЕД / кг (10 мкг / кг массы тела в сутки).
Поддержание нормального количества нейтрофилов Как только нейтропения восстанавливается, следует определить эффективную минимальную дозу для поддержания нормального количества нейтрофилов. Поддерживающая доза составляет 300 мкг / сут 2-3 раза в неделю по альтернативной схеме (через день). В зависимости от АНК пациента, может потребоваться дополнительное корректировки дозы для содержания числа нейтрофилов выше 2,0 * 10Э / л. Во время клинических исследований необходимо было вводить 300 мкг в сутки от 1 до 7 дней в неделю, чтобы поддерживать АНК выше 2,0 * 109 / л; средняя продолжительность введения этой дозы составляла 3 дня в неделю. Длительное применение препарата может быть необходимым для поддержания АНК 2,0 * 109 / л. Способ применения Аккофил вводят подкожно.
Специальные рекомендации при дозировке
Пожилые пациенты Особых рекомендаций по применению препарата Аккофил пациентов пожилого возраста нет. Пациенты с печеночной или почечной недостаточностью Исследование результатов приема филграстима пациентами с выраженной почечной или печеночной недостаточностью показали, что фармакокинетические и фармакодинамические профили практически похожи на те, что наблюдаются у здоровых лиц (см. ФАРМАКОКИНЕТИКА). Коррекция дозы для таких пациентов не требуется.
Дети
Рекомендации по дозированию для педиатрических пациентов, получающих миелосупрессивную цитотоксическую химиотерапию, или для педиатрических пациентов с тяжелой наследственной, периодической или идиопатической нейтропенией такие же, как и для взрослых. Данные клинических исследований педиатрических пациентов показывают, что безопасность и эффективность филграстиму сопоставима у взрослых и детей, прошедших миелосупрессивную химиотерапию. 65% пациентов, участвовавших в клинических исследованиях по поводу тяжелой хронической нейтропении, были моложе 18 лет. Лечение филграстимом в этой возрастной группе, в которой в основном входили пациенты с врожденной нейтропенией, оказалось эффективным. Что касается педиатрических пациентов, лечили тяжелую хроническую нейтропению, то не было обнаружено разницы относительно профиля безопасности препарата по сравнению со взрослыми.
Передозировка
Симптомы передозировки филграстиму неизвестны. Пациенты с выраженной хронической нейтропенией, получавших дозы, превышающие 14500000 ЕД (145 мкг) на килограмм массы тела в день, не имели патологических симптомов. У пациентов, получавших цитотоксическую химиотерапию с пересадкой костного мозга, было показано, что дозы до 7,0 млн ЕД (70 мкг) на килограмм массы тела хорошо переносятся. При передозировке через 1-2 дня после прекращения лечения количество нейтрофилов обычно снижается на 50%, а через 1-7 дней возвращается к норме.
Побочные эффекты
Список побочных реакций
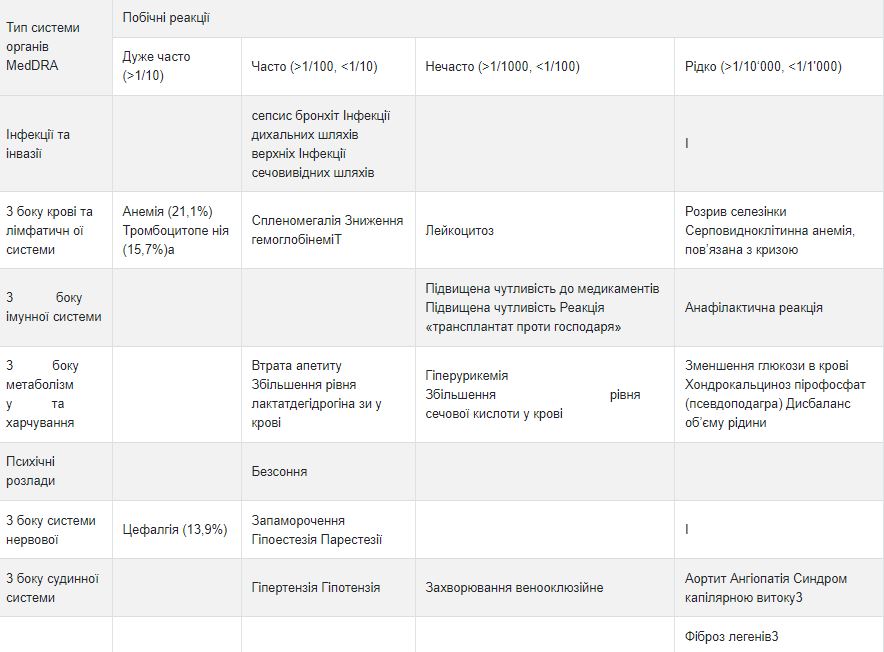
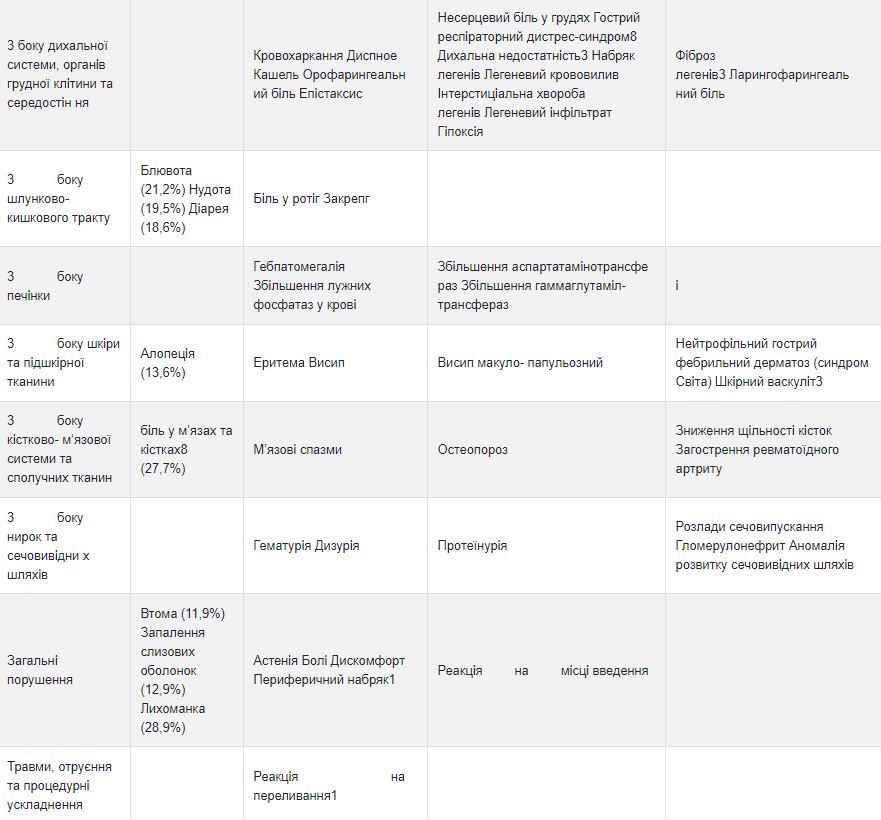
Клинические исследования Аккофил не показали разницы между профилем безопасности Аккофил и эталонным препаратом филграстим. Данные, приведенные в таблице, касаются побочных реакций, сообщенных в клинических исследованиях с применением эталонного препарата филграстима и в контексте спонтанного сообщения. В рамках каждой группы частоты побочных реакций представлены в порядке уменьшения тяжести.
б Сообщалось о случаях GvHD и смертей у пациентов после аллогенной трансплантации костного мозга.
с В том числе боль в костях, боли в спине, артралгия, миалгия, боль в конечностях, боли в опорно-двигательном аппарате, боли в опорно-двигательном аппарате в груди, боль в шее.
г Побочные реакции с наибольшей частотой заболевания у пациентов, получавших филграстим по сравнению с плацебо и связанные с последствиями основного злокачественного образования или цитотоксической химиотерапией.
Описание выбранных побочных реакций
Реакции повышенной чувствительности к лекарствам Сообщалось о реакции повышенной чувствительности, включая анафилаксии, сыпь, крапивница, ангионевротический отек, одышку и гипотензии во время первого лечения и при продолжении лечения, при клинических исследований и послемаркетингового опыта. В целом о таких симптомах сообщалось чаще после IV введения. Иногда повторное введение препарата приводит к повторному возникновению симптомов, говорит о причинно следственные связи. Аккофил следует отменить в случае сильной аллергической реакции. Побочные реакции со стороны легких О случаях легочных побочных реакций, включая интерстициальную пневмонию, отек легких и легочные инфильтраты, сообщалось в клинических и послемаркетингового исследованиях.
Синдром капиллярного утечки Сообщалось о синдроме капиллярного утечки после использования факторов роста с линии гранулоцитов. Эти явления, как правило, появляются у пациентов с запущенными злокачественными патологиями, сепсисом, получавших многократную химиотерапию или перенесших аферез после мобилизации ПСКК (см. ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ). Спленомегалия и разрыв селезенки После приема филграстима наблюдали спленомегалия и разрыв селезенки. Некоторые случаи разрыва селезенки оказались смертельными (см. ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ). Лейкоцитоз и тромбоцитопения После приема филграстима наблюдались случаи лейкоцитоза и тромбоцитопении (см. ОПЕРЕДЖЕННЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ).
Серповиднокпитинна анемия Постмаркетинговые отчеты об изолированных серповидноклеточная кризиса поступали о пациентах с серповидноклеточной признаку или серповиднокпитинною анемией (см. ПРЕДУПРЕЖДЕНИЯ И МЕРЫ ПРЕДОСТОРОЖНОСТИ). Кожный васкулит Сообщалось о кожный васкулит у пациентов, получавших филграстим. Дети и подростки Данные клинических исследований у детей и подростков показывают, что безопасность и эффективность филграстиму сопоставима у взрослых и детей, получающих цитотоксическую химиотерапию, что позволяет предположить, что нет возрастной разницы в фармакокинетике филграстима. Единственным систематически сообщенным побочным эффектом был мышечно-скелетные боли, не отличается от опыта взрослого населения. Недостаточно данных для дальнейшей оценки использования Аккофилу у детей и подростков. Другие особые группы пациентов
Пожилые пациенты Никакой существенной разницы в безопасности или эффективности не наблюдалось между людьми старше 65 лет и моложе взрослыми (> 18 лет), которые получали цитотоксическую химиотерапию. Клинический опыт не выявил разницы в ответах, полученных у пациентов пожилого и молодого возраста. Недостаточно данных для оценки использования Аккофилу у пожилых людей по другим утвержденным показаниям.
Дети и подростки с НКС Сообщалось о снижении плотности костной ткани и остеопороз у детей и подростков с тяжелой хронической нейтропенией, хронически лечились филграстимом.
Срок годности Аккофил
Условия хранения Аккофил
Хранить в холодильнике (2-8 ° С). Случайное попадание Аккофил до температур ниже температуры замерзания не имеет негативного влияния на стабильность продукта. Хранить в недоступном для детей месте. Хранить в оригинальной упаковке, защищенном от света. В течение срока годности лекарственного средства можно вынуть из холодильника и хранить один раз при комнатной температуре (не выше 25 ° С) в течение не более 15 дней. По истечении этого времени лекарства больше не следует возвращать в холодильник и их следует утилизировать. Физико-химическая стойкость разбавленного раствора для инфузий была продемонстрирована в течение 24 часов при температуре от +2 ° С до +8 ° С. С микробиологической точки зрения продукт следует использовать немедленно. Если его не использовать немедленно, ответственность за срок годности и условия хранения несет пользователь.
Упаковка
По 0,5 мл в предварительно наполненном шприце с инъекционной иглой, с защитным кожухом; по 1 предварительно наполненном шприца в блистере, по 5 блистеров со спиртовыми салфетками в картонной коробке.
Категория отпуска
По рецепту.
Производитель
Аккорд Хелскеа Лимитед.
Местонахождение производителя
Первый этаж, Сэйдж Хаус, 319 Пиннер Роуд, Хэрроу, НА1 4HF, Великобритания /
Первый этаж, Sage House, 319 Pinner Road, Harrow, HA1 4HF, Великобритания.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте Аккофил только по назначению врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- https://www.accord-healthcare.com - Аккорд Хелскеа Лимитед
| Тип данных | Сведения из реестра |
| Торговое наименование: | Аккофил |
| Производитель: | Аккорд Хелскеа Лимитед |
| Форма выпуска: | раствор для инъекций, 480 мг / 0,5 мл, по 0,5 мл в предварительно наполненном шприце с инъекционной иглой, с защитным кожухом; по 1 предварительно наполненном шприца в блистере, по 5 блистеров со спиртовыми салфетками в картонной коробке |
| Регистрационное удостоверение: | UA/18362/01/01 |
| Дата начала: | 06.10.2020 |
| Дата окончания: | 01.04.2023 |
| МНН: | Filgrastim |
| Условия отпуска: | по рецепту |
| Состав: | 1 предварительно заповненений шприц (0,5 мл) содержит филграстим 480 мг |
| Фармакологическая группа: | Колониестимулирующие факторы. Филграстим. |
| Код АТХ: | L03AA02 |
| Заявитель: | Аккорд Хелскеа АГ |
| Страна заявителя: | Швейцария |
| Адрес заявителя: | Вурматштрасе 23 4103 Ботминген, Швейцария |
| Тип ЛС: | Обычный |
| ЛС биологического происхождения: | Нет |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Моно |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| L | Антинеопластические и иммуномодулирующие средства |
| L03 | Иммуностимуляторы |
| L03A | Иммуностимуляторы |
| L03AA | Колонистимулюючи факторы |
| L03AA02 |
Филграстим
|